
[分值:50分]
1.(12分)(2025·南通模拟)工业以钼精矿为原料制备MoO3的过程如下:
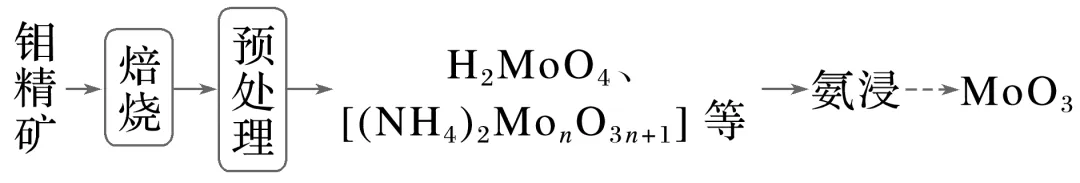
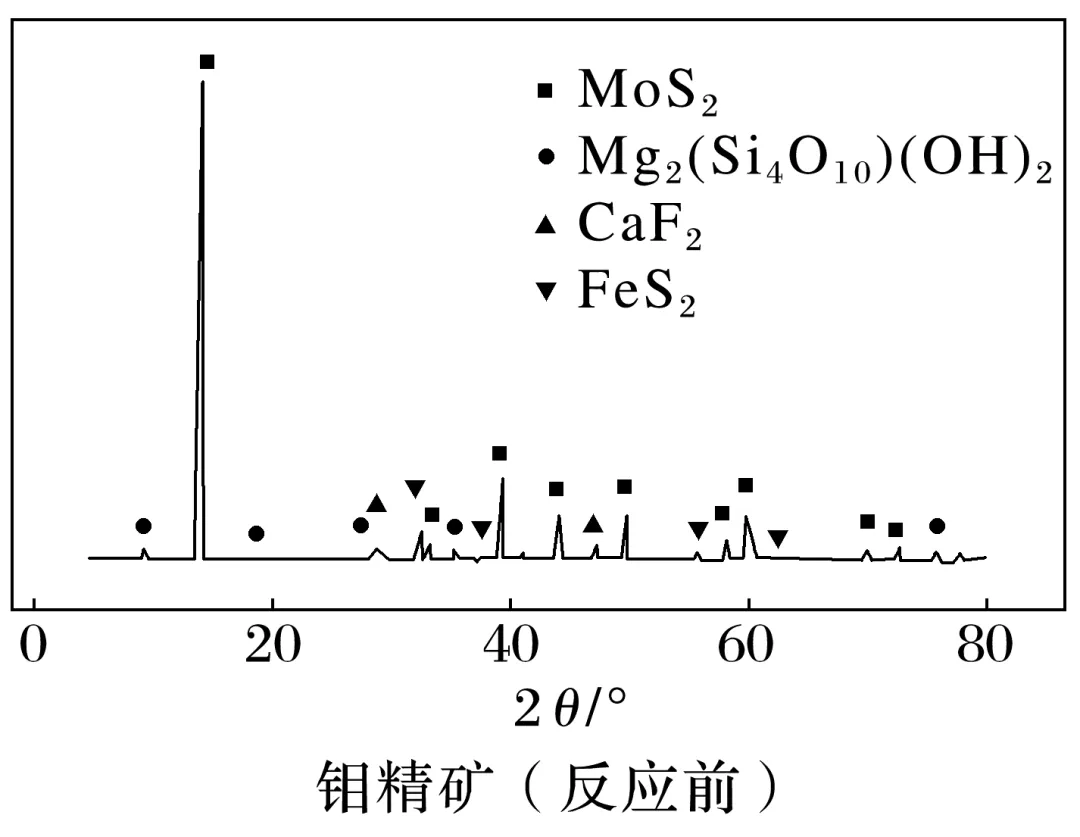
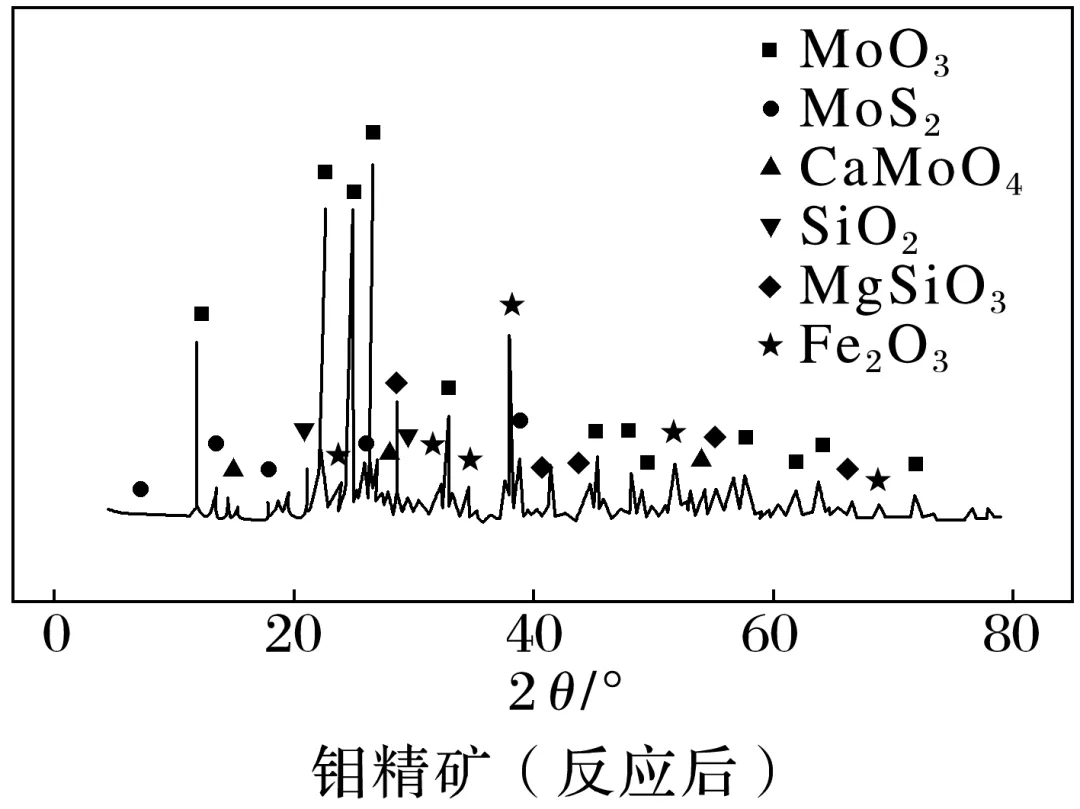
(1)“焙烧”:将钼精矿置于石英反应罐中并通入空气,高温充分反应得到钼焙砂。冷却后采用X射线衍射分析焙烧前后物相的变化如图所示。写出焙烧时生成MoO3的化学方程式:。
(2)“预处理”:将钼焙砂和HNO3、NH4NO3混合溶液按一定比例混合,加热反应一段时间,过滤后,得到含H2MoO4、多钼酸铵[(NH4)2MonO3n+1]、SiO2等滤渣。[已知(NH4)2MonO3n+1在水中存在平衡:(NH4)2MonO3n+1(s)2N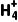 (aq)+Mo
(aq)+Mo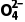 (aq)+(n-1)MoO3(s)]
(aq)+(n-1)MoO3(s)]
①“预处理”需在通风设备中进行,原因是。
②写出CaMoO4转化为(NH4)2MonO3n+1的化学方程式:。
③其他条件一定,适当增大NH4NO3浓度,所得滤渣中Mo的含量增大,原因是。
(3)“氨浸”:将预处理后所得滤渣用氨水浸泡,其中的H2MoO4、(NH4)2MonO3n+1可转化为可溶的(NH4)2MoO4,还有少量的CaMoO4难溶于氨水。为进一步提高Mo元素的浸出率,可在氨水中加入的物质是。
(4)五钼酸铵[(NH4)4Mo5O17,M=824 g·mol-1]在氮气中焙烧,可逐步分解,最终得到MoO3。取1.648 g五钼酸铵固体在氮气氛围中焙烧,有气体NH3和H2O生成,维持300 ℃时加热,当固体质量不再变化时,所得固体[组成为(NH4)aMobOc,Mo为+6价]质量为1.57 g。300 ℃所得固体的化学式为。
答案 (1)2MoS2+7O2 3+4SO2 (2)①钼焙砂和硝酸、硝酸铵混合加热反应,生成氮氧化物等有毒气体 ②nCaMoO4+2NH4NO3+(2n-2)HNO3
3+4SO2 (2)①钼焙砂和硝酸、硝酸铵混合加热反应,生成氮氧化物等有毒气体 ②nCaMoO4+2NH4NO3+(2n-2)HNO3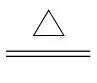 4)2MonO3n+1+nCa(NO3)2+(n-1)H2O ③(NH4)2MonO3n+1在水中存在平衡:(NH4)2MonO3n+1(s)2N
4)2MonO3n+1+nCa(NO3)2+(n-1)H2O ③(NH4)2MonO3n+1在水中存在平衡:(NH4)2MonO3n+1(s)2N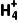 (aq)+Mo
(aq)+Mo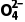 (aq)+(n-1)MoO3(s),其他条件一定,适当增大NH4NO3浓度,N
(aq)+(n-1)MoO3(s),其他条件一定,适当增大NH4NO3浓度,N 浓度增大,平衡逆向移动,析出更多的(NH4)2MonO3n+1,所得滤渣中Mo的含量增大 (3)碳酸铵 (4)(NH4)2.5Mo5O16.25
浓度增大,平衡逆向移动,析出更多的(NH4)2MonO3n+1,所得滤渣中Mo的含量增大 (3)碳酸铵 (4)(NH4)2.5Mo5O16.25
解析(2)②设(NH4)2MonO3n+1的化学计量数为1,由Ca、Mo、N 守恒得反应为nCaMoO4+2NH4NO3+xHNO3
守恒得反应为nCaMoO4+2NH4NO3+xHNO3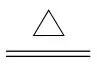 (NH4)2MonO3n+1+nCa(NO3)2+yH2O,由N原子守恒得4+x=2n+2、由H原子守恒得8+x=8+2y,解得x=2n-2、y=n-1,则CaMoO4转化为(NH4)2MonO3n+1的化学方程式为nCaMoO4+2NH4NO3+(2n-2)HNO3
(NH4)2MonO3n+1+nCa(NO3)2+yH2O,由N原子守恒得4+x=2n+2、由H原子守恒得8+x=8+2y,解得x=2n-2、y=n-1,则CaMoO4转化为(NH4)2MonO3n+1的化学方程式为nCaMoO4+2NH4NO3+(2n-2)HNO3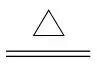 (NH4)2MonO3n+1+nCa(NO3)2+(n-1)H2O。(4)1.648g五钼酸铵的物质的量为0.002mol,五钼酸铵固体在氮气氛围中焙烧,有气体NH3和H2O生成,根据氮元素和氢元素质量守恒得到0.002×(4-a)×17+0.002×
(NH4)2MonO3n+1+nCa(NO3)2+(n-1)H2O。(4)1.648g五钼酸铵的物质的量为0.002mol,五钼酸铵固体在氮气氛围中焙烧,有气体NH3和H2O生成,根据氮元素和氢元素质量守恒得到0.002×(4-a)×17+0.002×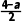 ×18g=(1.648-1.57) g,a=2.5,钼原子反应前后个数不变,则b=5,根据所得固体组成为(NH4)aMobOc,其中Mo为+6价,根据正负化合价代数和为0,则a+6b-2c=0,则c=16.25,则300℃所得固体的化学式为(NH4)2.5Mo5O16.25。
×18g=(1.648-1.57) g,a=2.5,钼原子反应前后个数不变,则b=5,根据所得固体组成为(NH4)aMobOc,其中Mo为+6价,根据正负化合价代数和为0,则a+6b-2c=0,则c=16.25,则300℃所得固体的化学式为(NH4)2.5Mo5O16.25。
2.(14分)(2025·苏北七市二模)高锰酸钾是工业和实验室常用的氧化剂,常用于物质的定性与定量分析。
(1)高锰酸钾的制备
步骤Ⅰ:称取一定质量的KOH和KClO3放入坩埚中加热,待混合物熔融后,加入一定量MnO2固体,继续加强热4~8 min后冷却,得墨绿色锰酸钾(K2MnO4)固体。
步骤Ⅱ:取步骤Ⅰ中获得的锰酸钾固体,制备高锰酸钾。
①步骤Ⅰ中发生反应的化学方程式为。
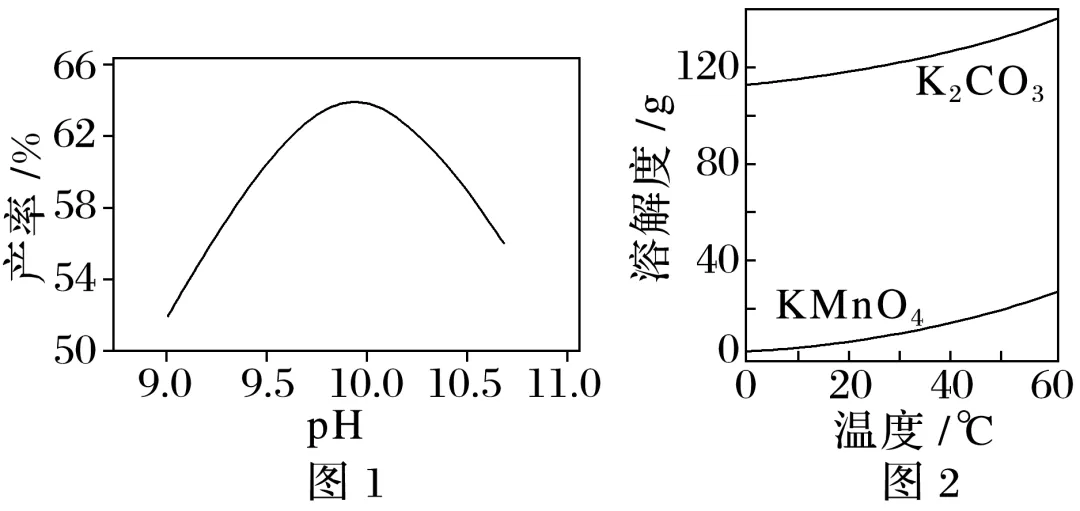
②锰酸钾在弱碱性环境发生歧化反应:3K2MnO4+2H2O===2KMnO4+MnO2↓+4KOH。不同pH对KMnO4产率影响如图1所示。KMnO4、K2CO3的溶解度随温度变化曲线如图2所示。请补充完整步骤Ⅱ中制取高锰酸钾的实验方案:取步骤Ⅰ中获得的K2MnO4固体加水溶解,,
得KMnO4固体。(实验中须使用的试剂和仪器:CO2、乙醇、pH计)
(2)数字化实验探究高锰酸钾与草酸钠反应
实验室使用0.02 mol·L-1KMnO4溶液和硫酸酸化的0.05 mol·L-1Na2C2O4溶液,进行了两种滴定实验,并记录了溶液中的氧化电势(ORP)和pH变化(已知:ORP越大,氧化性越强):
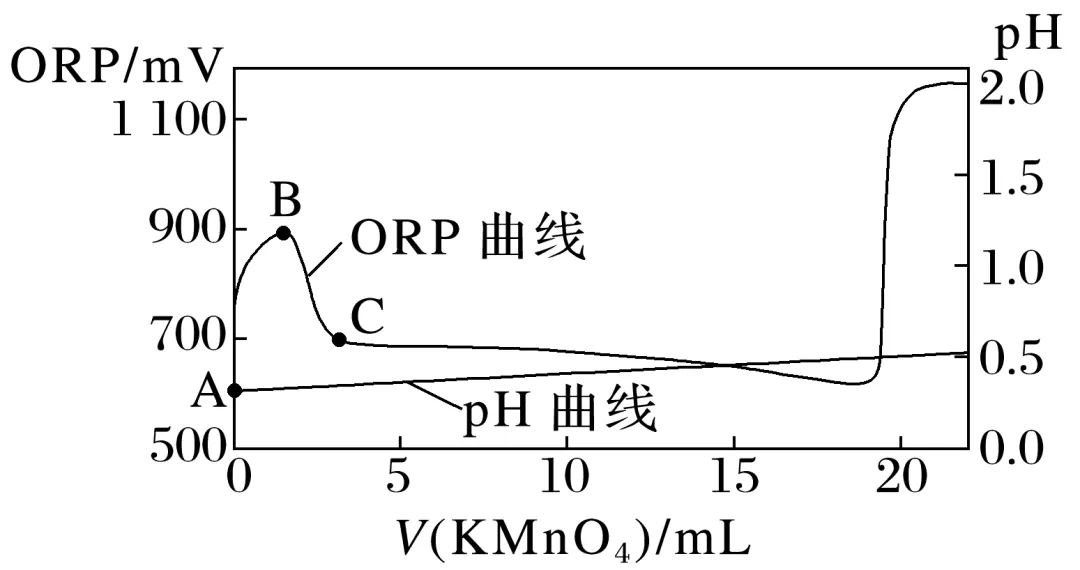
实验Ⅰ:量取20.00 mL的草酸钠溶液和10.00 mL去离子水于烧杯中,边搅拌边滴入KMnO4溶液,实验的曲线表征如图所示。
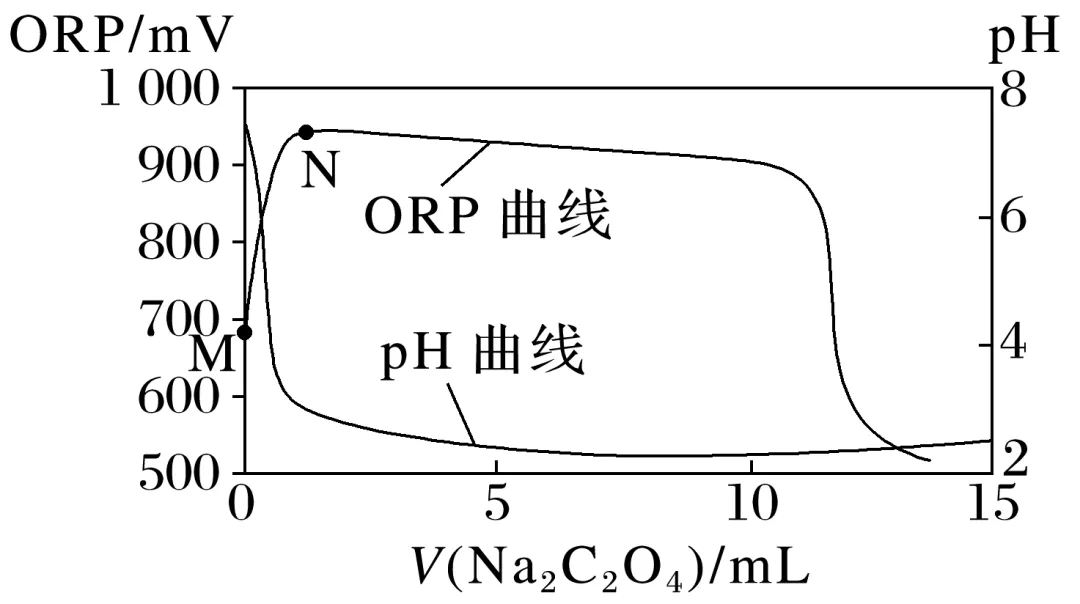
实验Ⅱ:量取6.00 mL的KMnO4溶液和20.00 mL去离子水于烧杯中,边搅拌边滴入草酸钠溶液,实验的曲线表征如图所示。
①实验Ⅰ滴定终点的现象为。
②实验Ⅰ中A→B段的反应速率较慢, 在溶液中累积,导致ORP曲线陡然增大。B→C段ORP曲线快速下降可能的原因是。
在溶液中累积,导致ORP曲线陡然增大。B→C段ORP曲线快速下降可能的原因是。
③实验Ⅱ中M→N段ORP曲线陡然增大的原因是。
④(4分)实验Ⅱ中出现滴定突跃时,理论上消耗Na2C2O4溶液的体积应为。
答案 (1)①3MnO2+KClO3+6KOH3K2MnO4+KCl+3H2O ②向溶液中通入CO2气体,用pH计测定溶液的pH,当pH在10.0时停止通入气体,过滤,将滤液加热浓缩至表面出现晶膜,停止加热,冷却结晶,过滤,用乙醇洗涤2~3次,干燥
(2)①当滴入最后半滴KMnO4溶液时,溶液由无色变为浅紫红色,且30 s内不褪色 ②产物中Mn2+起催化作用 ③酸性增强,酸性条件下的KMnO4的氧化性增强 ④6.00 mL
解析(2)①高锰酸钾与草酸钠反应离子方程式为2Mn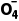 +5C2
+5C2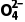 +16H+===2Mn2++10CO2↑+8H2O,高锰酸钾溶液本身为紫色,到达滴定终点时现象为当滴入最后半滴KMnO4溶液时,溶液由无色变为浅紫红色,且30s内不褪色。②实验Ⅰ中A→B段的反应速率较慢,
+16H+===2Mn2++10CO2↑+8H2O,高锰酸钾溶液本身为紫色,到达滴定终点时现象为当滴入最后半滴KMnO4溶液时,溶液由无色变为浅紫红色,且30s内不褪色。②实验Ⅰ中A→B段的反应速率较慢, 在溶液中累积,导致ORP曲线陡然增大;B→C段ORP曲线快速下降可能的原因是产物中Mn2+起催化作用,加快反应速率。④实验Ⅱ中出现滴定突跃时,理论上消耗Na2C2O4溶液的体积应为V,则0.05mol·L-1×V×
在溶液中累积,导致ORP曲线陡然增大;B→C段ORP曲线快速下降可能的原因是产物中Mn2+起催化作用,加快反应速率。④实验Ⅱ中出现滴定突跃时,理论上消耗Na2C2O4溶液的体积应为V,则0.05mol·L-1×V×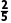 =0.02mol·L-1×6×10-3L,V=6×10-3L=6mL。
=0.02mol·L-1×6×10-3L,V=6×10-3L=6mL。
3.(12分)催化剂Mo(CO)6对于间位取代苯衍生物的合成至关重要,一种化合物H的合成路线如图:
通过网盘分享的文件:word讲义【更新联系lymsummers】等2个文件
链接: https://pan.baidu.com/s/1RCL2uLZQuQ-rZUf2_ekrWg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享