
一、沉淀重量分析法的应用与计算
沉淀重量分析法测定硫酸铜晶体的纯度
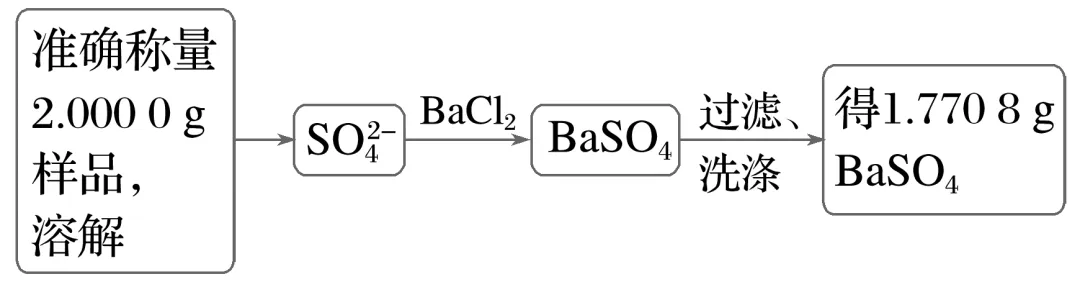
(1)如何判断S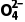 已被沉淀完全?。
已被沉淀完全?。
(2)洗涤沉淀BaSO4的操作是。
(3)判断沉淀已洗涤干净的方法是。
(4)根据数据计算产品纯度为。
答案 (1)静置,向上层清液中继续滴加少量BaCl2溶液,若无沉淀产生,则证明,S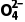 已沉淀完全 (2)沿玻璃棒向漏斗中注入蒸馏水至浸没沉淀,静置,待水自然流出后,重复操作2~3次 (3)取最后一次洗涤液于试管中,先滴加稀硝酸酸化,再滴加AgNO3溶液,若无白色沉淀产生则沉淀已洗涤干净 (4)95%
已沉淀完全 (2)沿玻璃棒向漏斗中注入蒸馏水至浸没沉淀,静置,待水自然流出后,重复操作2~3次 (3)取最后一次洗涤液于试管中,先滴加稀硝酸酸化,再滴加AgNO3溶液,若无白色沉淀产生则沉淀已洗涤干净 (4)95%
解析(4)w(CuSO4·5H2O)=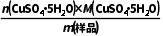 =
=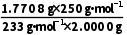 ×100%=95%。
×100%=95%。
二、热重法
命题特点:结合热重曲线定量分析物质失去结晶水或分解失重的过程。
方法技巧:
1.失重过程
一般含有结晶水的样品在受热过程中,一失氢键结合水,二失配位键结合水,三失其他非金属元素形成的气体。
2.计算原则
(1)金属元素始终残留在固体中,且质量守恒。
(2)挥发出的气体中的非金属元素与样品中对应元素质量守恒。
3.“五步法”厘清热重曲线解题思路
第一步 “设”:设晶体的物质的量为1 mol。
第二步 “算”:找出曲线中每步剩余固体的质量m余或根据数据计算每步剩余固体的质量m余[ ×100%=固体残留率]。
×100%=固体残留率]。
第三步 “失”:加热时,晶体一般是先失结晶水,再失非金属氧化物。
第四步 “稳”:晶体中金属质量不减少,仍在m余中。
第五步 “定”:失重最后得到的固体物质一般为金属氧化物,结合金属氧化物的相对分子质量和原晶体质量以及固体残留率可计算出金属氧化物中O的个数,进而可求出最终固体物质的化学式(元素物质的量之比为化学式中角标之比)。
 对点训练
对点训练
1.测定胆矾(CuSO4·nH2O)晶体中结晶水的含量
(1)称量干燥坩埚的质量为m1,加入胆矾后总质量为m2,将坩埚加热至胆矾全部变为白色,置于干燥器中冷却至室温后称量,重复上述操作,最终总质量恒定为m3。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。
(2)下列操作中,会导致结晶水数目测定值偏高的是(填标号)。
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少胆矾迸溅出来
答案 (1)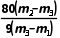 (2)①③
(2)①③
解析(1)称量干燥坩埚的质量为m1,加入胆矾后总质量为m2,将坩埚加热至胆矾全部变为白色,置于干燥器中冷却至室温后称量,重复上述操作,最终总质量恒定为m3。则水的质量是(m2-m3) g,所以胆矾(CuSO4·nH2O)中n值的表达式为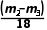 ∶
∶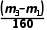 =n∶1,解得n=
=n∶1,解得n=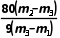 。
。
(2) ①胆矾未充分干燥,导致所测m2偏大,根据n=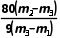 可知,最终会导致结晶水数目测定值偏高,符合题意;②坩埚未置于干燥器中冷却,部分白色硫酸铜会与空气中水蒸气结合重新生成胆矾,导致所测m3偏大,根据n=
可知,最终会导致结晶水数目测定值偏高,符合题意;②坩埚未置于干燥器中冷却,部分白色硫酸铜会与空气中水蒸气结合重新生成胆矾,导致所测m3偏大,根据n=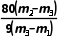 可知,最终会导致结晶水数目测定值偏低,不符合题意;③加热胆矾晶体时有晶体从坩埚中溅出,会使m3数值偏小,根据n=
可知,最终会导致结晶水数目测定值偏低,不符合题意;③加热胆矾晶体时有晶体从坩埚中溅出,会使m3数值偏小,根据n=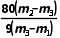 可知,最终会导致结晶水数目测定值偏高,符合题意。
可知,最终会导致结晶水数目测定值偏高,符合题意。
2.(2025·南京二模)铜阳极泥(含Cu、Ag、Au、Pd等)中回收贵金属的工艺流程如下:
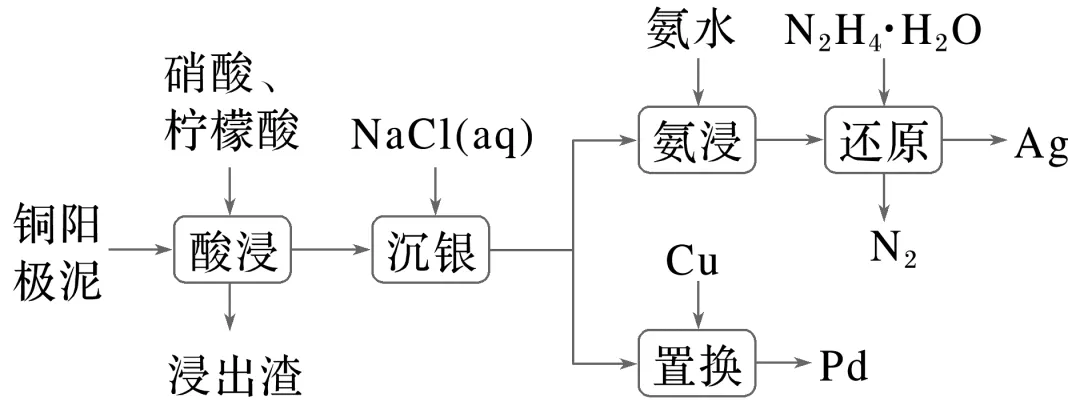
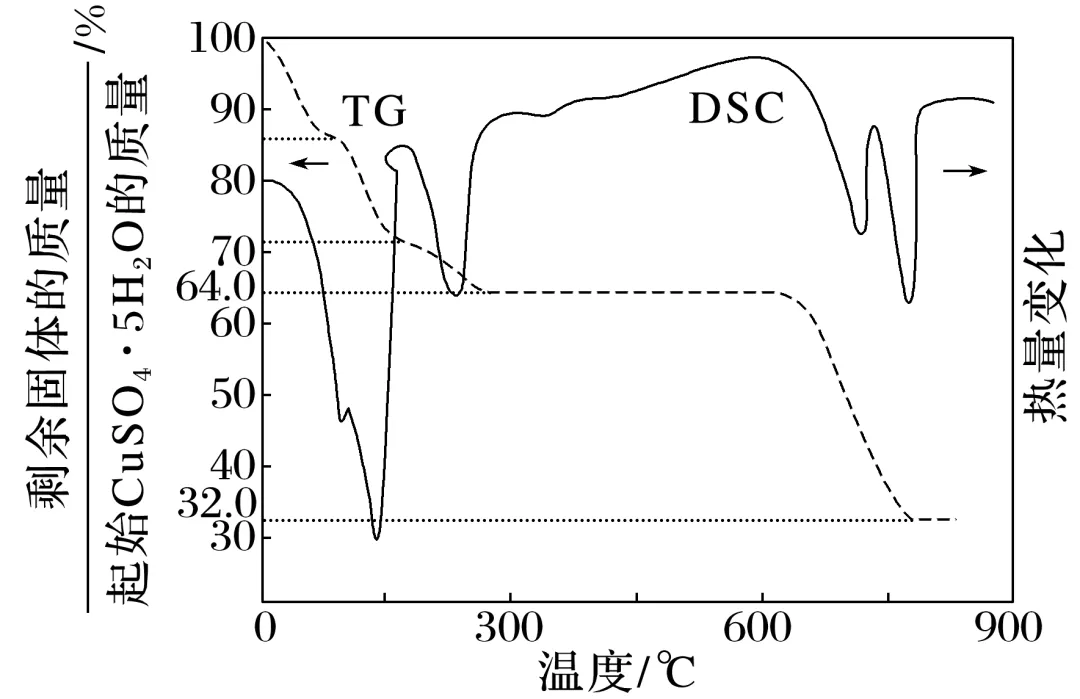
“置换”后的溶液可制备CuSO4·5H2O晶体,该晶体分解的TG曲线(热重)及DSC曲线(热量变化)如图所示。DSC曲线上650~850 ℃有两个吸热峰,可能发生的吸热反应为CuSO4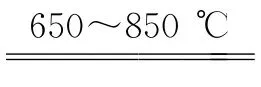 3↑、。
3↑、。
答案 2SO3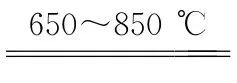 2+O2
2+O2
解析 DSC曲线上650~850℃有两个吸热峰,说明此时CuSO4发生热分解反应,从TG 图像可以看出,质量减少量为原CuSO4质量的一半,说明有固体CuO剩余,还有其他气体产出,此时气体产物为SO2、SO3、 O2,可能出现的化学方程式为CuSO4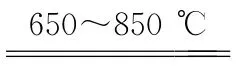 3↑、2SO3
3↑、2SO3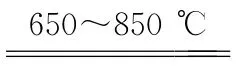 2+O2。
2+O2。
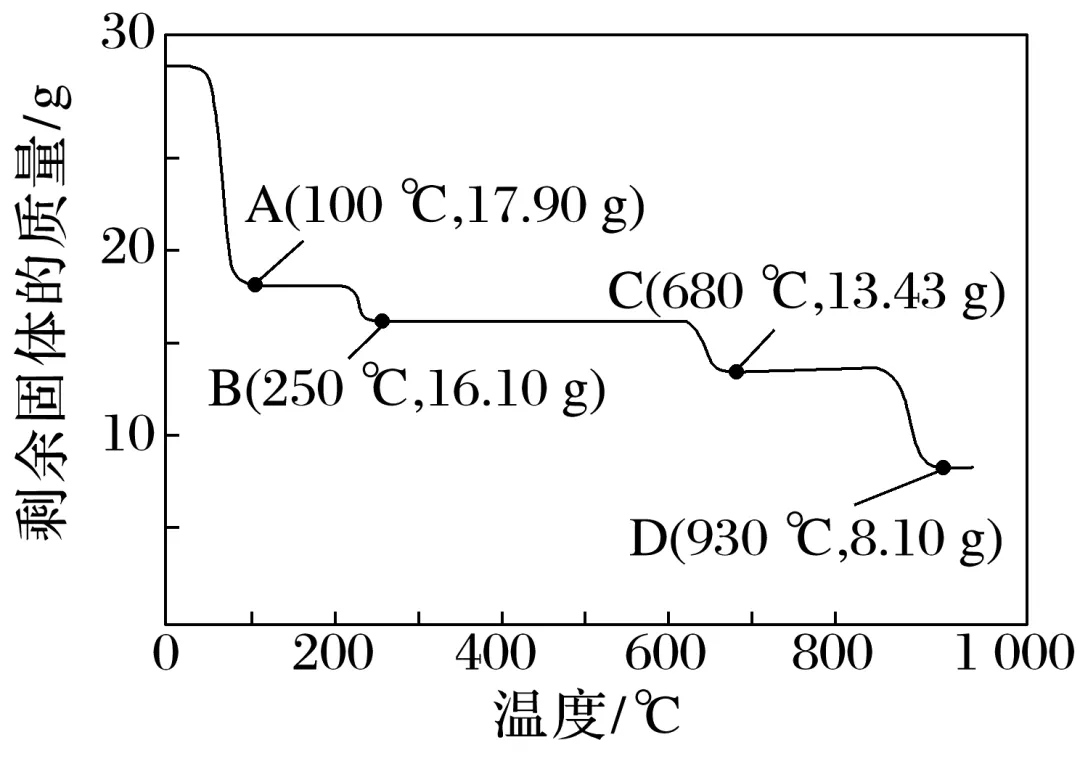
3.(2025·南京、盐城一模)加热28.7 g ZnSO4·7H2O晶体,测得加热过程中剩余固体的质量随温度的变化关系如图所示。A点物质为(填化学式)。
答案 ZnSO4·H2O
解析 28.7gZnSO4·7H2O的物质的量为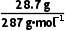 =0.1mol,A点物质的质量为17.9g,失去水的质量为10.8g,即0.6mol水,所以A点物质为ZnSO4·H2O。
=0.1mol,A点物质的质量为17.9g,失去水的质量为10.8g,即0.6mol水,所以A点物质为ZnSO4·H2O。
4.(2024·南京学情调研)2ZnCO3·3Zn(OH)2·2H2O固体在加热升温过程中的质量变化如图所示。
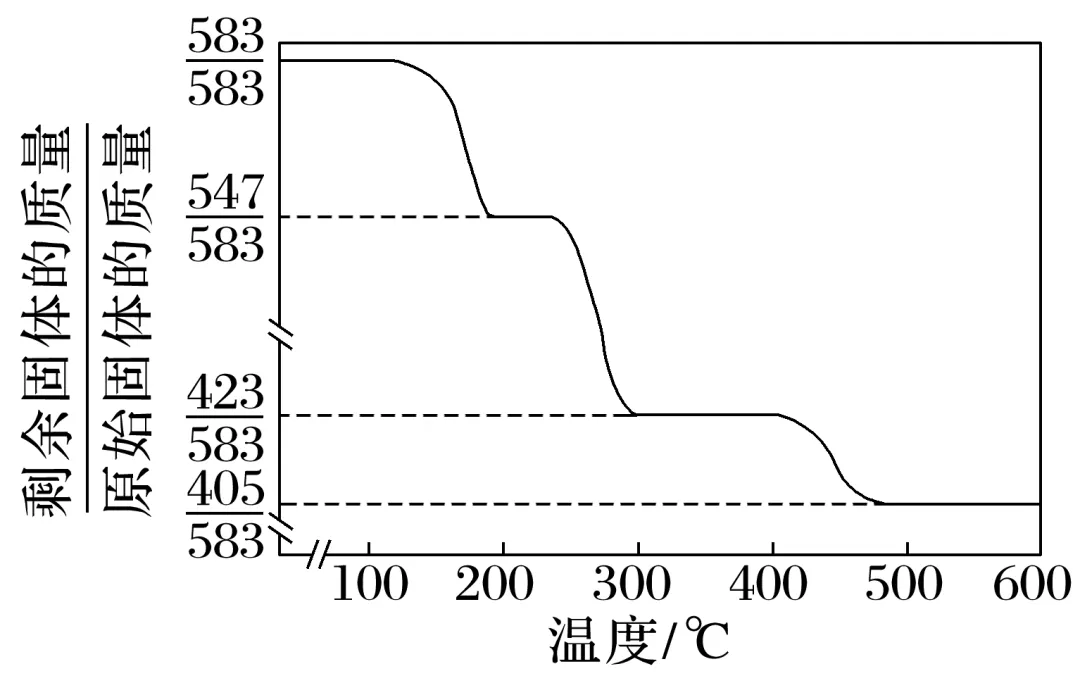
回答下列问题:
(1)350 ℃时,剩余固体中已不含碳元素,则剩余固体中含有(填化学式)。
(2)整个过程的总反应方程式为。
答案 (1)ZnO和Zn(OH)2
(2)2ZnCO3·3Zn(OH)2·2H2O5ZnO+5H2O+2CO2↑
解析
通过网盘分享的文件:word讲义【更新联系lymsummers】等2个文件
链接: https://pan.baidu.com/s/1RCL2uLZQuQ-rZUf2_ekrWg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享