

1.金属的腐蚀
(1)本质:金属原子失去电子变为金属阳离子,金属发生氧化反应。
(2)类型
①化学腐蚀与电化学腐蚀
类型 | 化学腐蚀 | 电化学腐蚀 |
条件 | 金属与其表面接触的一些物质(如O2、Cl2、SO2等)直接反应而引起的腐蚀 | 不纯金属与电解质溶液接触发生原电池反应 |
现象 | 无电流产生 | 有微弱电流产生 |
本质 | 金属被氧化 | 较活泼金属被氧化 |
联系 | 两者往往同时发生,电化学腐蚀更普遍 |
②析氢腐蚀与吸氧腐蚀(以钢铁的腐蚀为例)
类型 | 析氢腐蚀 | 吸氧腐蚀 |
条件 | 水膜酸性较强(pH≤4.3) | 水膜酸性很弱或呈中性 |
电极反应 | 负极 | Fe-2e-===Fe2+ |
正极 | 2H++2e-===H2↑ | O2+2H2O+4e-===4OH- |
总反应式 | Fe+2H+===Fe2++H2↑ | 2Fe+O2+2H2O===2Fe(OH)2 |
联系 | 吸氧腐蚀更普遍 |
(3)金属腐蚀快慢的一般规律
①对同一电解质溶液来说,腐蚀由快到慢:电解池原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护措施的腐蚀。
②活泼性不同的两种金属,活泼性差异越大,较活泼的金属腐蚀越快。
③对同一种电解质溶液,一般来说电解质溶液浓度越大,金属腐蚀越快。
2.金属的防护
(1)电化学保护法
①牺牲阳极法——原电池原理
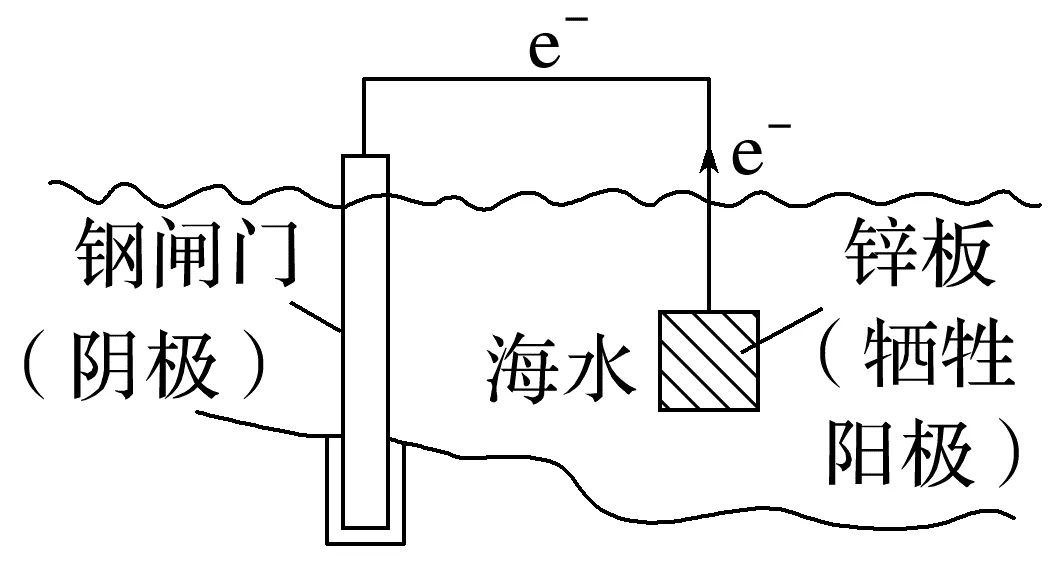
被保护的金属作原电池的正极(阴极),活泼金属作原电池的负极(阳极),阳极要定期检查更换。②外加电流法——电解池原理
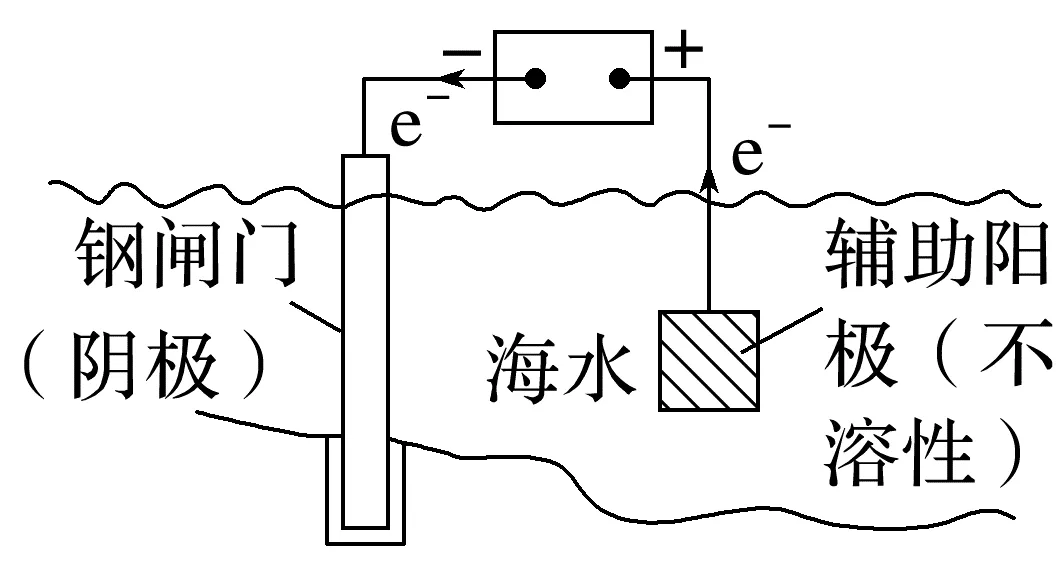
将被保护的金属与电源负极相连,作电解池的阴极,另一惰性电极与电源正极相连,作辅助阳极。
(2)改变金属材料的组成,如制成合金、不锈钢等。
(3)在金属表面覆盖保护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。

1.(2024·广东,5)我国自主设计建造的浮式生产储油装置“海葵一号”将在珠江口盆地海域使用,其钢铁外壳镶嵌了锌块,以利用电化学原理延缓外壳的腐蚀。下列有关说法正确的是( )
A.钢铁外壳为负极
B.镶嵌的锌块可永久使用
C.该法为外加电流法
D.锌发生反应:Zn-2e-===Zn2+
答案 D
解析由于金属活动性:Zn>Fe,钢铁外壳为正极,锌块为负极,故A错误;Zn失去电子,发生氧化反应:Zn-2e-===Zn2+,镶嵌的锌块会被逐渐消耗,需根据腐蚀情况进行维护和更换,不能永久使用,故B错误、D正确;该方法为牺牲阳极法,故C错误。
2.(2022·广东,11)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的3% NaCl溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是( )
A.加入AgNO3溶液产生沉淀
B.加入淀粉碘化钾溶液无蓝色出现
C.加入KSCN溶液无红色出现
D.加入K3[Fe(CN)6]溶液无蓝色沉淀生成
答案 D
解析将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中,会构成原电池,由于锌比铁活泼,锌作原电池的负极,铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶液反应产生氢气,溶液中会有亚铁离子生成。氯化钠溶液中始终存在氯离子,所以加入硝酸银溶液后,不管铁片是否被腐蚀,均会出现白色沉淀,故A不符合题意;淀粉碘化钾溶液可检测氧化性物质,但不论铁片是否被腐蚀,均无氧化性物质生成,故B不符合题意;KSCN溶液可检测铁离子的存在,上述过程中不会出现铁离子,所以无论铁片是否被腐蚀,加入KSCN溶液后,均无红色出现,故C不符合题意;K3[Fe(CN)6]溶液是用于检测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会生成亚铁离子,则加入K3[Fe(CN)6]溶液就不会出现蓝色沉淀,故D符合题意。
3.(2024·湖北,2)2024年5月8日,我国第三艘航空母舰福建舰顺利完成首次海试。舰体表面需要采取有效的防锈措施,下列防锈措施中不形成表面钝化膜的是( )
A.发蓝处理B.阳极氧化
C.表面渗镀D.喷涂油漆
答案 D
解析发蓝处理技术通常用于钢铁等黑色金属,通过在空气中加热或直接浸泡于浓氧化性溶液中来实现,可在金属表面形成一层极薄的氧化膜,这层氧化膜能有效防锈,A不符合题意;阳极氧化是将待保护的金属与电源正极连接,在金属表面形成一层氧化膜的过程,B不符合题意;表面渗镀是在高温下将气态、固态或熔化状态的欲渗镀的物质(金属或非金属元素)通过扩散作用从被渗镀的金属的表面渗入内部以形成表层合金镀层的一种表面处理的方法,C不符合题意;喷涂油漆是将油漆涂在待保护的金属表面,并没有在其表面形成钝化膜,D符合题意。
4.(2024·浙江6月选考,13)金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有关。下图为两种对海水中钢闸门的防腐措施示意图:
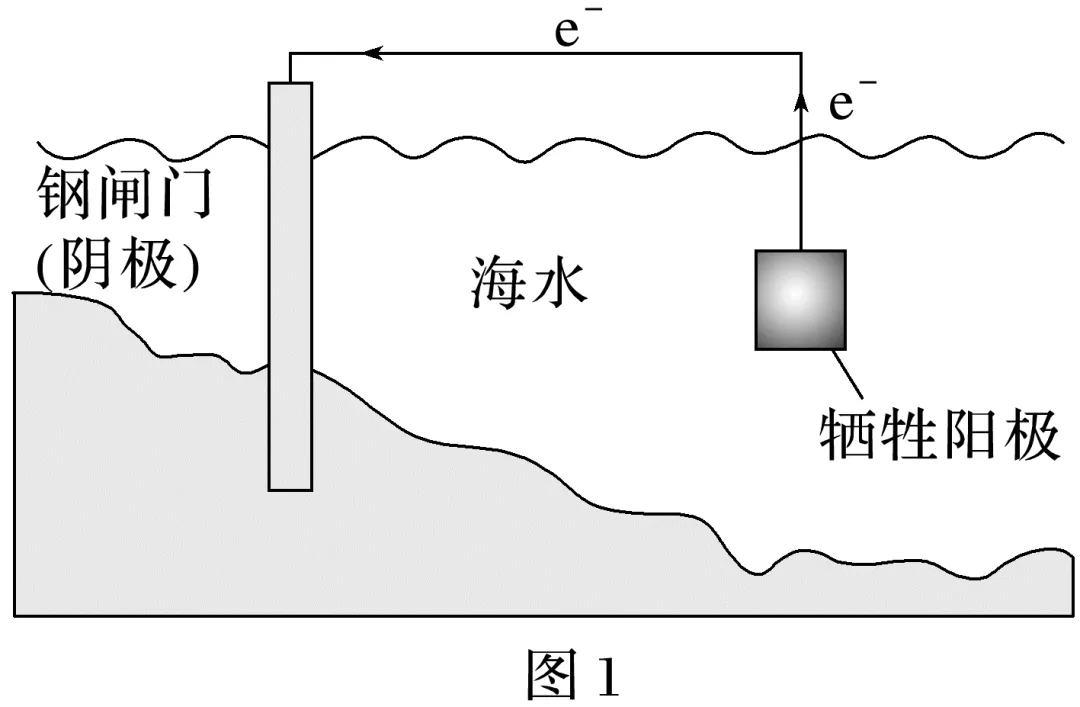
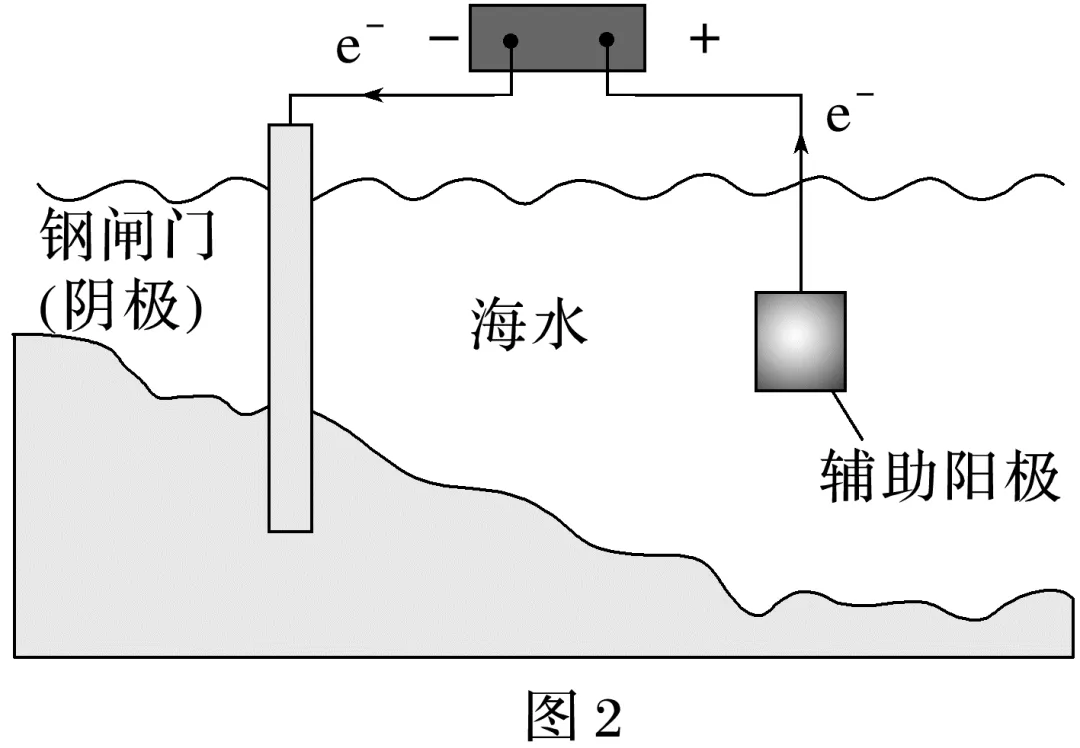
下列说法正确的是( )
A.图1、图2中,阳极材料本身均失去电子
B.图2中,外加电压偏高时,钢闸门表面可发生反应:O2+4e-+2H2O===4OH-
C.图2中,外加电压保持恒定不变,有利于提高对钢闸门的防护效果
D.图1、图2中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应
答案 B
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享