
一、实验现象的描述
 例1 [2025·江苏,16(2)节选]文物表面凝结物种类受文物材质和海洋环境等因素的影响。
例1 [2025·江苏,16(2)节选]文物表面凝结物种类受文物材质和海洋环境等因素的影响。
有氧环境中,海水中的铁质文物表面形成FeOOH等凝结物。
铁在盐水中腐蚀的可能原理如图所示。依据原理设计如下实验:向NaCl溶液中加入K3[Fe(CN)6]溶液(能与Fe2+形成蓝色沉淀)和酚酞,将混合液滴到生铁片上。预测该实验的现象为。
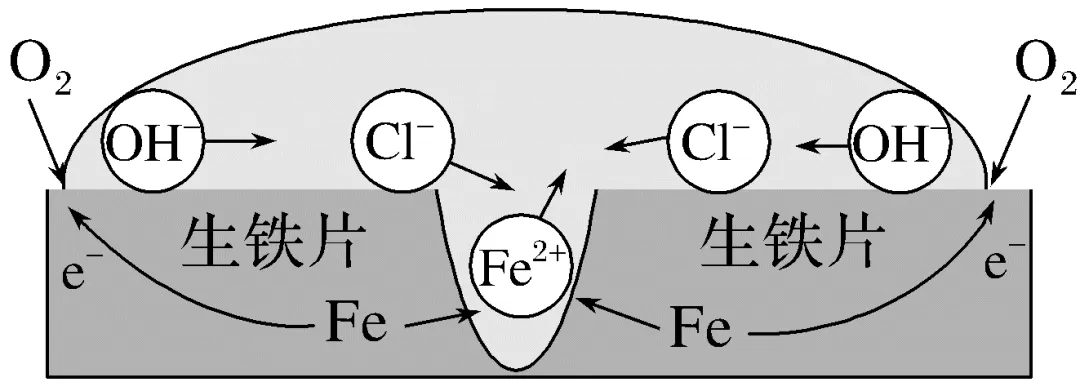
答案 液滴边缘形成红色环,生铁片中心产生蓝色沉淀
 例2 探究绿矾的热分解产物,某化学实验小组用如图所示装置进行实验(夹持仪器略)。
例2 探究绿矾的热分解产物,某化学实验小组用如图所示装置进行实验(夹持仪器略)。
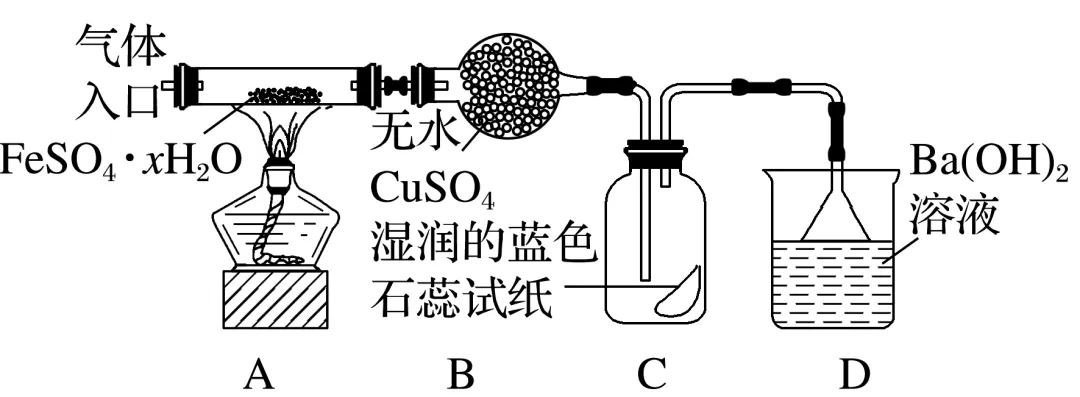
在实验过程中,观察到A中固体变红棕色,B中的现象:;
C中试纸的颜色变化是。
答案 固体由白色变为蓝色 由蓝色变为红色
解析在实验过程中,无水硫酸铜吸水,生成硫酸铜晶体,SO3、SO2都是酸性气体,能使湿润的蓝色石蕊试纸变红。
 对点训练
对点训练
1.[2024·湖南,15(3)节选]亚铜配合物广泛用作催化剂。实验室制备[Cu(CH3CN)4]ClO4的反应原理如下:Cu(ClO4)2·6H2O+Cu+8CH3CN===2[Cu(CH3CN)4]ClO4+6H2O。实验步骤如下:
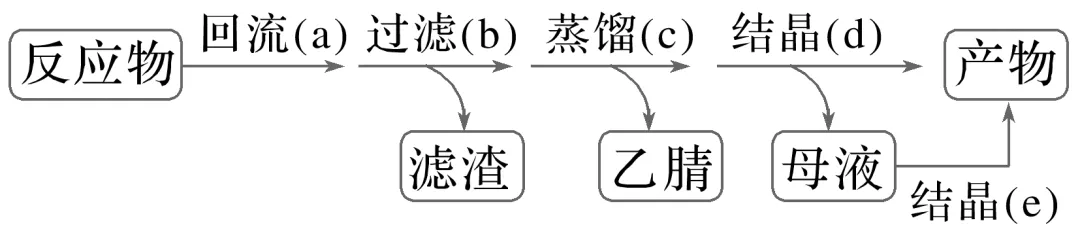
分别称取3.71 g Cu(ClO4)2·6H2O和0.76 g Cu粉置于100 mL乙腈(CH3CN)中反应,回流装置图(加热、夹持等装置略)如下:
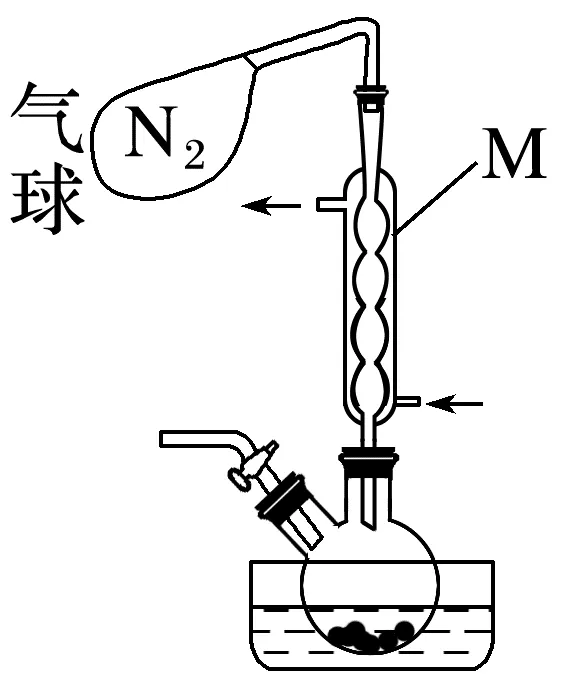
已知:①乙腈是一种易挥发的强极性配位溶剂;②相关物质的信息如下:
化合物 | [Cu(CH3CN)4]ClO4 | Cu(ClO4)2·6H2O |
相对分子质量 | 327.5 | 371 |
在乙腈中颜色 | 无色 | 蓝色 |
装置中反应完全的现象是。
答案 溶液蓝色褪去变为无色
2.[2024·天津,15(2)]写出蛋壳主要成分与醋酸反应的离子方程式,
此反应的实验现象是。
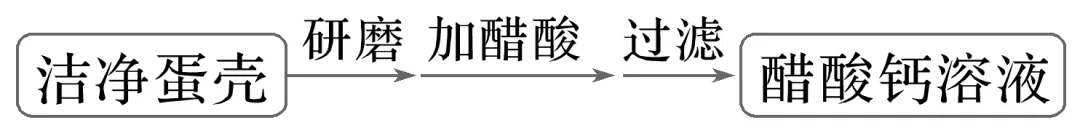
答案 CaCO3+2CH3COOH===Ca2++2CH3COO-+H2O+CO2↑ 蛋壳溶解,有气泡产生
3.实验室可利用Na2S2O8溶液来检验阳极液中是否含有Mn2+,反应的离子方程式为2Mn2++5S2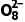 +8H2O===16H++10S
+8H2O===16H++10S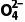 +2Mn
+2Mn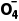 ,则Na2S2O8溶液可盛放于(填“酸式”或“碱式”)滴定管中,确认阳极液中Mn2+已反应完全的现象是。
,则Na2S2O8溶液可盛放于(填“酸式”或“碱式”)滴定管中,确认阳极液中Mn2+已反应完全的现象是。
答案 酸式 滴加Na2S2O8溶液,溶液不变紫色
二、控制反应条件及操作描述
 总体策略
总体策略
紧扣实验目的→联系物质性质→逻辑链条书写完整(不仅要答出“防止什么”,最好能点明“为什么要防止这个”)→答题时尽量考虑全面(一个操作或条件往往有多个目的)
 常见操作
常见操作
1.温度控制的目的
(1)加热的目的:增大化学反应速率或使化学平衡向某方向移动。
(2)降温的目的:防止某物质在高温时分解或使化学平衡向某方向移动。
(3)控制温度在一定范围的目的:若温度过低,则反应速率较小;若温度过高,则物质(如H2O2、氨水、草酸、浓硝酸、铵盐等)会分解或挥发。
(4)水浴加热的好处:受热均匀,温度可控,且温度不超过100 ℃。
(5)冰水浴冷却的目的:防止物质分解或挥发。
(6)趁热过滤的原因:保持过滤温度,防止温度降低后物质析出。
(7)减压蒸发的原因:减压蒸发降低了蒸发温度,可以防止物质分解或失去结晶水。
2.通入非反应物气体的作用
(1)实验开始前通入气体
实验开始前通入非反应物气体的主要作用是除去装置中的空气,防止实验物质与空气中的成分(如O2、CO2、H2O等)反应,若是定量的实验还要防止空气中成分影响被测气体量,减小误差等。
(2)实验过程中通入气体
实验过程中通入非反应物气体,是为了使反应顺利进行,其主要作用有:
①稀释反应气体,降低反应速率,使其充分反应。
②搅拌作用。
③使产物从反应容器中转移出去。
④作为保护气:防止外界气体进入反应;抑制反应进行,如抑制水解。
(3)实验结束后通入气体
实验结束后,通入非反应物气体最重要的目的是保护已有成果和实验的精确性。其主要作用有:
①使产生的气体全部逸出。
②作保护气,防止空气进入。
 对点训练
对点训练
1.(2025·南通模拟)制备K3[Fe(C2O4)3]·3H2O。将FeC2O4·2H2O加入如图所示的三颈烧瓶中(部分仪器略去),加入饱和K2C2O4溶液,维持温度在40 ℃左右,缓缓滴加过量H2O2溶液,滴加完后,加热溶液至微沸状态持续1 min。冷却后,加入H2C2O4溶液,浓缩结晶得到K3[Fe(C2O4)3]·3H2O。
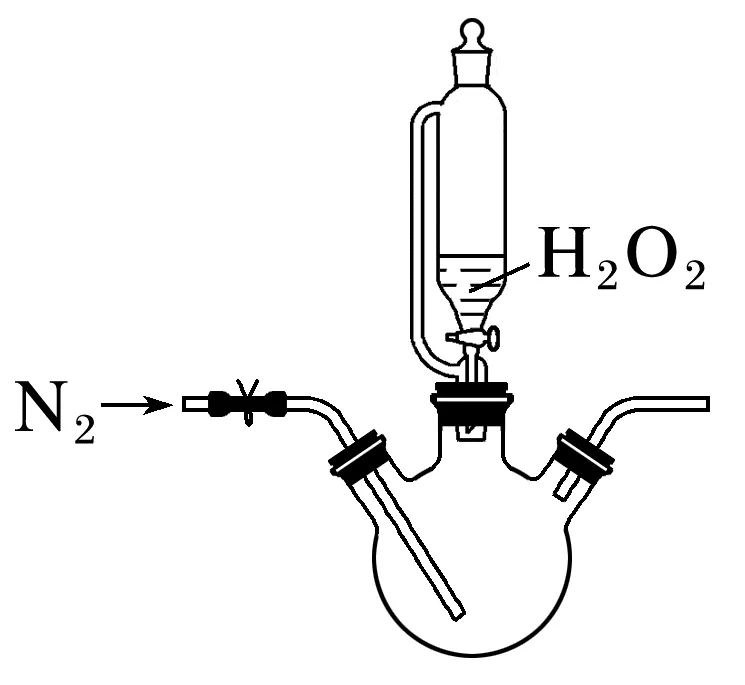
(1)实验过程中持续通入N2的目的是。
(2)先维持温度在40 ℃左右,后加热至微沸,其主要目的是。
答案 (1)搅拌,加快反应速率,使反应更充分 (2)维持温度在40 ℃左右,既可加快反应速率,也可防止H2O2分解;加热至微沸可除去过量的H2O2
2.某化学小组在实验室模拟用软锰矿粉(主要成分为MnO2)制备MnCO3,过程如下(部分操作和条件略)。已知:MnCO3不溶于水和乙醇,在干燥空气中稳定,潮湿时易被氧化。
(1)制备MnSO4溶液:m g软锰矿粉经除杂后制得MnO2浊液,向MnO2浊液中通入SO2,制得MnSO4溶液,实验装置如下图所示(夹持和加热装置略)。
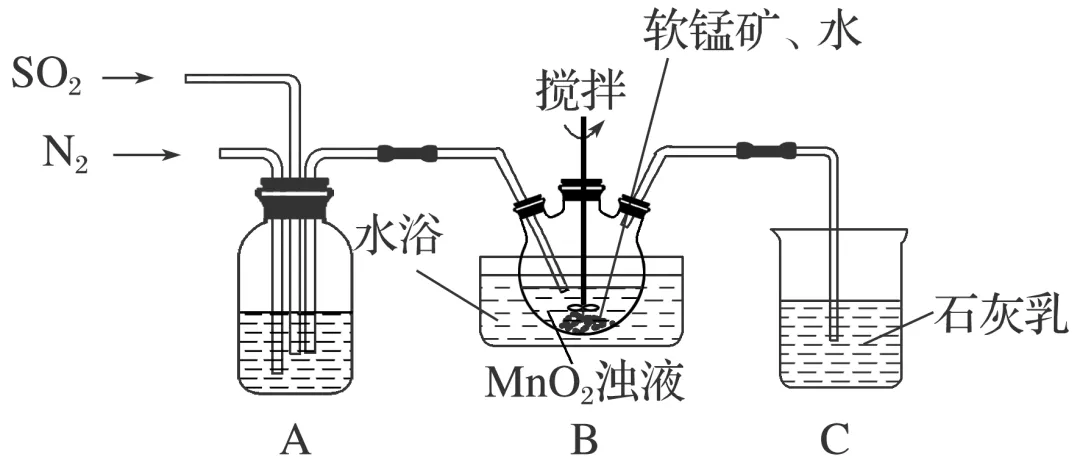
通过装置A可观察通入SO2与N2的快慢,则A中加入的最佳试剂是;为使SO2尽可能转化完全,在停止实验前应进行的操作是;
实验中若将N2换成空气,将导致S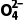 浓度明显大于Mn2+浓度,原因是。
浓度明显大于Mn2+浓度,原因是。
(2)制备MnCO3固体:在搅拌下向MnSO4溶液中缓慢滴加NH4HCO3溶液,过滤,分别用蒸馏水和乙醇洗涤,低于100 ℃干燥,得到MnCO3固体。若用同浓度的Na2CO3溶液代替NH4HCO3溶液,将导致制得的MnCO3产品中混有(填化学式);用乙醇洗涤的目的是。 
通过网盘分享的文件:word讲义【更新联系lymsummers】等2个文件
链接: https://pan.baidu.com/s/1RCL2uLZQuQ-rZUf2_ekrWg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享