
一、分子极性
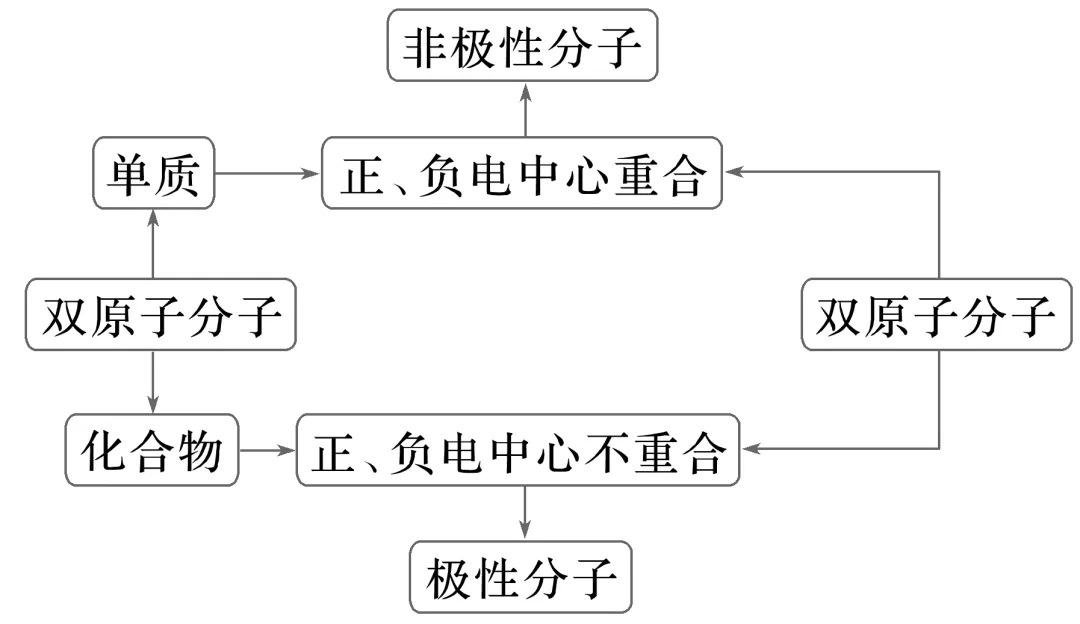
1.极性分子与非极性分子的判断
2.分子极性对物质溶解性的影响
“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。“相似相溶”还适用于分子结构的相似性,如在水中溶解度:乙醇>戊醇。
 对点训练
对点训练
1.在H2S、BF3、PCl3、CS2、CCl4、C2H4、N2H4、P4、HCN、苄氯()分子中:
(1)以非极性键结合的非极性分子是。
(2)以极性键相结合,具有直线形结构的非极性分子是。
(3)以极性键相结合,具有直线形结构的极性分子是。
(4)以极性键相结合,具有三角锥形结构的极性分子是。
(5)以极性键相结合,具有正四面体结构的非极性分子是。
(6)以极性键相结合,具有V形结构的极性分子是。
(7)以极性键相结合,具有平面正三角形结构的非极性分子是。
(8)既含极性键又含非极性键的非极性分子是。
(9)既含极性键又含非极性键的极性分子是。
答案 (1)P4 (2)CS2 (3)HCN (4)PCl3 (5)CCl4 (6)H2S (7)BF3 (8)C2H4 (9)N2H4、苄氯
2.下列现象中,不能用“相似相溶”规律解释的是(填字母)。
A.HCl易溶于H2O
B.Cl2易溶于NaOH溶液
C.Br2易溶于CCl4
D.I2易溶于CS2
答案 B
解析 HCl是极性分子,H2O是极性溶剂,HCl易溶于H2O能用“相似相溶”规律解释,A不符题意;Cl2易溶于NaOH溶液主要是Cl2与NaOH溶液反应所致,不能用“相似相溶”规律解释,B符合题意;Br2是非极性分子,CCl4是非极性溶剂,Br2易溶于CCl4能用“相似相溶”规律解释,C不符题意;I2是非极性分子,CS2是非极性溶剂,I2易溶于CS2能用“相似相溶”规律解释,D不符题意。
二、氢键
1.氢键的存在与形成
氢键通常用X—H…Y表示,氢键强弱与X和Y的吸引电子的能力有关,一般X、Y元素吸引电子能力越强(即电负性越大),则氢键越强。氢键强弱变化顺序为F—H…F>O—H…O>O—H…N>N—H…N。
2.氢键的类型
分子间氢键使物质熔、沸点升高,如;分子内氢键,如。
3.与氢键有关的答题模板
(1)熔、沸点:X分子与X分子之间存在氢键,导致其熔、沸点偏高。
(2)溶解度:X分子与水之间存在氢键,导致X在水中的溶解度偏大。
 对点训练
对点训练
氢键与物质性质的关系问题解答。
(1)苯胺()与甲苯()的相对分子质量相近,但苯胺的熔点(-5.9 ℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0 ℃)、沸点(110.6 ℃),原因是。
答案 苯胺分子间存在氢键,而甲苯分子间仅存在范德华力,苯胺的熔点和沸点显著高于甲苯
(2)[2024·山东,16(4)]FDCA()的熔点远大于HMF(),除相对分子质量存在差异外,另一重要原因是。
答案 FDCA形成的分子间氢键更多
(3)的沸点比高,原因是。
答案 形成分子内氢键,而形成分子间氢键,分子间氢键使分子间作用力增大,沸点升高
(4)已知苯酚()具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子能形成分子内氢键。据此判断,相同温度下,电离平衡常数Ka2(水杨酸)(填“>”或“<”)Ka(苯酚),其原因是。
答案 < —COO-与—OH形成分子内氢键,使其更难电离出H+
(5)硼酸晶体是片层结构,其中一层的结构如图所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是。
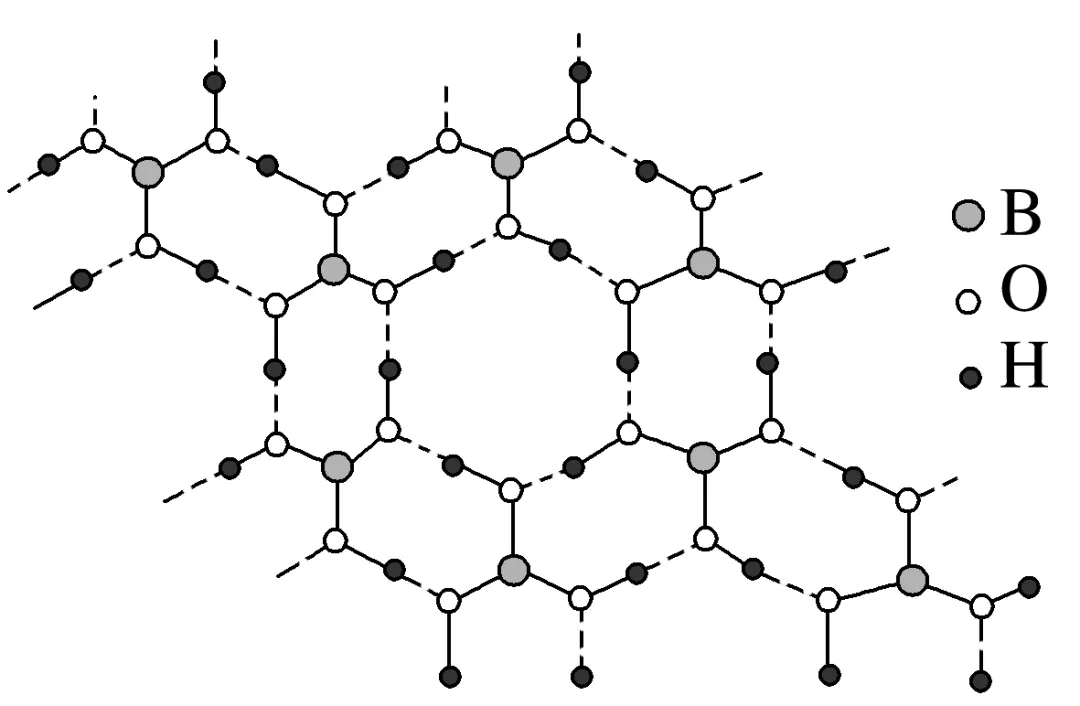
答案 晶体中硼酸分子间以氢键缔合在一起,难以溶解;加热时,晶体中部分氢键被破坏,硼酸分子与水分子形成氢键,溶解度增大
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享