
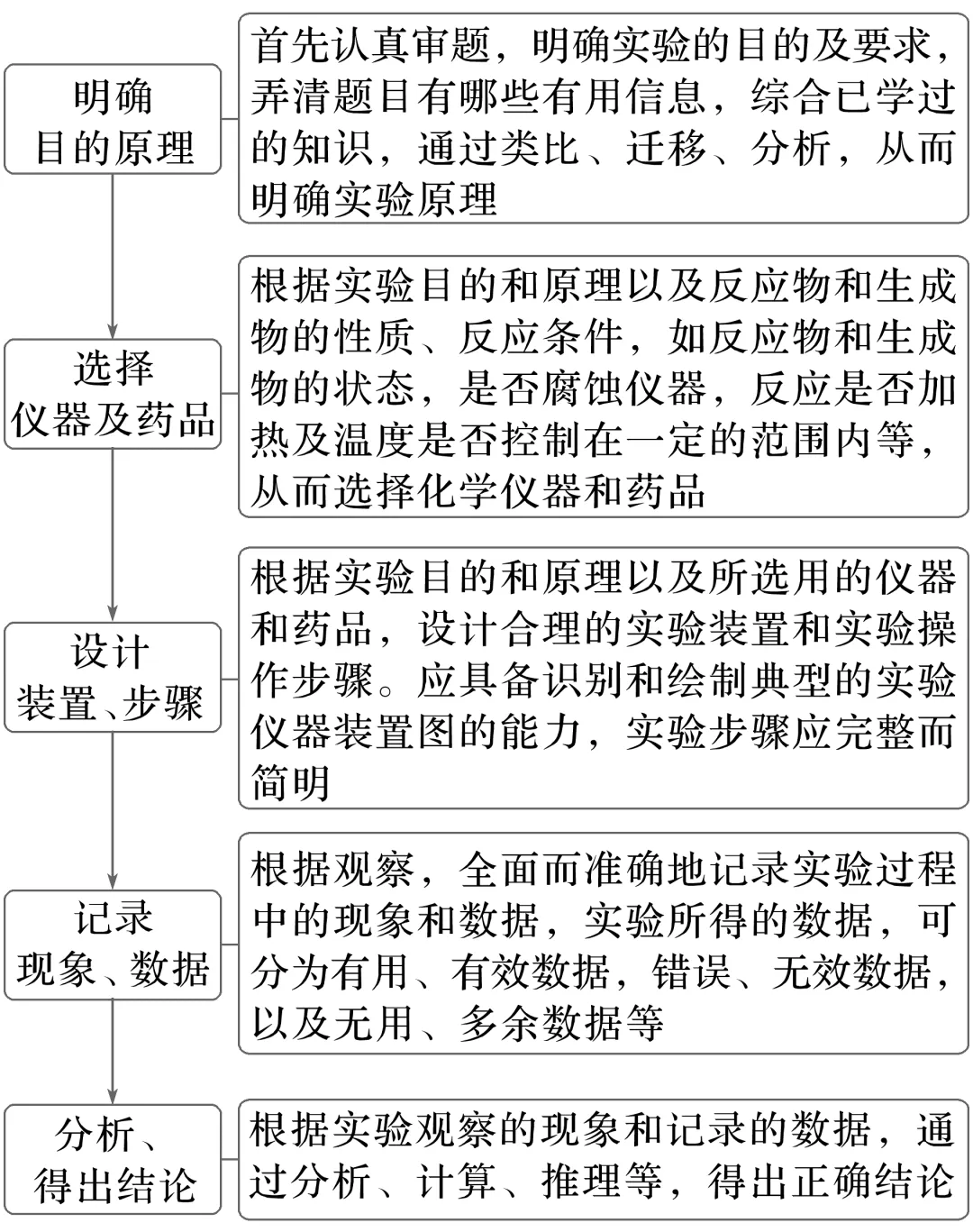
1.物质制备型实验题的思维方法
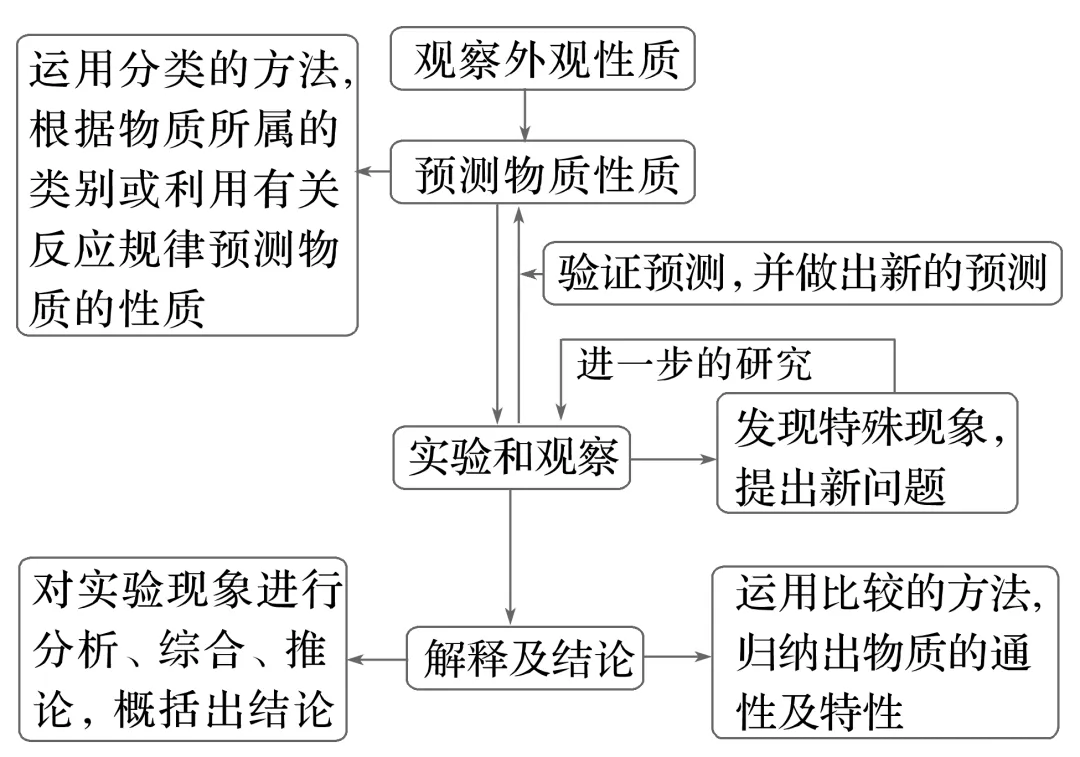
2.研究物质性质的基本方法和程序
注意事项:
(1)若探究影响物质性质的因素,首先应确定变量,其次是“定多变一”,即其他因素不变,只改变一种因素,看这种因素与探究的问题存在怎样的关系。
(2)多角度辩证地看问题
①研究反应物中各微粒的性质(即内因)。
②研究反应条件的影响(如温度、浓度、环境中的其他物质)。
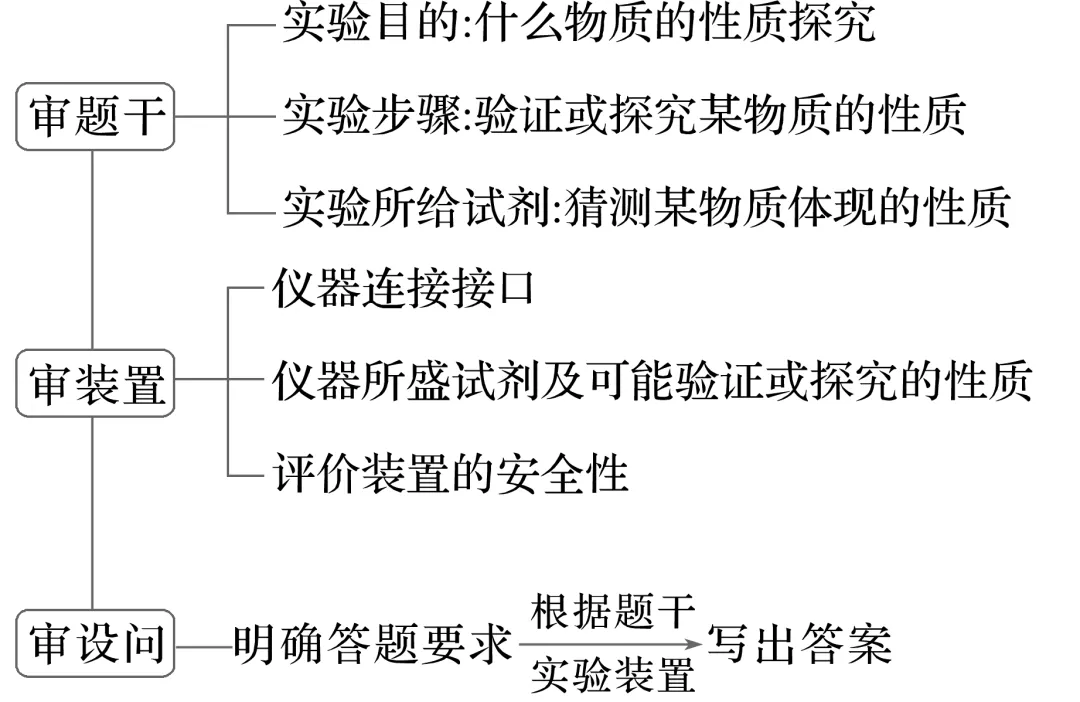
3.物质性质综合实验探究题的审题思路
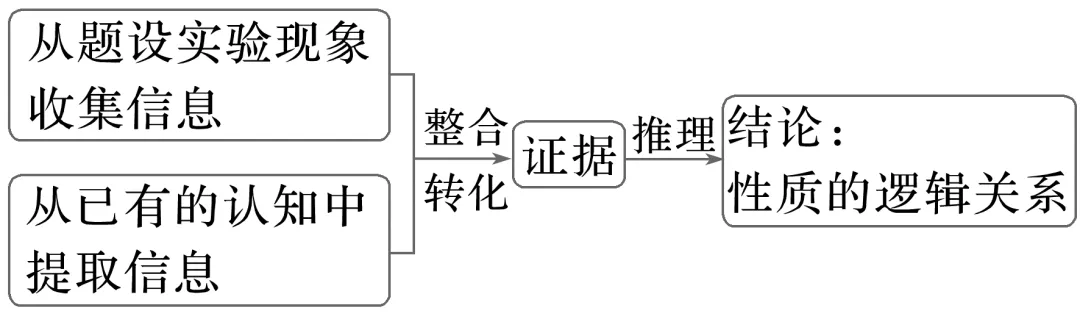
强化证据意识:

1.(2024·广东,17)含硫物质种类繁多,在一定条件下可相互转化。
(1)实验室中,浓硫酸与铜丝反应,所产生的尾气可用(填化学式)溶液吸收。
(2)工业上,烟气中的SO2可在通空气条件下用石灰石的浆液吸收,生成石膏。该过程中,(填元素符号)被氧化。
(3)工业锅炉需定期除水垢,其中的硫酸钙用纯碱溶液处理时,发生反应:CaSO4(s)+C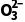 (aq)CaCO3
(aq)CaCO3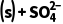 (aq)(Ⅰ)。兴趣小组在实验室探究Na2CO3溶液的浓度对反应(Ⅰ)的反应速率的影响。
(aq)(Ⅰ)。兴趣小组在实验室探究Na2CO3溶液的浓度对反应(Ⅰ)的反应速率的影响。
①用Na2CO3固体配制溶液,以滴定法测定其浓度。
ⅰ.该过程中用到的仪器有。
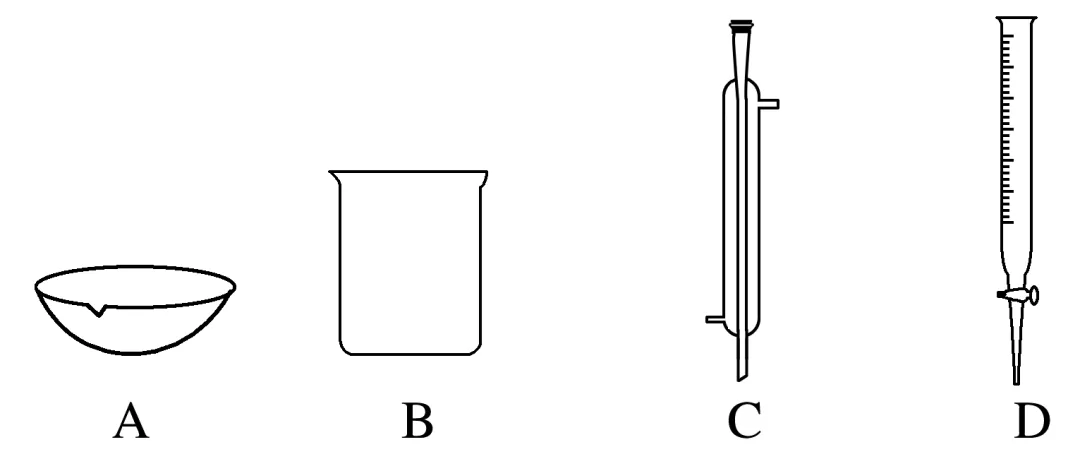
ⅱ.滴定数据及处理:Na2CO3溶液V0 mL,消耗c1 mol·L-1盐酸V1 mL(滴定终点时,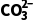 转化为
转化为 ),则c(Na2CO3)= mol·L-1。
),则c(Na2CO3)= mol·L-1。
②实验探究:取①中的Na2CO3溶液,按下表配制总体积相同的系列溶液,分别加入m1 g硫酸钙固体,反应t1 min后,过滤,取V0 mL滤液,用c1 mol·L-1盐酸参照①进行滴定。记录的部分数据如下表(忽略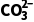 水解的影响)。
水解的影响)。
序号 | V(Na2CO3)/mL | V(H2O)/mL | V(滤液)/mL | V消耗(盐酸)/mL |
a | 100.0 | 0 | V0 | 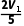
|
b | 80.0 | x | V0 | 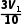
|
则x=,测得的平均反应速率之比va∶vb=。
(4)兴趣小组继续探究反应(Ⅰ)平衡的建立,进行实验。
①初步实验 将1.00 g硫酸钙(M=136 g·mol-1)加入100.0 mL 0.100 mol·L-1 Na2CO3溶液中,在25 ℃和搅拌条件下,利用pH计测得体系的pH随时间的变化曲线如图。
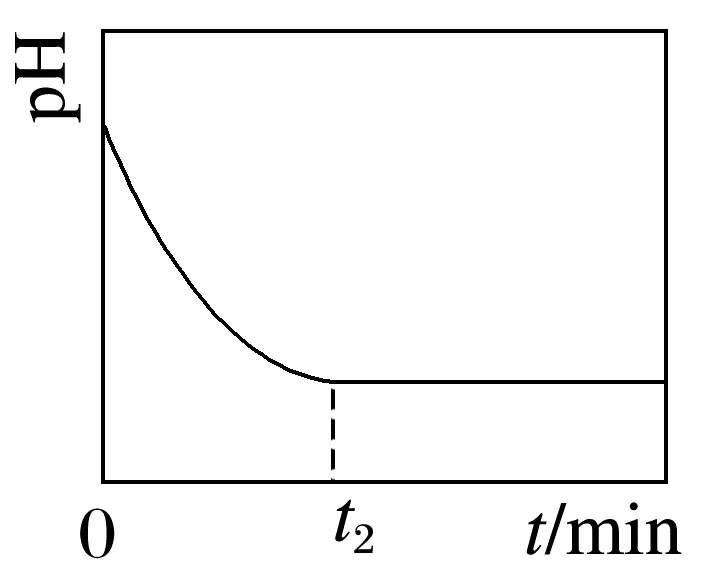
②分析讨论 甲同学根据t2 min后pH不改变,认为反应(Ⅰ)已达到平衡;乙同学认为证据不足,并提出如下假设:
假设1 硫酸钙固体已完全消耗;
假设2 硫酸钙固体有剩余,但被碳酸钙沉淀包裹。
③验证假设,乙同学设计如下方案,进行实验。
步骤 | 现象 |
ⅰ.将①实验中的反应混合物进行固液分离 | - |
ⅱ.取少量分离出的沉淀置于试管中,滴加 | ,沉淀完全溶解 |
ⅲ.继续向ⅱ的试管中滴加 | 无白色沉淀生成 |
④实验小结 假设1成立,假设2不成立。①实验中反应(Ⅰ)平衡未建立。
⑤优化方案、建立平衡 写出优化的实验方案,并给出反应(Ⅰ)平衡已建立的判断依据:。
答案 (1)NaOH(其他合理答案也可) (2)S (3)①ⅰ. BD ⅱ .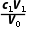 ②20.0 6∶5 (4)③过量稀盐酸 有气体产生 BaCl2溶液 ⑤将不少于1.36 g的硫酸钙加入100.0 mL 0.100 mol·L-1Na2CO3溶液中,在25 ℃和搅拌条件下,利用pH计测体系的pH,当pH不变时,加入Na2SO4固体,若pH变大,说明反应 Ⅰ 平衡已建立
②20.0 6∶5 (4)③过量稀盐酸 有气体产生 BaCl2溶液 ⑤将不少于1.36 g的硫酸钙加入100.0 mL 0.100 mol·L-1Na2CO3溶液中,在25 ℃和搅拌条件下,利用pH计测体系的pH,当pH不变时,加入Na2SO4固体,若pH变大,说明反应 Ⅰ 平衡已建立
解析(1)浓硫酸与铜丝反应的化学方程式为Cu+2H2SO4(浓)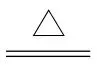 4+SO2↑+2H2O,所产生的尾气为SO2,可用NaOH溶液吸收。(2)SO2生成石膏(主要成分CaSO4),S元素的化合价由+4价升高到+6价,失去电子,被氧化。(3)①用Na2CO3固体配制溶液,以滴定法测定其浓度,该过程用到所给仪器中的烧杯、酸式滴定管,故选B、D;根据离子方程式
4+SO2↑+2H2O,所产生的尾气为SO2,可用NaOH溶液吸收。(2)SO2生成石膏(主要成分CaSO4),S元素的化合价由+4价升高到+6价,失去电子,被氧化。(3)①用Na2CO3固体配制溶液,以滴定法测定其浓度,该过程用到所给仪器中的烧杯、酸式滴定管,故选B、D;根据离子方程式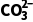 +H+===
+H+=== 可知,c(Na2CO3)=
可知,c(Na2CO3)=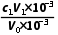 mol·L-1=
mol·L-1=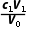

通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享