

(1)实验仪器
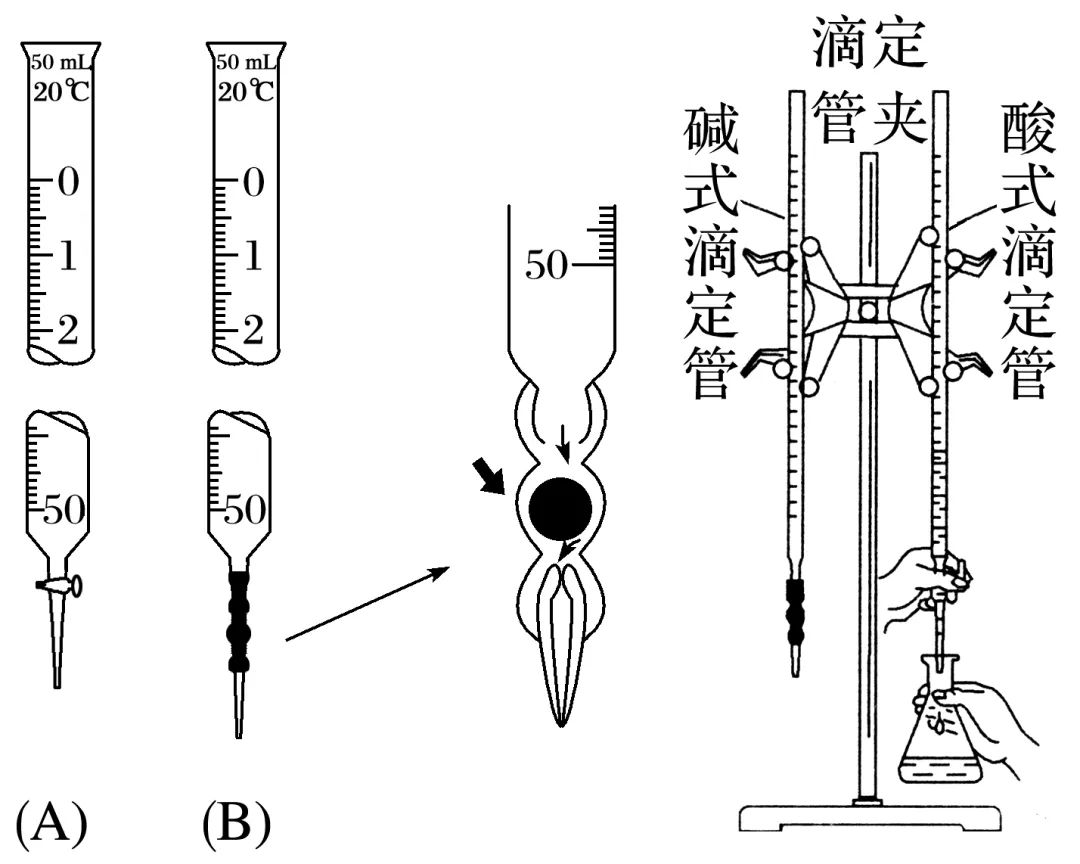
(2)检查是否漏液
酸式 滴定管 | 关闭活塞,向滴定管中加入适量水,用滴定管夹将滴定管固定在铁架台上,观察是否漏水,若2分钟内不漏水,将活塞旋转180°,重复上述操作 |
碱式 滴定管 | 向滴定管中加入适量水,用滴定管夹将滴定管固定在铁架台上,观察是否漏水,若2分钟内不漏水,轻轻挤压玻璃球,放出少量液体,再次观察滴定管是否漏水 |
(3)滴定管排气泡的操作
酸式 滴定管 | 右手将滴定管倾斜30°左右,左手迅速打开活塞使溶液流出,从而使溶液充满尖嘴 |
碱式 滴定管 | 将胶管弯曲使玻璃尖嘴向上倾斜,用两指捏住胶管,轻轻挤压玻璃球,使溶液从尖嘴流出 |
(4)指示剂的选择
类型 | 滴定过程 | 指示剂 | 终点颜色变化 |
酸碱中 和反应 | 强酸滴定强碱(或弱碱) | 甲基橙 | 溶液由黄色变为橙色 |
强碱滴定强酸(或弱酸) | 酚酞 | 溶液由无色变为浅红色 |
氧化还 原反应 | Na2S2O3溶液滴定未知浓度的碘水 | 淀粉溶液 | 溶液由蓝色变为无色 |
酸性KMnO4溶液滴定H2O2(或H2C2O4)溶液 | 不需要指示剂 | 溶液由无色变为浅红色 |
沉淀 反应 | AgNO3溶液滴定含Cl-的溶液 | K2CrO4溶液 | 出现淡红色沉淀(Ag2CrO4为砖红色沉淀) |
判断滴定终点答题模板:当滴入最后半滴标准液,溶液由××色变成××色,且30 s内不变化。
(5)滴定操作
滴定时,左手控制滴定管活塞,右手振荡锥形瓶,眼睛注视锥形瓶内溶液颜色的变化。
(6)误差分析
写出计算式,分析操作对V标的影响,由计算式得出对最终测定结果的影响,切忌死记硬背结论。此外对读数视线问题要学会画图分析。
如:①没有用标准溶液润洗滴定管,导致待测物浓度偏大;
②滴定到终点时,俯视读数,导致待测物浓度偏小;
③滴定前没有赶气泡,导致待测物浓度偏大。

1.(2022·广东,17)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离平衡密切相关。25 ℃时,HAc的Ka=1.75×10-5≈10-4.76。
(1)配制250 mL 0.1 mol·L-1的HAc溶液,需5 mol·L-1HAc溶液的体积为 mL。
(2)下列关于250 mL容量瓶的操作,正确的是。
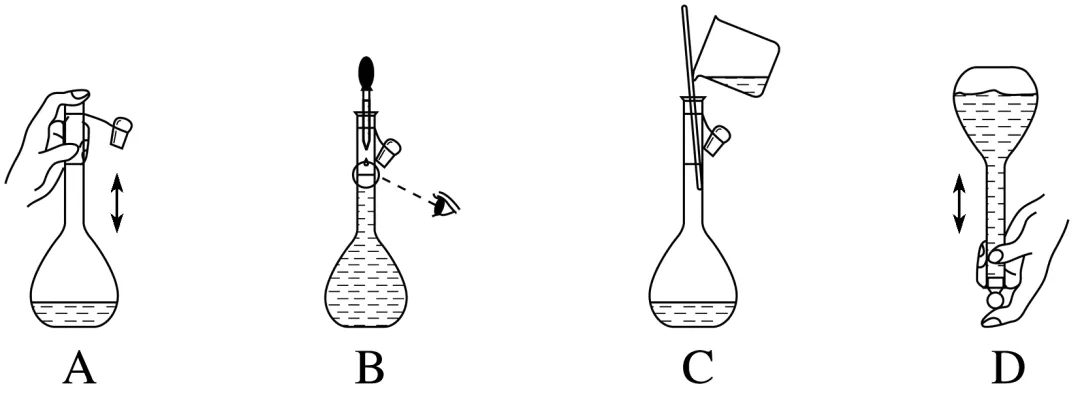
(3)某小组研究25 ℃下HAc电离平衡的影响因素。
提出假设 稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。
设计方案并完成实验 用浓度均为0.1 mol·L-1的HAc和NaAc溶液,按下表配制总体积相同的系列溶液,测定pH,记录数据。
序号 | V(HAc) /mL | V(NaAc) /mL | V(H2O) /mL | n(NaAc) ∶n(HAc) | pH |
Ⅰ | 40.00 | / | / | 0 | 2.86 |
Ⅱ | 4.00 | / | 36.00 | 0 | 3.36 |
… | … | … | … | … | … |
Ⅶ | 4.00 | a | b | 3∶4 | 4.53 |
Ⅷ | 4.00 | 4.00 | 32.00 | 1∶1 | 4.65 |
①根据表中信息,补充数据:a= ,b=。
②由实验 Ⅰ 和 Ⅱ 可知,稀释HAc溶液,电离平衡(填“正”或“逆”)向移动;结合表中数据,给出判断理由:。
③由实验 Ⅱ~Ⅷ 可知,增大Ac-浓度,HAc电离平衡逆向移动。
实验结论 假设成立。
(4)小组分析上表数据发现:随着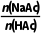 的增加,c(H+)的值逐渐接近HAc的Ka。
的增加,c(H+)的值逐渐接近HAc的Ka。
查阅资料获悉:一定条件下,按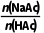 =1配制的溶液中,c(H+)的值等于HAc的Ka。
=1配制的溶液中,c(H+)的值等于HAc的Ka。
对比数据发现,实验Ⅷ中pH=4.65与资料数据Ka=10-4.76存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取20.00 mL HAc溶液,加入2滴酚酞溶液,用0.100 0 mol·L-1NaOH溶液滴定至终点,消耗体积为22.08 mL,则该HAc溶液的浓度为 mol·L-1。画出上述过程的滴定曲线示意图并标注滴定终点。
②用上述HAc溶液和0.100 0 mol·L-1NaOH溶液,配制等物质的量的HAc与NaAc混合溶液,测定pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为0.1 mol·L-1的HAc和NaOH溶液,如何准确测定HAc的Ka?小组同学设计方案并进行实验。请完成下表中 Ⅱ 的内容。
Ⅰ | 移取20.00 mL HAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V1 mL |
Ⅱ | _________________,测得溶液的pH为4.76 |
实验总结 得到的结果与资料数据相符,方案可行。
(6)根据Ka可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途:。
答案 (1)5.0 (2)C (3)①3.00 33.00
②正 实验 Ⅱ 相较于实验 Ⅰ,醋酸溶液稀释了10倍,而实验 Ⅱ 的pH增大值小于1
(4)①0.110 4
(5)向滴定后的混合液中加入20 mL HAc溶液 (6)HClO:漂白剂和消毒液(或H2SO3:还原剂、防腐剂或H3PO4:食品添加剂、制药、生产肥料)
解析(1)溶液稀释过程中,溶质的物质的量不变,因此250×10-3L×0.1mol·L-1=V×5mol·L-1,解得V=5×10-3L=5.0mL。(2)振荡时应用瓶塞塞住容量瓶口,不可用手指压住容量瓶口,故A错误;定容时,视线、溶液凹液面和刻度线应“三线相切”,不能仰视或俯视,且胶头滴管不能插入容量瓶中,故B错误;向容量瓶中转移液体,需用玻璃棒引流,玻璃棒下端位于刻度线以下,同时玻璃棒不能接触容量瓶瓶口,
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享