

1.基元反应与非基元反应
例如H++OH-===H2O是反应物一步直接转化为生成物的,其总反应就是基元反应,又称为简单反应;而2HI===H2+I2的实际机理是分两步进行的,每一步都是一个基元反应:2HIH2+2I·、2I·I2,带有单电子的原子或原子团称为自由基,反应活性高, 寿命短,2HI===H2 + I2称为非基元反应。
2.过渡态
A+BC[A…B…C]AB+C
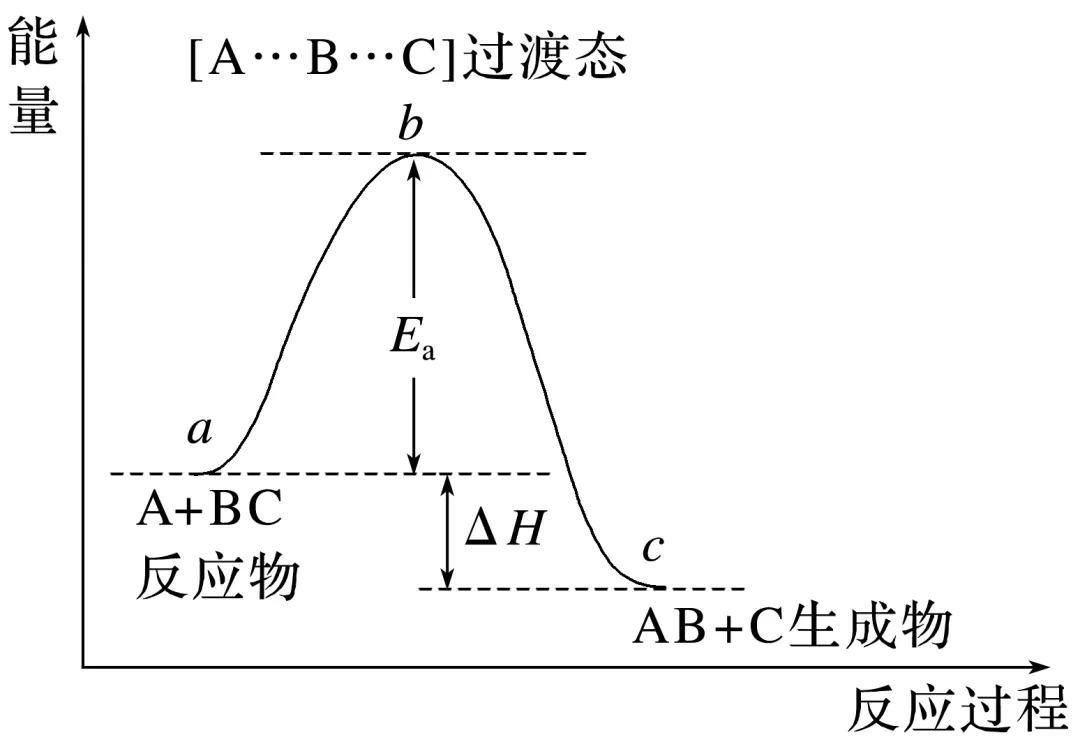
备注(1)以上为一种基元反应,其中正反应活化能Ea正=b-a,逆反应活化能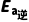 =b-c, ΔH=
=b-c, ΔH=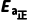 -
-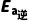 。(2)过渡态[A…B…C]不稳定。
。(2)过渡态[A…B…C]不稳定。
3.中间体
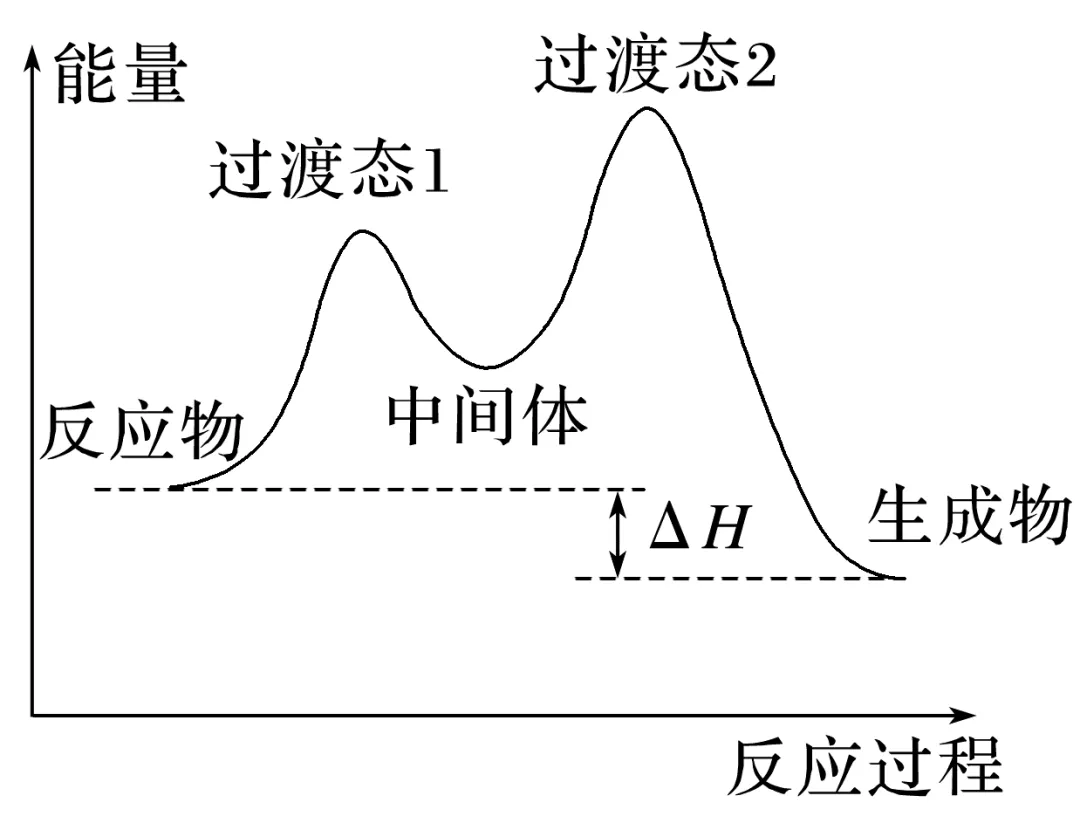
备注处于能量最高点的是反应的过渡态,在多步反应中两个过渡态之间的是中间体,中间体很活泼,寿命很短,但是会比过渡态更稳定些。
4.催化机理能垒图
(1)在催化机理能垒图中,有几个活化状态,就有几个基元反应。可以用图中每步基元反应前后的活性物质,写出其热化学方程式。注意:如果纵坐标相对能量的单位是电子伏特(eV),焓变应转化成每摩尔。
(2)每步基元反应的快慢取决于其能垒的大小,能垒越大,反应速率越慢。
(3)决速步为反应速率最慢的基元反应,即能垒最大的基元反应。
例如:在Rh催化下,甲酸分解制H2反应的过程如图所示。
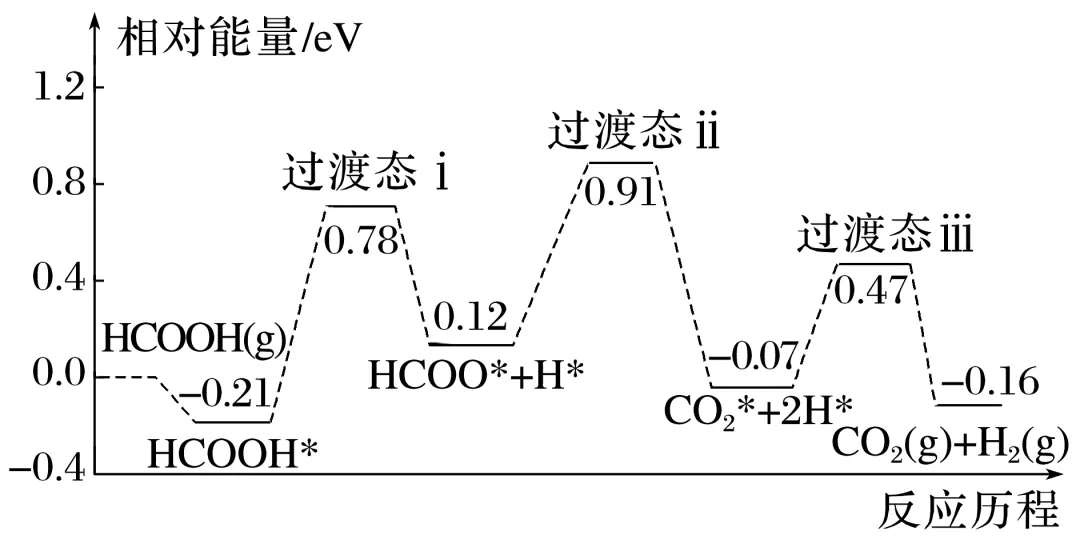
其中带“*”的物种表示吸附在Rh表面,该反应过程中决定反应速率步骤的化学方程式为HCOOH*===HCOO*+H*;甲酸分解制H2的热化学方程式可表示为HCOOH(g)===CO2(g)+H2(g) ΔH=-0.16NA eV·mol-1(阿伏加德罗常数的值用NA表示)。

1.(2024·广东,15)对反应S(g)T(g)(I为中间产物),相同条件下:①加入催化剂,反应达到平衡所需时间大幅缩短;②提高反应温度,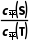 增大,
增大,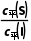 减小。基于以上事实,可能的反应历程示意图(—为无催化剂, ┈为有催化剂)为( )
减小。基于以上事实,可能的反应历程示意图(—为无催化剂, ┈为有催化剂)为( )
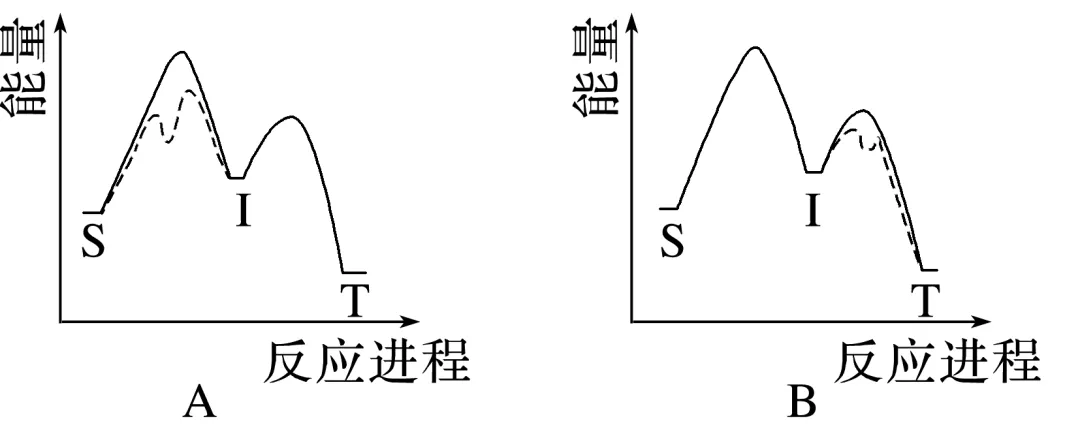
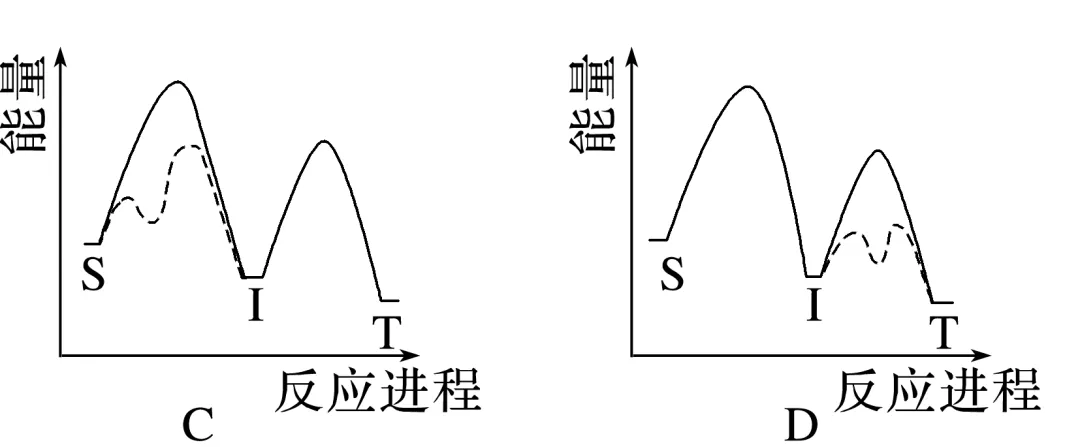
答案 A
解析提高反应温度,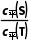 增大,说明反应S(g)
增大,说明反应S(g)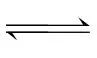 (g)的平衡逆向移动,即该反应为放热反应,
(g)的平衡逆向移动,即该反应为放热反应,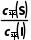 减小,说明S生成中间产物I的反应平衡正向移动,属于吸热反应,由此可排除C、D选项,加入催化剂,反应达到平衡所需时间大幅缩短,即反应的决速步骤的活化能下降,使得反应速率大幅加快,活化能大的步骤为决速步骤,符合条件的反应历程示意图为A。
减小,说明S生成中间产物I的反应平衡正向移动,属于吸热反应,由此可排除C、D选项,加入催化剂,反应达到平衡所需时间大幅缩短,即反应的决速步骤的活化能下降,使得反应速率大幅加快,活化能大的步骤为决速步骤,符合条件的反应历程示意图为A。
2.(2023·广东,15)催化剂Ⅰ和Ⅱ均能催化反应R(g)P(g)。反应历程(下图)中,M为中间产物。其他条件相同时,下列说法不正确的是( )
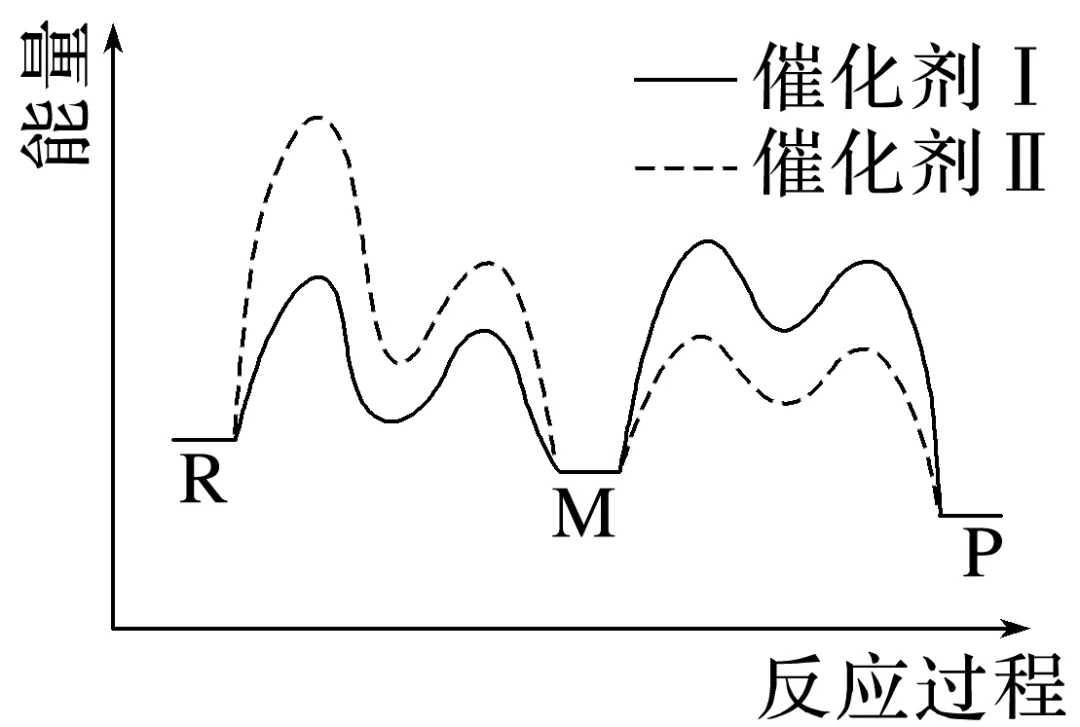
A.使用 Ⅰ 和 Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用 Ⅱ 时,反应体系更快达到平衡
D.使用 Ⅰ 时,反应过程中M所能达到的最高浓度更大
答案 C
解析由图可知两种催化剂均出现四个波峰,所以使用 Ⅰ 和 Ⅱ,反应历程都分4步进行,A正确;该反应是放热反应,升高温度平衡向左移动,R的浓度增大,B正确;由图可知使用 Ⅰ 的最高活化能小于使用 Ⅱ 的最高活化能,所以使用 Ⅰ 时反应速率更快,反应体系更快达到平衡,C错误;在前两个历程中使用 Ⅰ 活化能较低反应速率较快,后两个历程中使用 Ⅰ 活化能较高反应速率较慢,所以使用 Ⅰ 时,反应过程中M所能达到的最高浓度更大,D正确。
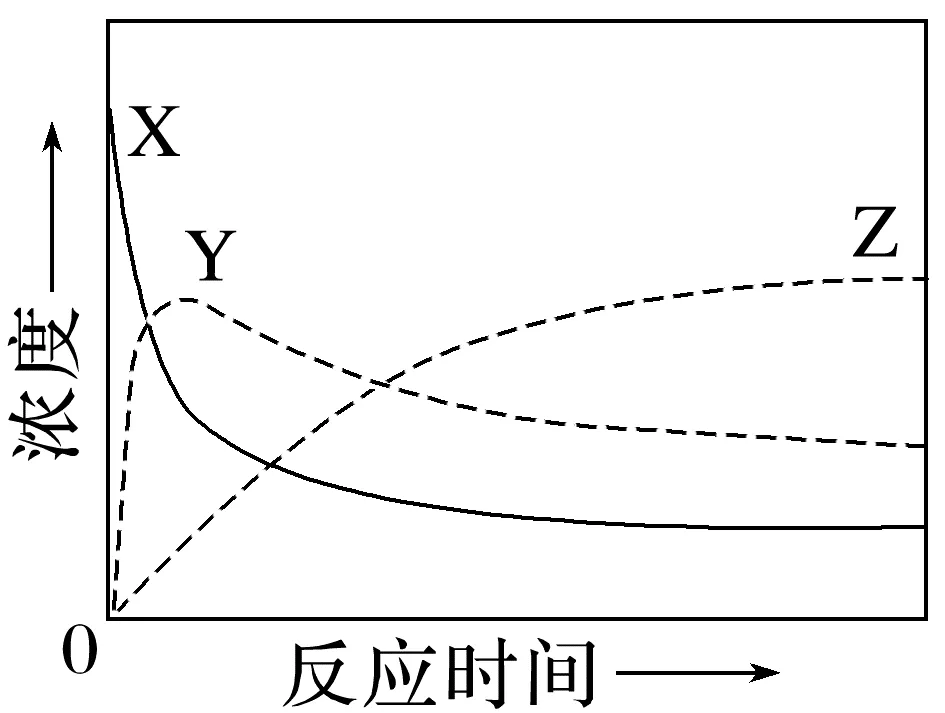
3.(2024·安徽,10)某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g)Y(g)(ΔH1<0),Y(g)Z(g)(ΔH2<0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的是( )
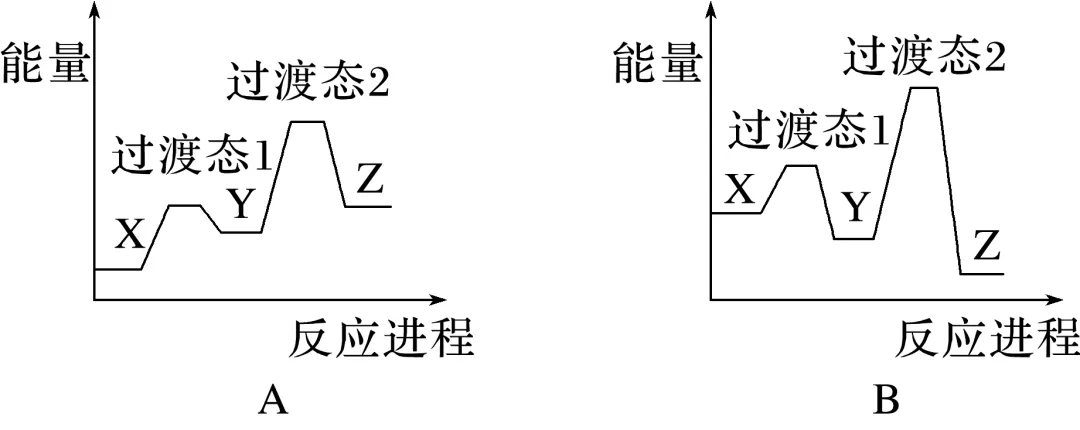
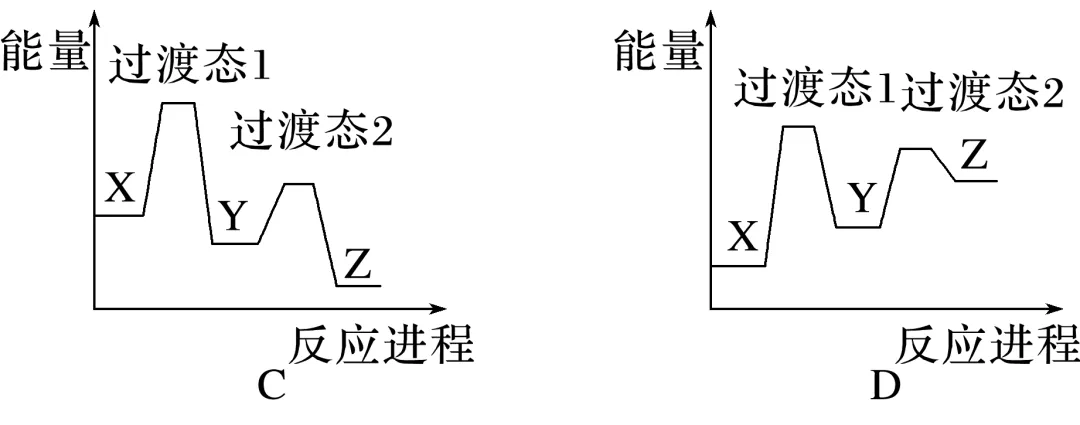
答案 B
解析由X(g)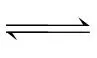 (g)和Y(g)
(g)和Y(g)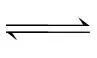 (g)的ΔH都小于0可知,两反应均为放热反应,即反应物的总能量大于生成物的总能量,故A、D不符合题意;由各气体浓度与反应时间的关系图可知,X(g)
(g)的ΔH都小于0可知,两反应均为放热反应,即反应物的总能量大于生成物的总能量,故A、D不符合题意;由各气体浓度与反应时间的关系图可知,X(g)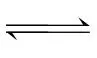 (g)的反应速率大于Y(g)
(g)的反应速率大于Y(g)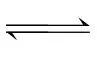 (g)的反应速率,反应X(g)
(g)的反应速率,反应X(g)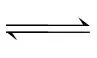 (g)的活化能小于反应Y(g)
(g)的活化能小于反应Y(g)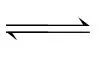 (g)的活化能,故C不符合题意。
(g)的活化能,故C不符合题意。
4.(2023·浙江1月选考,14)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知O2(g)和Cl2(g)的相对能量为0],下列说法不正确的是( )
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享