
[分值:50分]
1.(12分)MnSO4·H2O在工业、农业等方面有广泛的应用,工业上可由高铁菱锰矿(主要成分为MnCO3,还含有FeCO3、Al2O3、MgO、SiO2、CaO等杂质)制备,部分工艺流程如图所示:
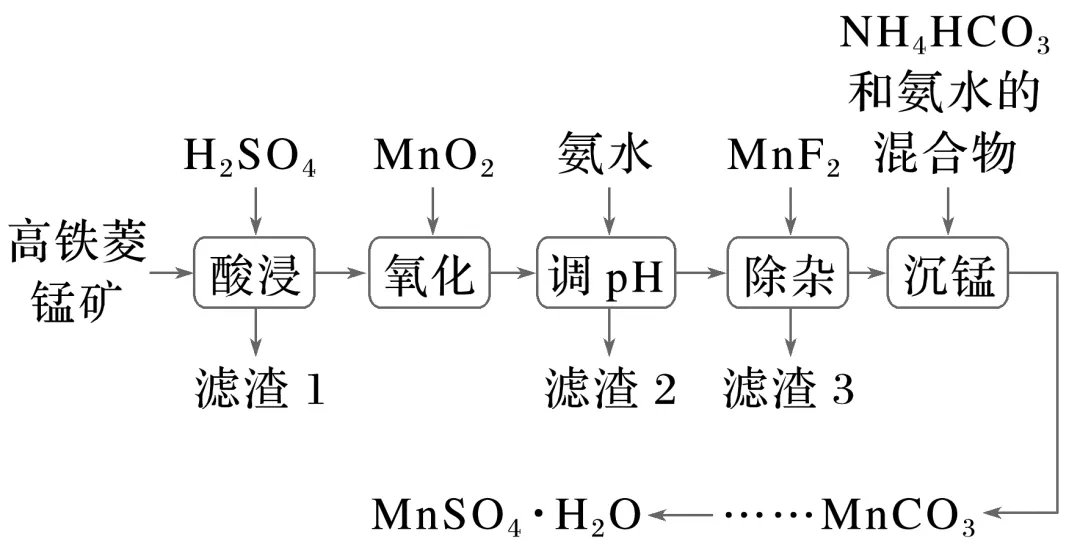
已知:
①相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按离子浓度为0.1 mol·L-1计算)
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
完全沉淀的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
②常温下,CaF2、MgF2的溶度积分别为1.48×10-10、7.40×10-11。
(1)酸浸时需将高铁菱锰矿粉碎,目的是;滤渣1的主要成分是。
(2)“氧化”时发生反应的离子方程式为。
“调pH”的范围是。
(3)“除杂”过程中加入MnF2的目的是。
(4)“沉锰”过程中发生反应的离子方程式为。
(5)生成的MnCO3沉淀需经充分洗涤,检验沉淀是否洗涤干净的方法是。
答案 (1)增大接触面,加快酸浸速率(或增大浸出率) SiO2、CaSO4 (2)2Fe2++4H++MnO2===2Fe3++Mn2++2H2O 5.2≤pH<8.8 (3)将Ca2+、Mg2+转变为CaF2、MgF2沉淀除去 (4)Mn2++HC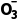 +NH3·H2O===MnCO3↓+H2O+N
+NH3·H2O===MnCO3↓+H2O+N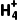 (5)取少量最后一次的洗涤液于试管中,先向其中滴加盐酸,再加BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净
(5)取少量最后一次的洗涤液于试管中,先向其中滴加盐酸,再加BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净
2.(4分)工业上用高硫铝土矿(主要成分为Fe2O3、Al2O3、SiO2,少量FeS2)为原料制备聚合硫酸铁的部分工艺流程如下:
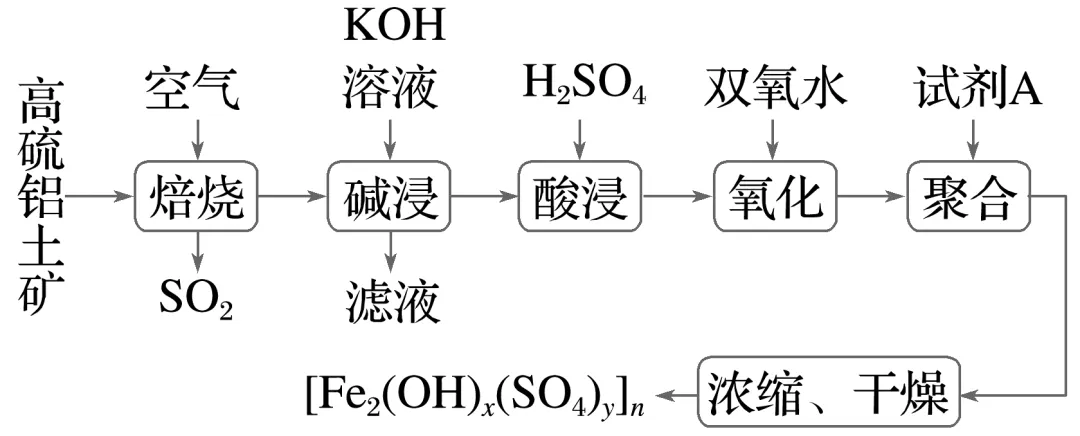
氧化过程中加入双氧水的目的为,
实际生产过程中温度不宜过高且要控制H2O2的投加速度,其原因为。
答案 将Fe2+氧化为Fe3+ 温度过高时H2O2易分解,投加速度过快时,H2O2在Fe3+作用下发生分解
3.(5分)实验室以二氧化铈CeO2废渣为原料制备Cl-含量少的Ce2(CO3)3,其部分实验过程如下:
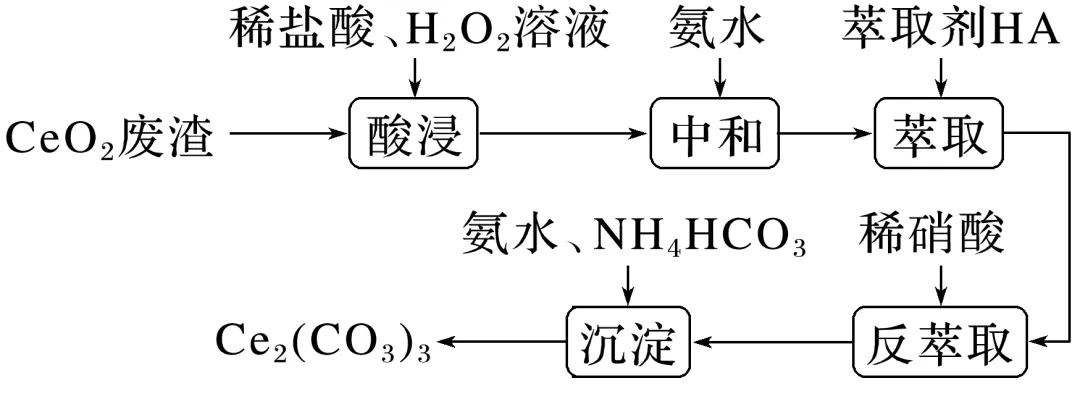
通过中和、萃取、反萃取、沉淀等过程,可制备Cl-含量少的Ce2(CO3)3。已知Ce3+能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
Ce3+(水层)+3HA(有机层)Ce(A)3(有机层)+3H+(水层)
(1)加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是。
(2)反萃取的目的是将有机层Ce3+转移到水层。使Ce3+尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有(填两项)。
(3)与“反萃取”得到的水溶液比较,过滤Ce2(CO3)3溶液的滤液中,物质的量减小的离子有(填化学式)。
答案 (1)降低溶液中氢离子的浓度,促进Ce3+萃取平衡正向移动,提高Ce3+萃取率 (2)适当提高稀硝酸的浓度,多次萃取 (3)Ce3+、H+
4.(9分)(2025·南通、泰州、镇江、盐城部分学校调研)一种以软锰矿(主要含MnO2和少量Fe2O3、MgO、CaCO3、SiO2等)和黄铁矿(主要成分为FeS2)为原料制备Mn3O4的流程如下:
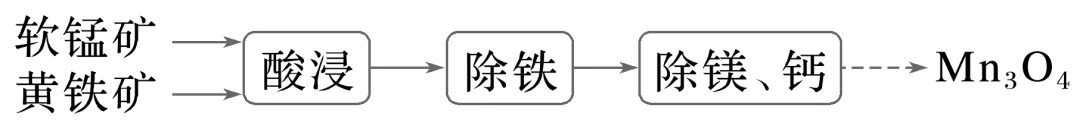
(1)酸浸。将软锰矿、黄铁矿与H2SO4溶液混合搅拌,反应过程中铁元素的变化为FeS2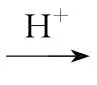 2+
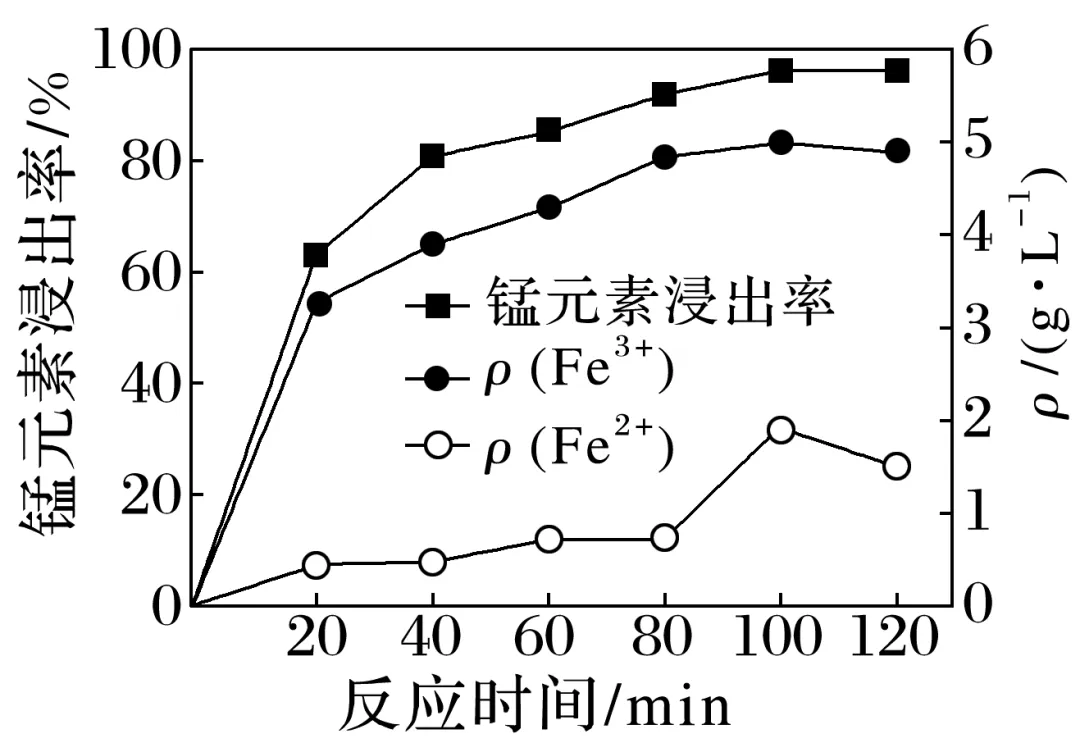
2+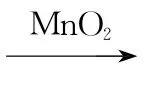 3+。90 ℃下酸浸,锰元素浸出率及Fe3+、Fe2+的ρ(质量浓度)随时间的变化如图所示。
3+。90 ℃下酸浸,锰元素浸出率及Fe3+、Fe2+的ρ(质量浓度)随时间的变化如图所示。
①0~20 min内,FeS2中的硫元素被氧化为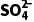 。此时,FeS2和MnO2发生主要反应的离子方程式为
。此时,FeS2和MnO2发生主要反应的离子方程式为
。
②0~20 min内,ρ(Fe2+)逐渐增大的原因是。
③100 min后,ρ(Fe2+)逐渐减小的原因是。
(2)除铁。向“酸浸”所得浸出液中加入过量H2O2,调节溶液pH,充分反应后过滤。H2O2的实际用量比理论计算用量大得多,其原因是。
(3)制Mn3O4。向“除镁、钙”后的溶液中滴加适量氨水,充分反应后过滤、洗涤。将所得沉淀加水制成悬浊液,向其中通入空气可制得Mn3O4。若通入空气时间过长,所得Mn3O4样品中锰元素的质量分数会降低,其原因是。
答案 (1)①2FeS2+15MnO2+28H+===2Fe3++4S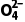 +15Mn2++14H2O ②FeS2与酸反应生成Fe2+的速率大于Fe2+被MnO2氧化的速率
+15Mn2++14H2O ②FeS2与酸反应生成Fe2+的速率大于Fe2+被MnO2氧化的速率
③Fe2+被空气中的氧气氧化为Fe3+ (2)溶液中Fe3+催化H2O2分解 (3)部分锰元素被氧化成高价态锰氧化物
5.(10分)(2025·淮安一模)一种以废铜渣(主要是CuO,含有少量Fe2O3杂质)为原料制备碱式碳酸铜[Cu2(OH)2CO3]的流程如图。
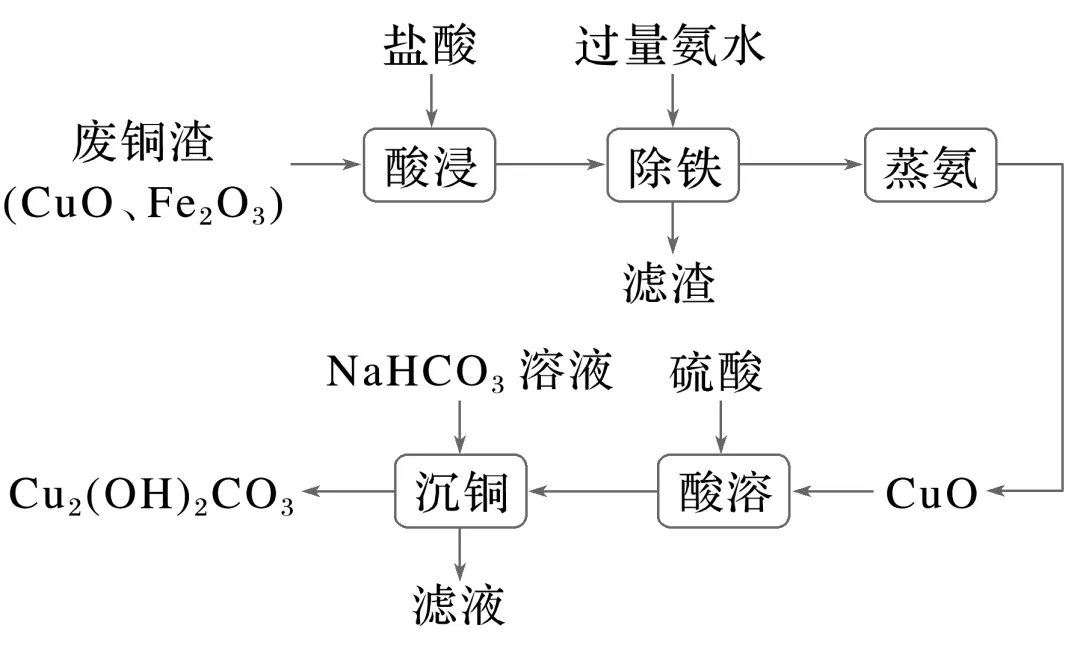
(1)“酸浸”时,采取下列措施一定能提高铜元素浸出率的有(填字母)。
A.升高酸浸温度B.加快搅拌速度
C.缩短酸浸时间D.粉碎废铜渣
(2)“除铁”时滤渣主要成分为(填化学式)。
(3)“蒸氨”过程中生成CuO,该过程发生反应的化学方程式为。
(4)①制备碱式碳酸铜时,不采取向“除铁”后的溶液中直接加入NaHCO3溶液的原因是。
②“沉铜”时发生反应的离子方程式为。
③“沉铜”时也可以利用Na2CO3和NaHCO3的混合溶液,已知25 ℃时,碱式碳酸铜的饱和溶液pH约为8.5,溶液中H2CO3、 、
、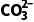 的分布系数δ随pH的变化如图所示。当恰好形成饱和碱式碳酸铜溶液时,溶液中c(
的分布系数δ随pH的变化如图所示。当恰好形成饱和碱式碳酸铜溶液时,溶液中c(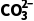 )∶c(
)∶c( )=。
)=。 
通过网盘分享的文件:word讲义【更新联系lymsummers】等2个文件
链接: https://pan.baidu.com/s/1RCL2uLZQuQ-rZUf2_ekrWg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享