

1.化学键的存在
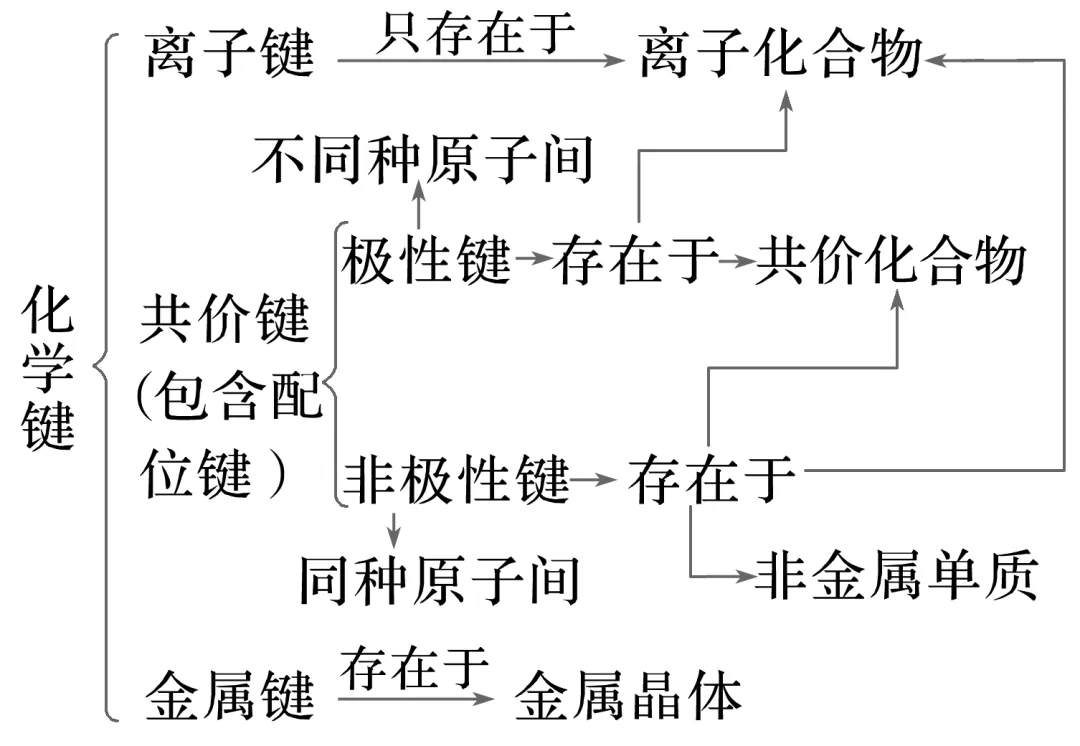
2.共价键
(1)共价键的分类
分类依据 | 类型 |
形成共价键的原子轨道重叠方式 | σ键 | 电子云“头碰头”重叠 |
π键 | 电子云“肩并肩”重叠 |
形成共价键的电子对是否偏移 | 极性键 | 共用电子对发生偏移 |
非极性键 | 共用电子对不发生偏移 |
原子间共用电子对的数目 | 单键 | 原子间有一个共用电子对 |
双键 | 原子间有两个共用电子对 |
三键 | 原子间有三个共用电子对 |
说明相同原子之间形成的共价键可以是非极性键也可以是极性键,如O2中的共价键是非极性键,而O3中的共价键是极性键。
(2)共价键对物质化学性质的影响
①共价键的强弱对物质稳定性的影响
键能越大,键长越短,分子越稳定。
②共价键的极性对羧酸酸性的影响
键的极性对羧酸酸性大小的影响实质是通过改变羧基中羟基的极性而实现的,羧基中羟基的极性越大,越容易电离出H+,则羧酸的酸性越强。
注意与羧基相连的基团会影响羧基中羟基的极性。
ⅰ.烷基是推电子基团,烷基越长推电子效应越大,使羧基中的羟基的极性越小,羧酸的酸性越弱;
ⅱ.与羧基相邻的共价键的极性越大,通过传导作用使羧基中羟基的极性越大,则羧酸的酸性越强。
3.配位键
配位键 | ①配位键是一种特殊的共价键,也具有共价键的特征——方向性和饱和性; ②形成条件:成键原子一方有孤电子对,另一方有空轨道; ③表示方法:常用“A→B”表示配位键 |
配合物 | 通常把金属离子或原子与某些分子或离子以配位键结合形成的化合物称为配合物。 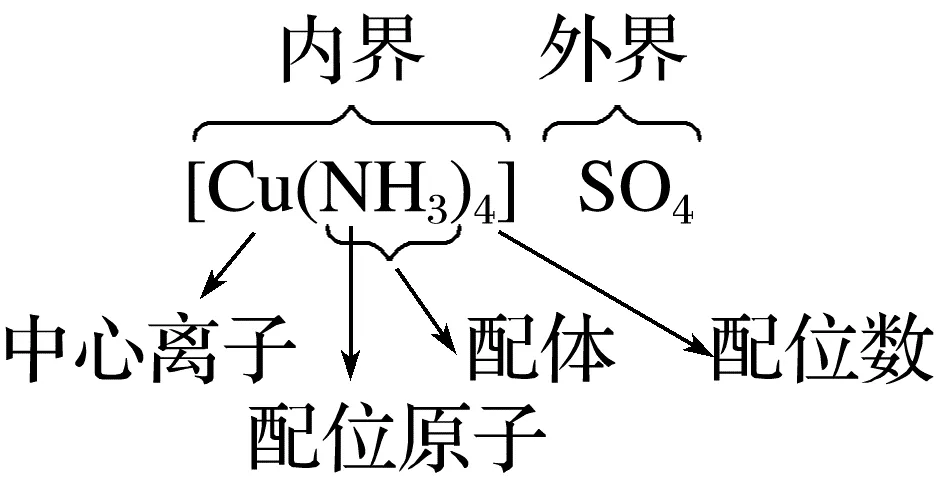
|
多齿配体 | 一个配体中有两个或两个以上的配位原子 |
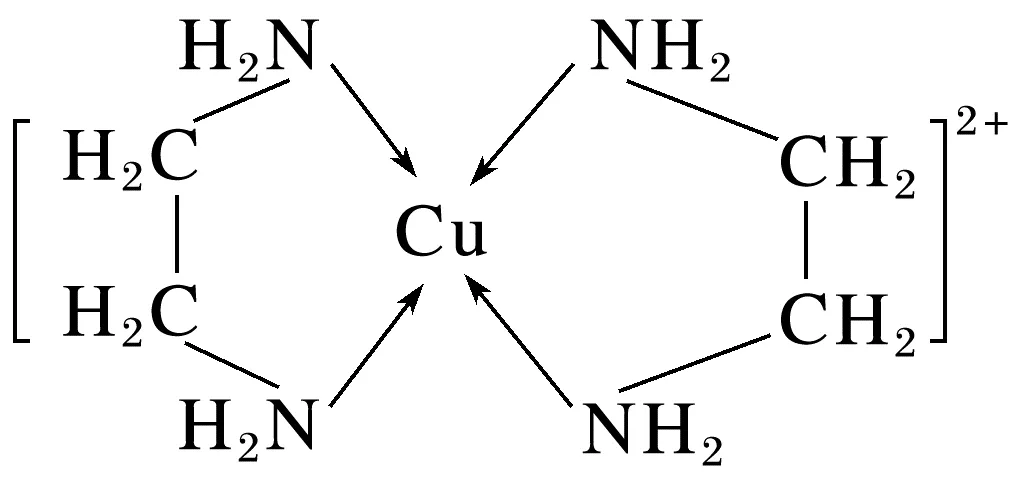
说明①一般来说,配合物内界与外界之间为离子键,电荷相互抵消。②配体可能有多个配位原子,与中心原子或离子形成螯合物。以铜离子与乙二胺形成的配离子为例:

1.(2025·湖北,13)N和P为同主族相邻元素。下列关于物质或现象的解释错误的是( )
A.KNO3的熔点比K3PO4的低,因为KNO3的离子键更强
B.磷单质通常不以P2形式存在,因为磷磷之间难以形成三键
C.次磷酸比硝酸的酸性弱,因为前者的H—O键极性小
D.P形成PF5而N形成NF3,因为P的价层电子轨道更多且半径更大
答案 A
解析离子化合物熔点的差异源于离子键的强度,K3PO4中P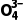 带3个负电荷,而KNO3中N
带3个负电荷,而KNO3中N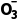 只带1个负电荷,离子或离子团所带电荷越高,离子键越强,熔点越高,因此,K3PO4的离子键比KNO3的强,A错误;氮原子因原子半径小,p轨道重叠程度大,能形成稳定的N≡N,磷原子半径大,p轨道重叠差,难以形成稳定的P≡P,因此倾向于形成P4四面体结构,B正确;含氧酸的酸性与O—H键极性有关,中心原子电负性越高,O—H键极性越大,越易解离H+,氮的电负性高于磷,因此HNO3中O—H键极性更大,酸性更强,C正确;氮价层仅有2s和2p轨道,NF3的中心原子N形成sp3杂化后有3个σ键和1个孤电子对,磷有3d轨道可参与sp3d杂化,且原子半径大,能容纳5个配体,故形成PF5,D正确。
只带1个负电荷,离子或离子团所带电荷越高,离子键越强,熔点越高,因此,K3PO4的离子键比KNO3的强,A错误;氮原子因原子半径小,p轨道重叠程度大,能形成稳定的N≡N,磷原子半径大,p轨道重叠差,难以形成稳定的P≡P,因此倾向于形成P4四面体结构,B正确;含氧酸的酸性与O—H键极性有关,中心原子电负性越高,O—H键极性越大,越易解离H+,氮的电负性高于磷,因此HNO3中O—H键极性更大,酸性更强,C正确;氮价层仅有2s和2p轨道,NF3的中心原子N形成sp3杂化后有3个σ键和1个孤电子对,磷有3d轨道可参与sp3d杂化,且原子半径大,能容纳5个配体,故形成PF5,D正确。
2.[2025·广东,17(4)]该小组继续探究取代基对芳香酸酸性的影响。
①知识回顾 羧酸酸性可用Ka衡量。下列羧酸Ka的变化顺序为
CH3COOH <CH< span>2ClCOOH <CCl< span>3COOH <CF< span>3COOH </CF<> </CCl<> </CH<>
随着卤原子电负性,羧基中的羟基增大,酸性增强。
②提出假设 甲同学根据①中规律推测下列芳香酸的酸性强弱顺序为
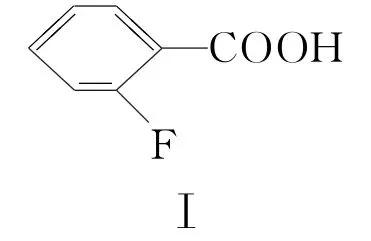
③验证假设 甲同学测得常温下三种酸的饱和溶液的pH大小顺序为Ⅲ>Ⅱ>Ⅰ,据此推断假设成立。但乙同学认为该推断依据不足,不能用所测得的pH直接判断Ka大小顺序,因为。
乙同学测定了上述三种酸的Ka,其顺序为Ⅱ>Ⅰ>Ⅲ。
④实验小结 假设不成立,芳香环上取代基效应较复杂,①中规律不可随意推广。
答案①增强 极性 ③三种酸的饱和溶液浓度不同
解析①卤素原子电负性越强,吸电子效应就越强,则羧基中H—O的极性增大,容易发生断裂,更易电离出氢离子,因此酸性增强。③实验探究时应控制单一变量,不同物质在同一温度下的溶解度不同,故不同物质的饱和溶液的浓度一般不同,则要比较三种酸的酸性强弱,除物质不同外,其他条件均应该保持相同,即三种酸溶液的浓度应相同,所以乙同学的实验方案不合理。
3.[2021·广东,20(4)]很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。
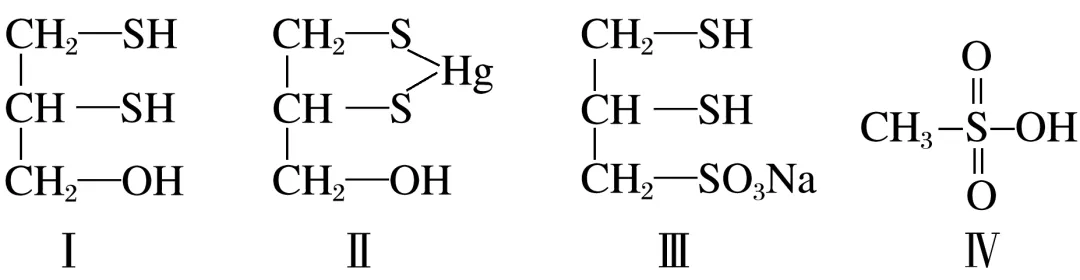
化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有。
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C—C—C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
答案 AD
解析中S原子的价层电子对数为2+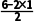 =4,因此S原子采取sp3杂化,故A正确;
=4,因此S原子采取sp3杂化,故A正确;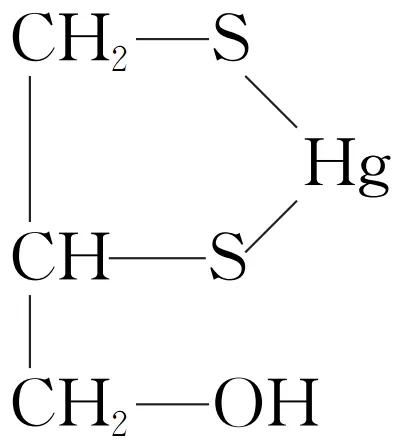 中含有的元素为H、C、O、S、Hg,同周期元素从左至右元素的电负性逐渐增大,同主族元
中含有的元素为H、C、O、S、Hg,同周期元素从左至右元素的电负性逐渐增大,同主族元
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享