
1.晶胞中微粒数目的计算方法——均摊法
晶胞类型 | 计算方法 |
立方(四方)晶胞 | 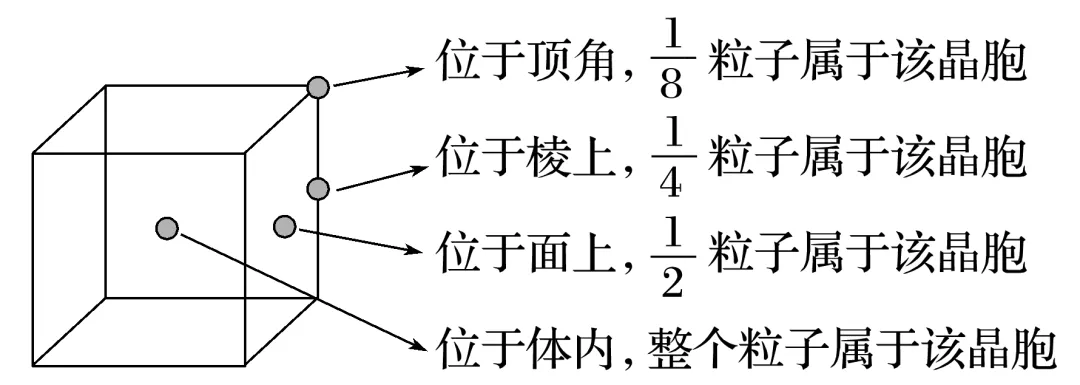
|
六方晶胞(平行六面体形) | 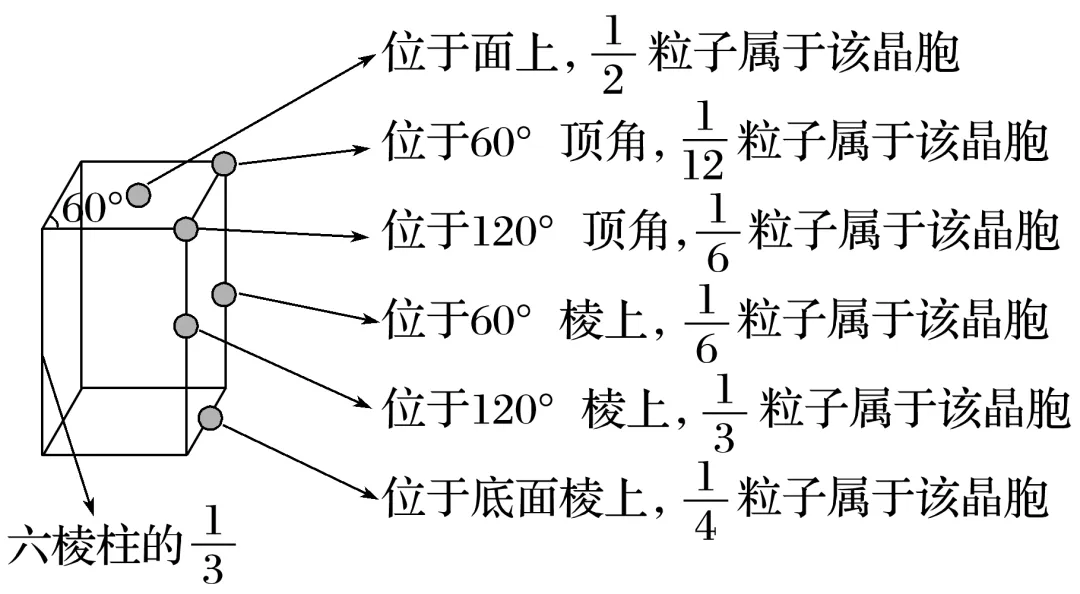
|
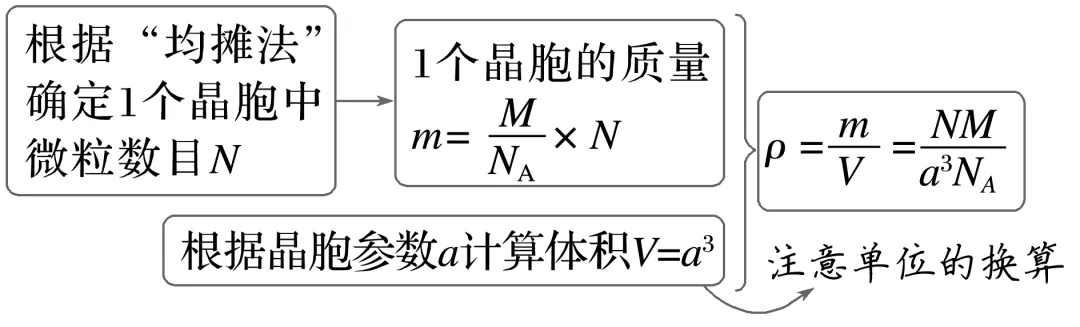
2.晶体密度计算模型

1.(2025·浙江1月选考,13)某化合物Fe(NH3)2Cl2的晶胞如图所示,下列说法不正确的是( )
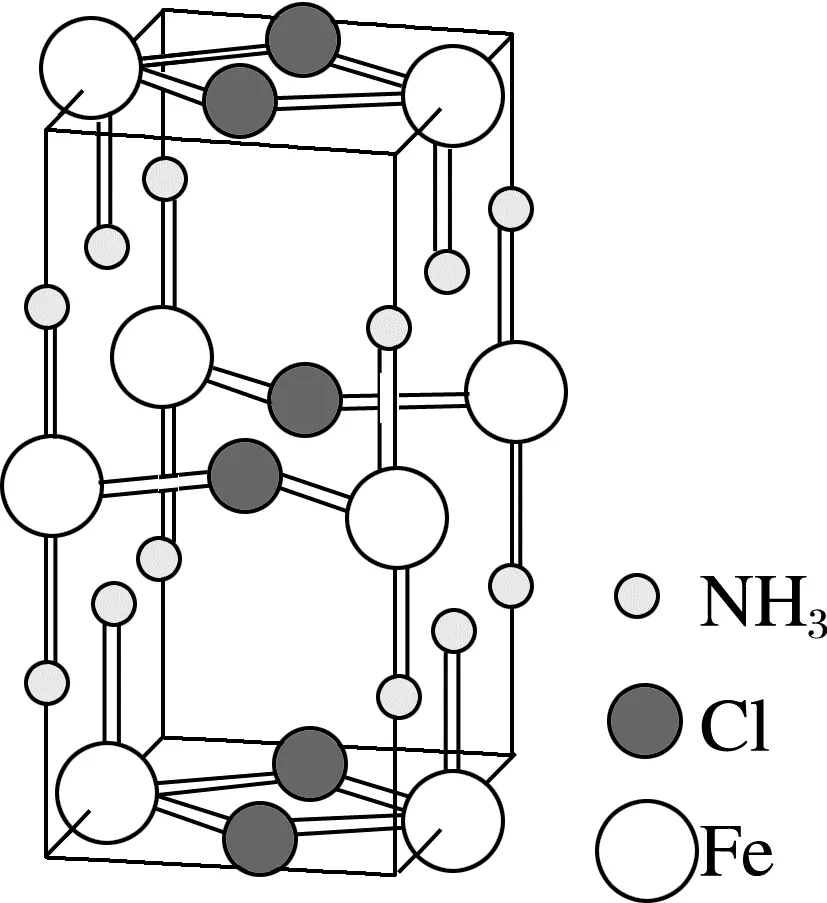
A.晶体类型为混合晶体
B.NH3与二价铁形成配位键
C.该化合物与水反应有难溶物生成
D.该化合物热稳定性比FeCl2高
答案 D
解析由图可知,Fe(NH3)2Cl2晶体中存在离子键、配位键、分子间作用力,具有分子晶体和离子晶体的特性,属于混合晶体,A正确;NH3与二价铁通过配位键形成[Fe(NH3)2]2+,B正确;Fe(NH3)2Cl2与水反应可以生成Fe(OH)2沉淀,化学方程式为Fe(NH3)2Cl2+2H2O===Fe(OH)2↓+2NH4Cl,C正确;Fe(NH3)2Cl2中[Fe(NH3)2]2+离子半径大于Fe2+,[Fe(NH3)2]2+与Cl-之间的键能小于Fe2+与Cl-之间的键能,Fe(NH3)2Cl2热稳定性比FeCl2弱,D错误。
2.(2025·重庆,8)化合物X的晶胞如图所示,下列叙述正确的是( )
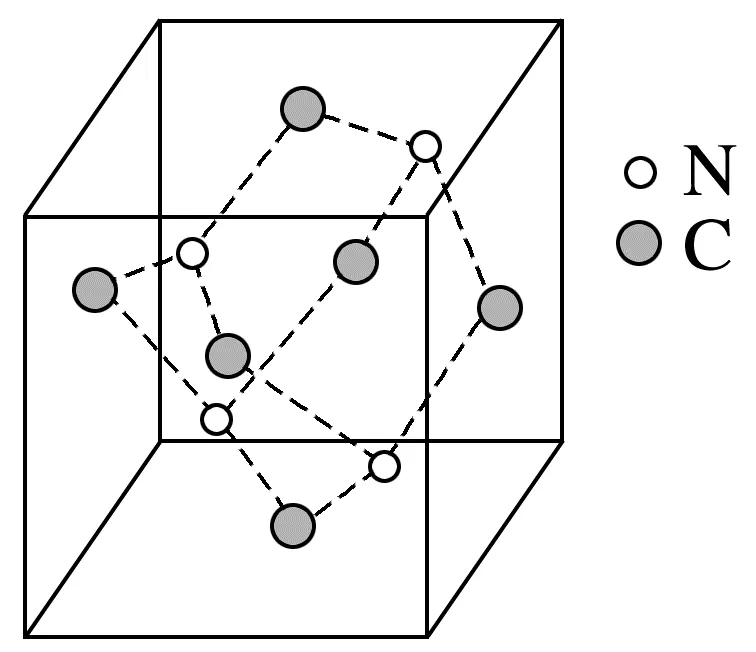
A.X中存在π键
B.X属于混合型晶体
C.X的化学式可表示为C3N4
D.X中C原子上有1对孤电子对
答案 C
解析 C、N均以单键连接,晶胞中不含π键,A错误;晶胞内只存在共价键,不是混合型晶体,B错误;由图可知,晶胞中C原子的个数是6×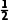 =3,N位于晶胞内部,个数为4,则晶胞化学式为C3N4,C正确;位于面心的C原子与周围4个氮原子(位于两个晶胞内)相连,其配位数为4,不存在孤电子对,D错误。
=3,N位于晶胞内部,个数为4,则晶胞化学式为C3N4,C正确;位于面心的C原子与周围4个氮原子(位于两个晶胞内)相连,其配位数为4,不存在孤电子对,D错误。
3.(2024·湖南,12)Li2CN2是一种高活性的人工固氮产物,其合成反应为2LiH+C+N2 2CN2+H2,晶胞如图所示,下列说法错误的是( )
2CN2+H2,晶胞如图所示,下列说法错误的是( )
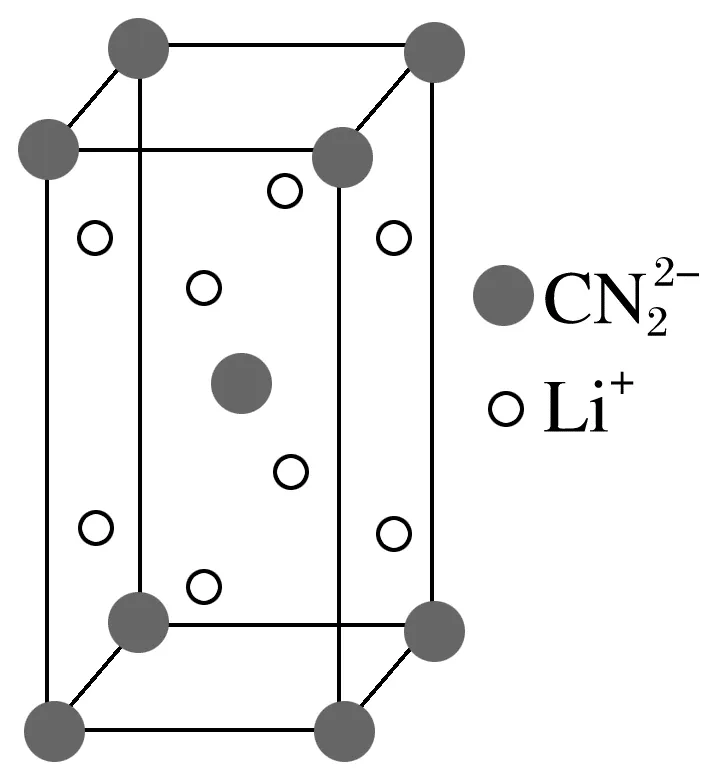
A.合成反应中,还原剂是LiH和C
B.晶胞中含有的Li+个数为4
C.每个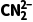 周围与它最近且距离相等的Li+有8个
周围与它最近且距离相等的Li+有8个
D.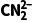 为V形结构
为V形结构
答案 D
解析反应2LiH+C+N2 2CN2+H2中,LiH中H元素由-1价升高到0价,C元素由0价升高到+4价,N元素由0价降低到-3价,还原剂是LiH和C,A正确;Li+位于晶胞中的面上,晶胞中含有的Li+个数为8×
2CN2+H2中,LiH中H元素由-1价升高到0价,C元素由0价升高到+4价,N元素由0价降低到-3价,还原剂是LiH和C,A正确;Li+位于晶胞中的面上,晶胞中含有的Li+个数为8×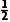 =4,B正确;以位于体心的
=4,B正确;以位于体心的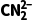 为标准,与它最近且距离相等的Li+有8个,C正确;
为标准,与它最近且距离相等的Li+有8个,C正确;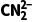 的中心原子C原子的价层电子对数为2+
的中心原子C原子的价层电子对数为2+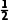 ×(4+2-3×2)=2,C原子为sp杂化,或
×(4+2-3×2)=2,C原子为sp杂化,或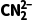 与CO2互为等电子体,可知
与CO2互为等电子体,可知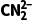 为直线形分子,D错误。
为直线形分子,D错误。
4.(2025·黑吉辽蒙,9)NaxWO3晶体因x变化形成空位而导致颜色各异,当0.44≤x≤0.95时,其立方晶胞结构如图。设NA为阿伏加德罗常数的值,下列说法错误的是( )
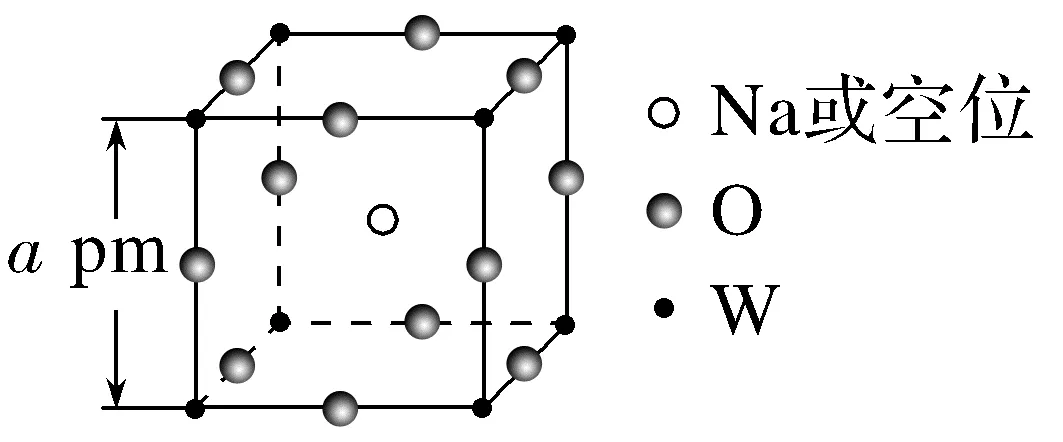
A.与W最近且等距的O有6个
B.x增大时,W的平均价态升高
C.密度为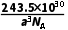 g·cm-3时,x=0.5
g·cm-3时,x=0.5
D.空位数不同,吸收的可见光波长不同
答案 B
解析由图可知,W位于O形成的八面体空隙中,故与W最近且等距的O有6个,A正确;NaxWO3中Na为+1价,O为-2价,由化合物中各元素化合价代数和为零可知,x增大,W的平均价态降低,B错误;由均摊法可知,W位于晶胞顶点,个数为8×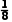 =1,O位于晶胞棱心,个数为12×
=1,O位于晶胞棱心,个数为12×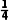 =3,当x=0.5时,晶胞中Na的个数为0.5,则晶体密度为
=3,当x=0.5时,晶胞中Na的个数为0.5,则晶体密度为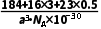 g·cm-3=
g·cm-3=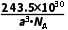 g·cm-3,C正确;由题目信息知,NaxWO3晶体因x变化形成空位而导致颜色各异,空位能够捕获自由电子或空穴而对可见光产生选择性吸收,光的颜色与波长有关,故空位数不同,吸收的可见光波长不同,D正确。
g·cm-3,C正确;由题目信息知,NaxWO3晶体因x变化形成空位而导致颜色各异,空位能够捕获自由电子或空穴而对可见光产生选择性吸收,光的颜色与波长有关,故空位数不同,吸收的可见光波长不同,D正确。
5.(2023·浙江6月选考,17(3))某含氮化合物晶胞如图,其化学式为,每个阴离子团的配位数(紧邻的阳离子数)为。
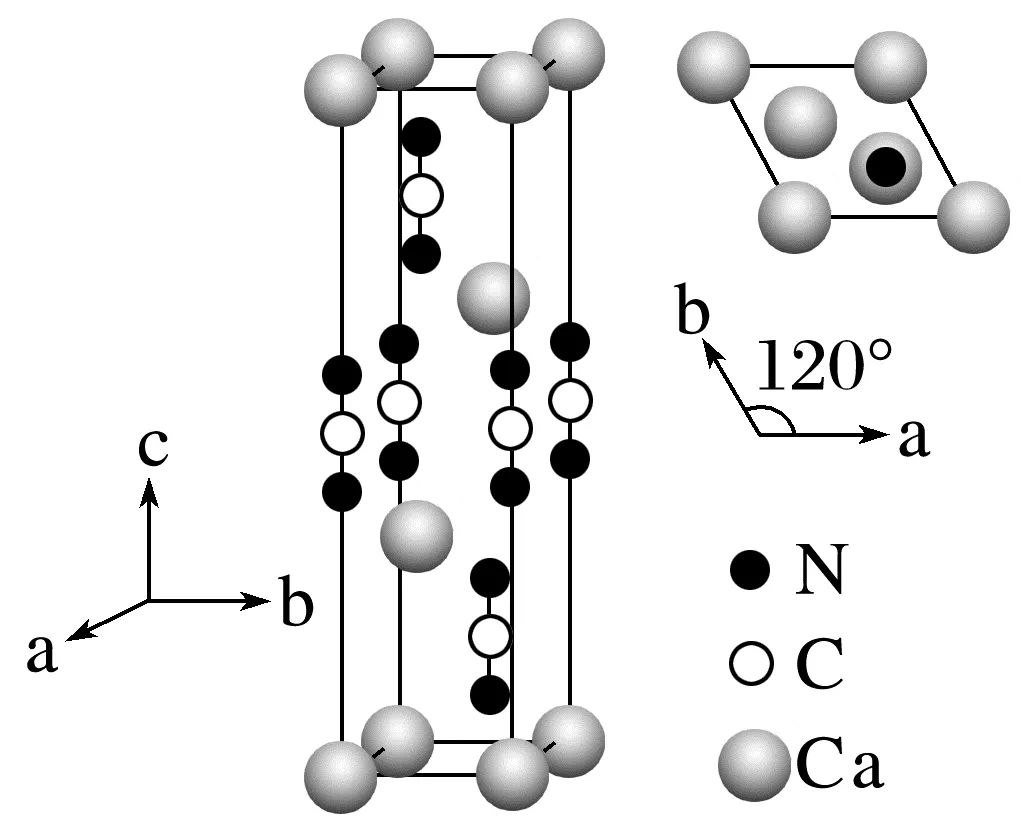
答案 CaCN2 6
解析钙个数为2+4×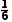 +4×
+4×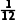 =3,个数为2+2×
=3,个数为2+2×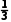 +2×
+2×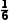 =3,则其化学式为CaCN2。本题中分析得到
=3,则其化学式为CaCN2。本题中分析得到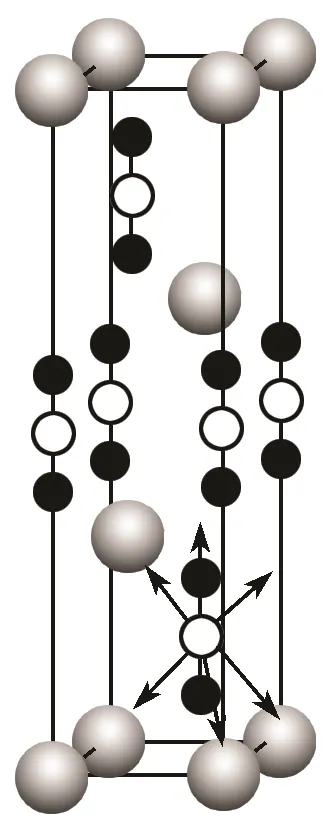 ,以这个进行分析,其俯视图为
,以这个进行分析,其俯视图为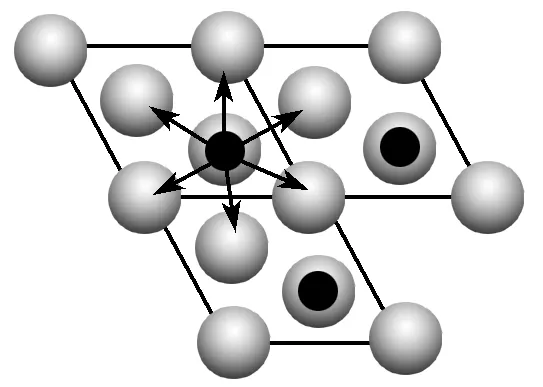 ,因此距离最近的钙离子个数为6,其配位数为6。
,因此距离最近的钙离子个数为6,其配位数为6。
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享