
[分值:50分]
(1~10题,每小题5分)
1.(2025·佛山期中)H3PO2是一种一元弱酸,与等浓度等体积的NaOH溶液完全反应后生成NaH2PO2,下列叙述正确的是( )
A.NaH2PO2是酸式盐
B.H3PO2溶液中存在电离平衡:H2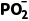
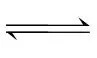
 +H+
+H+
C.0.01 mol·L-1H3PO2水溶液加水稀释,pH增大
D.H3PO2溶液与NaOH溶液反应的离子方程式为H++OH-===H2O
答案 C
解析 H3PO2是一种一元弱酸,则NaH2PO2是正盐,A错误;H3PO2是一种一元弱酸,所以只能发生H3PO2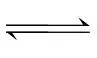 2
2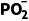 +H+,不存在二级电离,B错误;0.01mol·L-1H3PO2水溶液加水稀释,氢离子浓度减小,pH增大,C正确;H3PO2溶液与NaOH溶液反应的离子方程式为H3PO2+OH-===H2
+H+,不存在二级电离,B错误;0.01mol·L-1H3PO2水溶液加水稀释,氢离子浓度减小,pH增大,C正确;H3PO2溶液与NaOH溶液反应的离子方程式为H3PO2+OH-===H2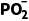 +H2O,D错误。
+H2O,D错误。
2.(2025·广东模拟预测)葡萄酒中含有的酒石酸(H2T)常用作食品添加剂。已知Na2T溶液呈碱性,NaHT溶液呈酸性。下列说法错误的是( )
A.0.05 mol·L-1H2T溶液的pH大于1
B.H2T溶液的pH随温度升高而增大
C.NaHT在水中的电离方程式为NaHT===Na++HT-
D.0.01 mol·L-1 Na2T溶液中:c(OH-)=c(H+)+c(HT-)+2c(H2T)
答案 B
解析 Na2T溶液呈碱性,则T2-发生水解反应,H2T的二级电离不完全,0.05mol·L-1H2T溶液的氢离子的浓度小于0.1mol·L-1,pH大于1,故A正确;电离为吸热反应,H2T的电离随温度升高而增大,氢离子浓度变大,pH减小,故B错误;NaHT属于强电解质,H2T的二级电离不完全,故NaHT在水中的电离方程式为NaHT===Na++HT-,故C正确;根据质子守恒得,c(OH-)=c(H+)+c(HT-)+2c(H2T),D正确。
3.(2024·梅州一模)乙氨酸(H2NCH2COOH)是一种两性有机物,可与盐酸反应生成盐酸盐(HOOCCH2NH3Cl)。已知HOOCCH2NH3Cl水溶液呈酸性,下列叙述正确的是( )
A.0.001 mol·L-1 HOOCCH2NH3Cl水溶液的pH=3
B.0.001 mol·L-1HOOCCH2NH3Cl水溶液加水稀释,pH升高
C.HOOCCH2NH3Cl在水中的电离方程式为HOOCCH2NH3Cl===HOOCCH2NH2+HCl
D.HOOCCH2NH3Cl水溶液中:c(OH-)+c(Cl-)=c(HOOCCH2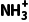 )+c(HOOCCH2NH2)
)+c(HOOCCH2NH2)
答案 B
解析 HOOCCH2NH3Cl为强酸弱碱盐,电离出的HOOCCH2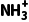 会发生水解,弱碱离子的水解较为微弱,因此0.001mol·L-1HOOCCH2NH3Cl水溶液的pH>3,故A错误;稀释溶液时,HOOCCH2
会发生水解,弱碱离子的水解较为微弱,因此0.001mol·L-1HOOCCH2NH3Cl水溶液的pH>3,故A错误;稀释溶液时,HOOCCH2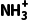 水解程度增大,根据勒夏特列原理可知,溶液中氢离子浓度减小,溶液pH升高,故B正确;HOOCCH2NH3Cl为强酸弱碱盐,在水中的电离方程式为HOOCCH2NH3Cl===HOOCCH2
水解程度增大,根据勒夏特列原理可知,溶液中氢离子浓度减小,溶液pH升高,故B正确;HOOCCH2NH3Cl为强酸弱碱盐,在水中的电离方程式为HOOCCH2NH3Cl===HOOCCH2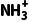 +Cl-,故C错误;根据电荷守恒可知,溶液中c(OH-)+c(Cl-)=c(HOOCCH2
+Cl-,故C错误;根据电荷守恒可知,溶液中c(OH-)+c(Cl-)=c(HOOCCH2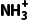 )+c(H+),根据元素守恒,有c(Cl-)=c(HOOCCH2
)+c(H+),根据元素守恒,有c(Cl-)=c(HOOCCH2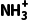 )+c(HOOCCH2NH2),都与选项中等式不对应,故D错误。
)+c(HOOCCH2NH2),都与选项中等式不对应,故D错误。
4.(2025·湛江一模)25 ℃时,H2SeO4第一步完全电离,第二步电离平衡常数Ka=2.18×10-2。则25 ℃时,下列说法正确的是( )
A.KHSeO4的溶液显碱性
B.K2SeO4溶液中存在c(K+)=2[c(HSe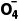 )+c(Se
)+c(Se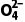 )]
)]
C.0.5 mol·L-1的H2SeO4溶液中,c(HSe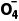 )+2c(Se
)+2c(Se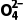 )+c(OH-)=0.5 mol·L-1
)+c(OH-)=0.5 mol·L-1
D.向H2SeO4溶液中滴加KOH溶液至中性时,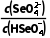 =2.18×104
=2.18×104
答案 B
解析 H2SeO4第一步完全电离,则KHSeO4只电离不水解,溶液显酸性,A错误;根据元素守恒可知,K2SeO4溶液中存在c(K+)=2[c(HSe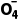 )+c(Se
)+c(Se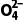 )],B正确;根据元素守恒可知,0.5mol·L-1的H2SeO4溶液中,c(HSe
)],B正确;根据元素守恒可知,0.5mol·L-1的H2SeO4溶液中,c(HSe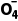 )+c(Se
)+c(Se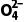 )=0.5mol·L-1,C错误;向H2SeO4溶液中滴加KOH溶液至中性时,c(H+)=10-7mol·L-1,=
)=0.5mol·L-1,C错误;向H2SeO4溶液中滴加KOH溶液至中性时,c(H+)=10-7mol·L-1,=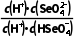 =
=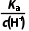 =2.18×105,D错误。
=2.18×105,D错误。
5.(2024·广东二模)安息香酸(HR)是最简单的一元芳香酸,其钠盐(用NaR表示)的水溶液呈碱性。已知常温下,Ka(HR)>Ka1(H2CO3)。下列说法正确的是( )
A.常温下,0.001 mol·L-1 HR水溶液的pH=3
B.向NaR水溶液中加水稀释,溶液的pH升高
C.NaR水溶液中,c(HR)+c(H+)=c(R-)+c(OH-)
D.常温下,NaR溶液的碱性比同浓度的NaHCO3溶液弱
答案 D
解析 HR是弱酸,不完全电离,常温下,0.001mol·L-1HR水溶液的pH>3,A错误;NaR水溶液中由于R-水解显碱性,加水稀释水解程度变大,但是碱性变弱,溶液的pH减小,B错误;NaR水溶液中的质子守恒为c(HR)+c(H+)=c(OH-),C错误;已知Ka(HR)>Ka1(H2CO3),HR酸性比碳酸强,根据越弱越水解,同浓度的NaHCO3溶液水解程度大,碱性强,D正确。
6.(2025·广州大联考)赖氨酸[H3N+(CH2)4CH(NH2)COO-,用HR表示]是人体必需氨基酸。常温下,赖氨酸与足量盐酸反应可得盐酸盐(H3RCl2,其水溶液呈酸性),在水溶液中存在电离平衡:H3R2+ 2R+
2R+ -。下列叙述正确的是( )
-。下列叙述正确的是( )
A.0.01 mol·L-1的H3RCl2水溶液稀释10倍后,pH=3
B.H3RCl2的水溶液中c水(H+)<10-7 mol·L-1
C.H3RCl2水溶液中c(Cl-)+c(OH-)+c(R-)=2c(H3R2+)+c(H+)
D.NaR水溶液中R-的水解平衡常数Kh与K3的关系为Kh·K3=1014
答案 B
解析 0.01mol·L-1的H3RCl2的水溶液稀释10倍后浓度为0.001mol·L-1,根据题意,H3RCl2不能完全电离,pH>3,A错误;H3RCl2是盐酸盐,通过H3R2+的电离使溶液呈酸性,抑制了水的电离,水的电离程度减小,c水(H+)<10-7mol·L-1,B正确;H3RCl2水溶液中还存在H2R+,电荷守恒关系为c(Cl-)+c(OH-)+c(R-)=2c(H3R2+)+c(H+)+c(H2R+),C错误;NaR水溶液中R-的水解平衡常数Kh与K3的关系为Kh=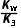 ,即Kh与K3的关系为Kh·K3=Kw=10-14,D错误。
,即Kh与K3的关系为Kh·K3=Kw=10-14,D错误。
7.(2024·广东高三阶段练习)某二元弱酸H2A在常温下的电离平衡常数Ka1=1.0×10-2,Ka2=2.6×10-7。下列说法不正确的是( )
A.向H2A溶液中加入少量NaOH固体,则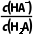 变小
变小
B.0.1 mol·L-1H2A溶液中:c(H+)>2c(A2-)+c(HA-)>c(OH-)
C.对H2A溶液升温,溶液的pH变小
D.0.1 mol·L-1NaHA溶液呈酸性
答案 A
解析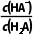 =
=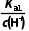 ,加入少量NaOH固体,氢离子浓度减小,Ka1不变,所以
,加入少量NaOH固体,氢离子浓度减小,Ka1不变,所以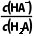 变大,A项错误;溶液中存在电荷守恒:c(H+)=c(HA-)+2c(A2-)+c(OH-),所以c(H+)>2c(A2-)+c(HA-),由于氢氧根离子只由水电离产生,所以浓度最低,B项正确;升温促进H2A的电离,溶液的pH变小,C项正确;0.1mol·L-1NaHA溶液中,HA-既发生水解,又发生电离,其电离平衡常数为Ka2=2.6×10-7,水解平衡常数为Kh=
变大,A项错误;溶液中存在电荷守恒:c(H+)=c(HA-)+2c(A2-)+c(OH-),所以c(H+)>2c(A2-)+c(HA-),由于氢氧根离子只由水电离产生,所以浓度最低,B项正确;升温促进H2A的电离,溶液的pH变小,C项正确;0.1mol·L-1NaHA溶液中,HA-既发生水解,又发生电离,其电离平衡常数为Ka2=2.6×10-7,水解平衡常数为Kh=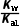 =
=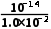 =1.0×10-12,电离平衡常数大于水解平衡常数,说明电离程度大于水解程度,溶液呈酸性,D项正确。
=1.0×10-12,电离平衡常数大于水解平衡常数,说明电离程度大于水解程度,溶液呈酸性,D项正确。
8.(2025·梅州二模)柠檬、柑橘等植物中含有丰富的柠檬酸(H3A),其是一种三羧酸类化合物。已知常温下,Ka1(H3A)=7.4×10-4,下列说法正确的是( )
A.H3A在水中的电离方程式为H3A===3H++A3-
B.Na3A溶液中:c(Na+)<3c(A3-)+2c(HA2-)+c(H2A-)
C.Na3A溶液加水稀释过程中,水的电离程度减小,Kw减小
D.向H3A溶液中滴入小苏打溶液,产生大量气泡,则Ka1(H2CO3)<7.4×10-4
答案 D
解析羧酸为弱酸,故H3A在水中的电离方程式为H3AH++H2A-、H2A-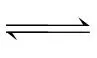 ++HA2-、HA2-
++HA2-、HA2-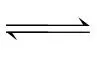 ++A3-,A错误;根据电荷守恒,c(Na+)+c(H+)=3c(A3-)+2c(HA2-)+c(H2A-)+c(OH-),由于Na3A水解呈碱性,c(OH-)>c(H+),则c(Na+)>3c(A3-)+2c(HA2-)+c(H2A-),B错误;Kw只受温度影响,稀释过程中Kw不变,C错误;H3A溶液中滴入小苏打溶液,产生CO2,根据强酸制取弱酸原理,H3A酸性大于H2CO3,则Ka1(H2CO3)<7.4×10-4,D正确。
++A3-,A错误;根据电荷守恒,c(Na+)+c(H+)=3c(A3-)+2c(HA2-)+c(H2A-)+c(OH-),由于Na3A水解呈碱性,c(OH-)>c(H+),则c(Na+)>3c(A3-)+2c(HA2-)+c(H2A-),B错误;Kw只受温度影响,稀释过程中Kw不变,C错误;H3A溶液中滴入小苏打溶液,产生CO2,根据强酸制取弱酸原理,H3A酸性大于H2CO3,则Ka1(H2CO3)<7.4×10-4,D正确。
9.(2025·中山二模)25 ℃时,苯胺(C6H5NH2)的电离平衡常数Kb=4×10-10。下列说法正确的是( )
A.苯胺的电离方程式为C6H5NH2+H2O===C6H5N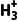 +OH-
+OH-
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享