

1.(2022·浙江1月选考,19)在恒温恒容条件下,发生反应A(s)+2B(g)3X(g),c(B)随时间的变化如图中曲线甲所示。下列说法不正确的是( )
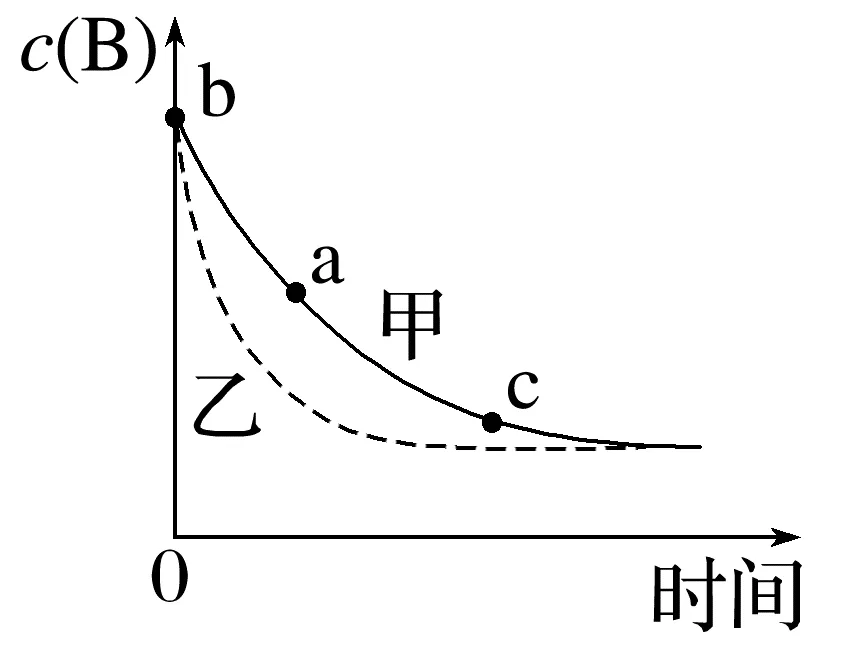
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线乙所示
答案 C
解析 b点处切线的斜率是此时刻物质浓度除以此时刻时间,为B的瞬时速率,B正确;由化学反应速率之比等于化学方程式计量数之比分析,在不同时刻都存在关系:3v(B)=2v(X),C不正确;维持温度、容积不变,向反应体系中加入催化剂,平衡不移动,反应速率增大,达到的新的平衡状态与原来的平衡状态相同,D正确。
2.(2025·安徽,11)恒温恒压密闭容器中,t=0时加入A(g),各组分物质的量分数x随反应时间t变化的曲线如图(反应速率v=kx,k为反应速率常数)。
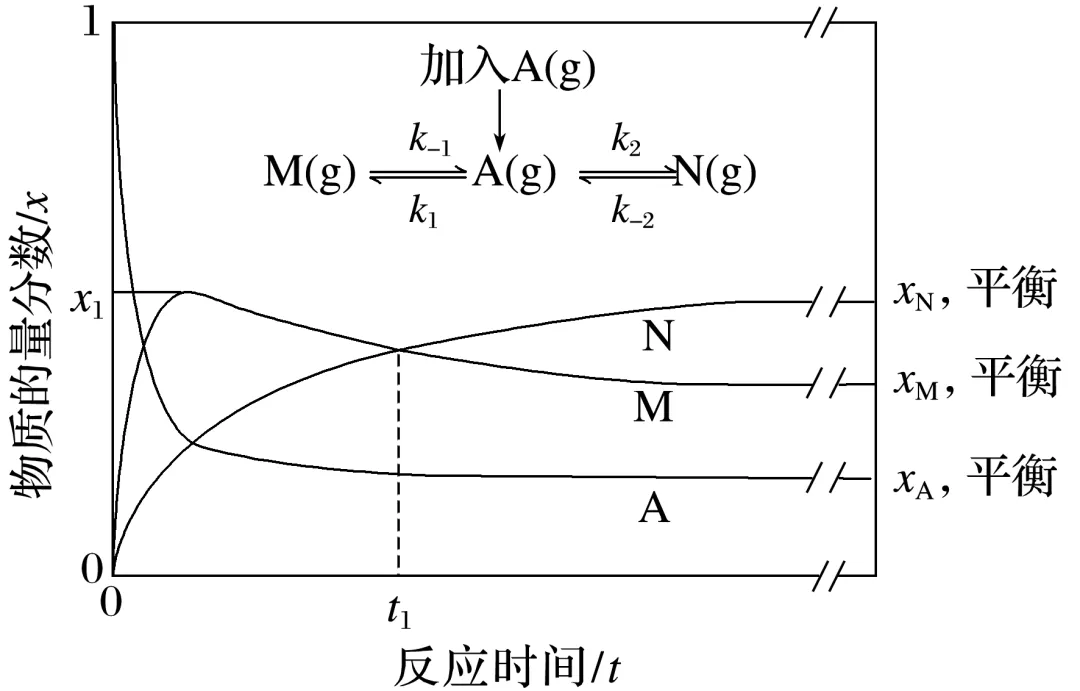
下列说法错误的是( )
A.该条件下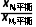 =
=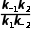
B.0~t1时间段,生成M和N的平均反应速率相等
C.若加入催化剂,k1增大,k2不变,则x1和xM,平衡均变大
D.若A(g)→M(g)和A(g)→N(g)均为放热反应,升高温度则xA,平衡变大
答案 C
解析反应达到平衡时,正、逆反应速率相等,则对于反应M(g)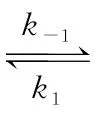 (g)存在关系式:k-1·xM,平衡=k1·xA,平衡,对于反应A(g)
(g)存在关系式:k-1·xM,平衡=k1·xA,平衡,对于反应A(g)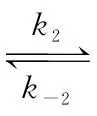 (g)存在关系式:k-2·xN,平衡=k2·xA,平衡,两式联立可得
(g)存在关系式:k-2·xN,平衡=k2·xA,平衡,两式联立可得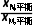 =
=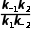 正确;起始时,xM和xN均为0,t1时,xM=xN,则0~t1时间段,生成M和N的平均反应速率相等,B正确;催化剂不影响平衡移动,故xM,平衡不变,C错误;A(g)→M(g)和A(g)→N(g)均为放热反应,则升高温度,平衡均逆向移动,故xA,平衡变大,D正确。
正确;起始时,xM和xN均为0,t1时,xM=xN,则0~t1时间段,生成M和N的平均反应速率相等,B正确;催化剂不影响平衡移动,故xM,平衡不变,C错误;A(g)→M(g)和A(g)→N(g)均为放热反应,则升高温度,平衡均逆向移动,故xA,平衡变大,D正确。
3.(2025·诸暨高三模拟)纳米碗C40H10是一种奇特的碗状共轭体系。高温条件下,C40H10可以由C40H20分子经过连续5步氢抽提和闭环脱氢反应生成。C40H20(g)C40H18(g)+H2(g)的反应机理和能量变化如图所示,其中最后一个基元反应的逆反应活化能为22.8 kJ·mol-1:
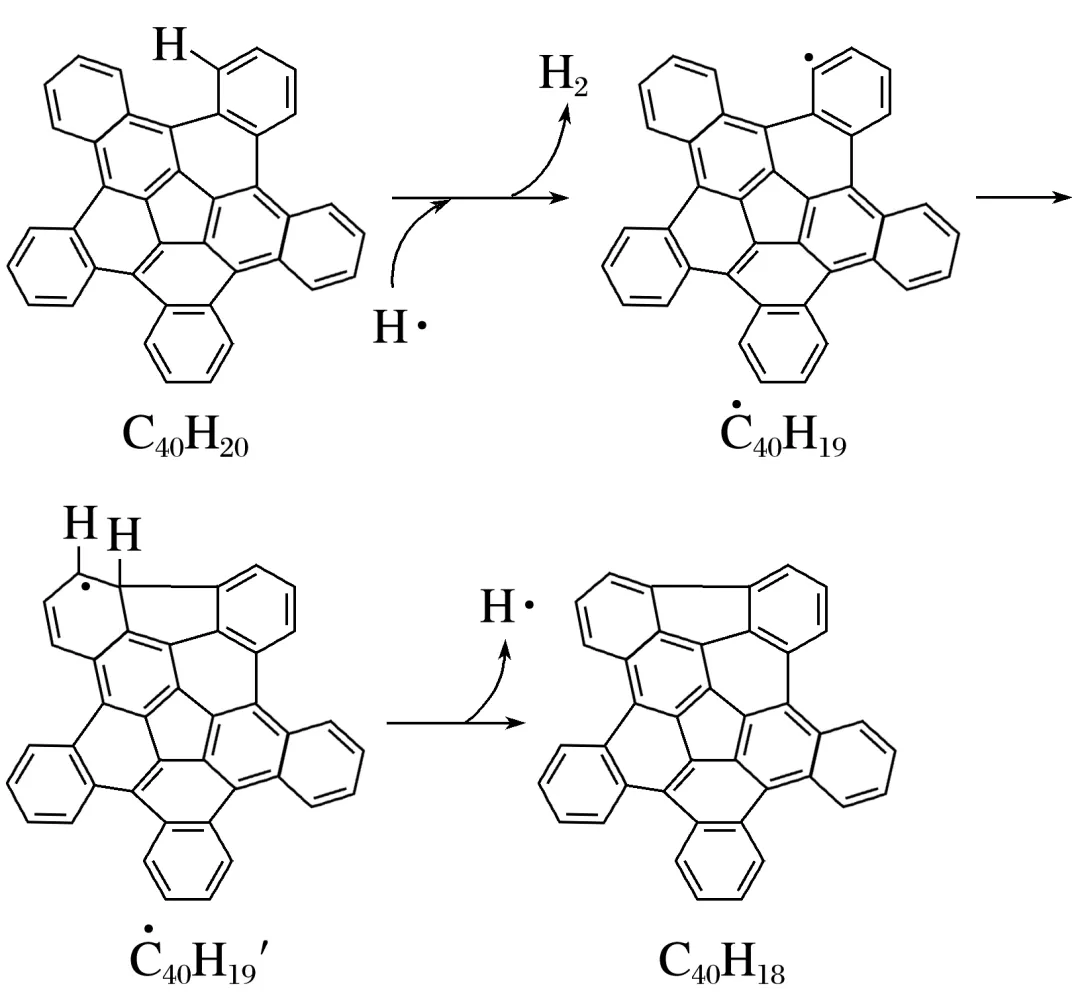
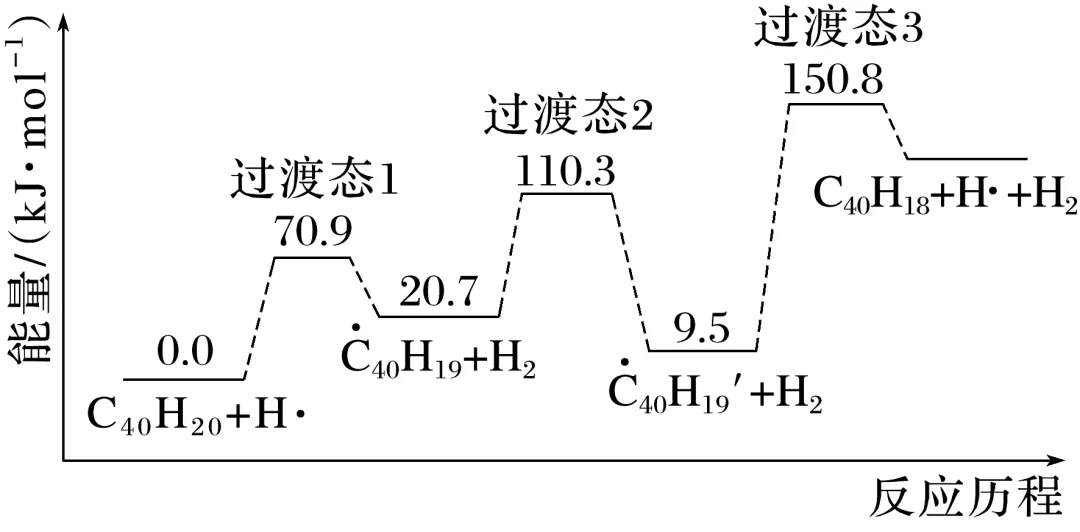
下列说法不正确的是( )
A.C40H20(g)C40H18(g)+H2(g)反应的ΔH=+128 kJ·mol-1
B.上述图示历程中包括3个基元反应,且第一个反应速率最快
C.根据上述反应机理,C40H10纳米碗中含6个五元环
D.升高温度和增大压强均既能增大生成C40H10的反应速率,又能提高反应物的平衡转化率
答案 D
解析由题干反应历程图可知,C40H20(g)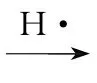 40H18(g)+H2(g)的ΔH=+128kJ·mol-1,A正确;该反应包含3个基元反应,分别为C40H20+H··C40H19+H2,·C40H19
40H18(g)+H2(g)的ΔH=+128kJ·mol-1,A正确;该反应包含3个基元反应,分别为C40H20+H··C40H19+H2,·C40H19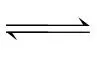 40H19'、·C40H19'C40H18+H·,其中第一个反应的活化能最小,反应速率最快,B正确;由C40H20的结构可知其中含有1个五元环,10个六元环,每脱两个氢形成一个五元环,则C40H10总共含有6个五元环,10个六元环,C正确;结合A的分析可知,生成C40H10的反应是气体分子数增大的吸热反应,则增大压强,平衡逆向移动,反应物转化率减小,D错误。
40H19'、·C40H19'C40H18+H·,其中第一个反应的活化能最小,反应速率最快,B正确;由C40H20的结构可知其中含有1个五元环,10个六元环,每脱两个氢形成一个五元环,则C40H10总共含有6个五元环,10个六元环,C正确;结合A的分析可知,生成C40H10的反应是气体分子数增大的吸热反应,则增大压强,平衡逆向移动,反应物转化率减小,D错误。
4.(2025·浙江高三普通高校招生模拟)已知Cl2溶于水存在以下平衡:
Ⅰ. Cl2+H2OHCl+HClO K1=4.0×10-4
Ⅱ. Cl-+Cl2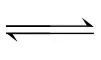
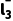 K2=0.20
K2=0.20
298 K时,测得Cl2在不同浓度的盐酸中的溶解度(见表)和盐酸浓度与溶解Cl2及含氯微粒变化关系(见图)。下列说法不正确的是( )
盐酸浓度/(mol·L-1) | 0.200 | 0.500 | 1.000 | 2.000 | 3.000 | 4.000 |
Cl2溶解度/(mol·L-1) | 0.062 0 | 0.063 0 | 0.066 5 | 0.740 | 0.083 0 | 0.091 0 |
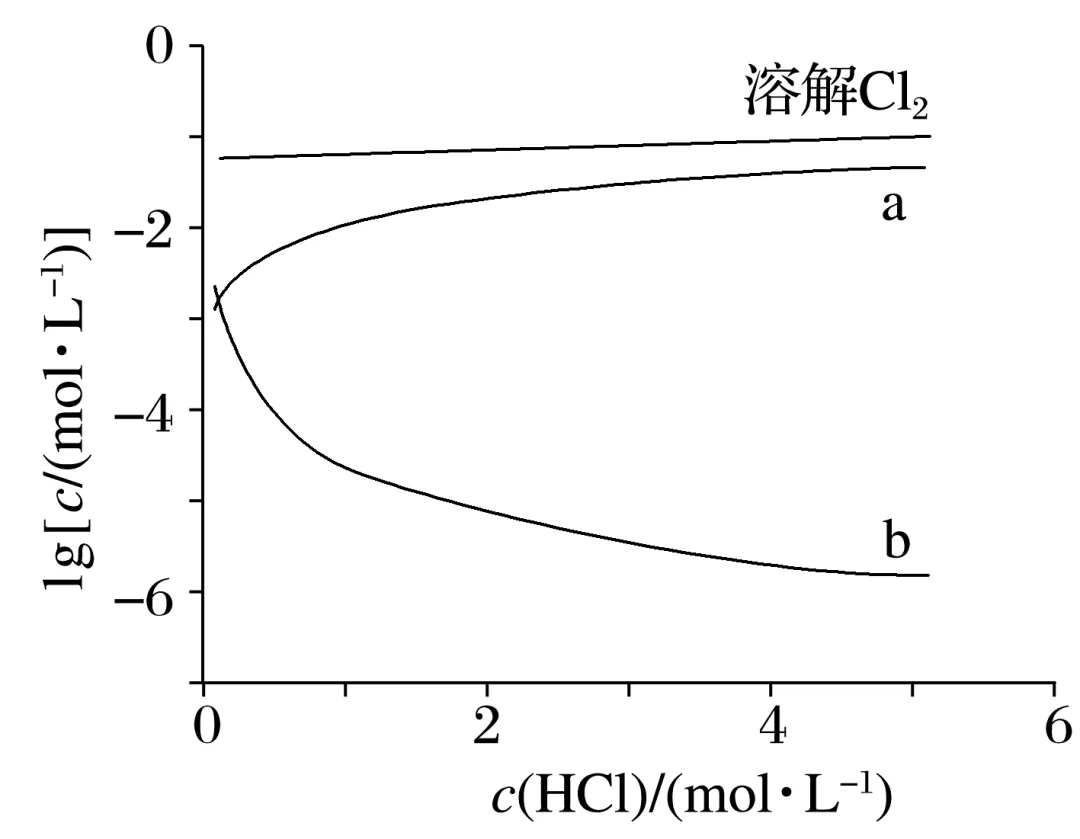
A.盐酸浓度越大,Cl2溶解度越大
B.当c(HCl)=1.000 mol·L-1时,溶液中c(Cl2)=0.053 0 mol·L-1,此时c(C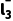 )<c(HClO)
)<c(HClO)
C.除去Cl2中的HCl气体时,为降低Cl2的溶解应使用浓NaCl溶液效果更佳
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享