
1.转化率、产率的计算公式
反应物的转化率= ×100%
×100%
生成物的产率= ×100%
×100%
2.分压与压强平衡常数
对于可逆反应:aA(g)+bB(g)cC(g)+dD(g),在一定温度下达到化学平衡时,若用p(A)、p(B)、p(C)、p(D)分别表示A、B、C、D各气体的分压,用Kp表示压强平衡常数,则有:
(1)p(C)=平衡时的总压×物质C的物质的量分数。
(2)Kp=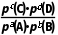 。
。
3.相关反应平衡常数的相互计算
(1)同一可逆反应中,K正·K逆=1。
(2)同一化学方程式中的化学计量数等倍扩大或缩小n倍,则新平衡常数K'与原平衡常数K间的关系是K'=Kn或K'=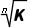 。
。
(3)几个可逆反应的化学方程式相加得总化学方程式,则总化学反应的平衡常数等于各分步反应平衡常数之积。
4.速率方程、速率常数及应用
对于基元反应:aA(g)+bB(g)dD(g)+eE(g)
(1)速率方程v正=k正·ca(A)·cb(B);v逆=k逆·cd(D)·ce(E)。
(2)速率常数(k)是一个与温度有关,而与浓度、压强无关的量。
(3)基元反应的平衡常数K=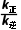 。
。
5.“三段式”法的计算模式
(1)

(2)模式:对反应mA(g)+nB(g)pC(g)+qD(g),设A、B起始物质的量分别为a mol、b mol,达到平衡后,A的消耗量为mx mol,容器容积为V L。
mA(g)+nB(g)pC(g)+qD(g)
始/mol ab 0 0
转/mol mxnxpxqx
平/mol a-mxb-nxpxqx
则有K=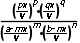 。
。

1.[2024·浙江1月选考,19(2)②]反应Ⅲ:CO2(g)+H2(g)HCOOH(g) ΔH3
在恒温、恒容的密闭容器中进行,CO2和H2的投料浓度均为1.0 mol·L-1,平衡常数K=2.4×10-8,则CO2的平衡转化率为。
答案 2.4×10-6%
解析根据三段式,设转化的CO2为xmol·L-1,则:
CO2(g)+H2(g)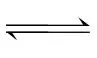 (g)
(g)
起始/(mol·L-1) 1.01.00
转化/(mol·L-1) xxx
平衡/(mol·L-1) 1.0-x1.0-xx
则K=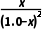 =2.4×10-8,x≈2.4×10-8,则转化率为
=2.4×10-8,x≈2.4×10-8,则转化率为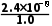 ×100%=2.4×10-6%。
×100%=2.4×10-6%。
2.[2023·浙江6月选考,19(2)①]水煤气变换反应是工业上的重要反应,可用于制氢。
水煤气变换反应:CO(g)+H2O(g)CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
恒定总压1.70 MPa和水碳比[n(H2O)/n(CO)=12∶5]投料,在不同条件下达到平衡时CO2和H2的分压(某成分分压=总压×该成分的物质的量分数)如下表:
| p(CO2)/MPa | p(H2)/MPa | p(CH4)/MPa |
条件1 | 0.40 | 0.40 | 0 |
条件2 | 0.42 | 0.36 | 0.02 |
在条件1下,水煤气变换反应的平衡常数K=。
答案 2
解析条件1下没有甲烷生成,只发生了水煤气变换反应,该反应是一个气体分子数不变的反应。设在条件1下平衡时容器的总体积为V,水蒸气和一氧化碳的投料分别为12mol和5mol,参加反应的一氧化碳为xmol,根据已知信息可得以下三段式:
CO(g)+H2O(g)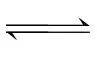 2(g)+H2(g)
2(g)+H2(g)
开始/mol 5 12 0 0
转化/mol xxxx
平衡/mol 5-x 12-xxx
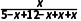 ×1.7MPa=0.40MPa,解得x=4。则平衡常数K=
×1.7MPa=0.40MPa,解得x=4。则平衡常数K=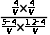 =2。
=2。
3.[2022·浙江6月选考,29(1)]主要成分为H2S的工业废气的回收利用有重要意义。
回收单质硫。将三分之一的H2S燃烧,产生的SO2与其余H2S混合后反应:
2H2S(g)+SO2(g)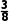 S8(s)+2H2O(g)。在某温度下达到平衡,测得密闭系统中各组分浓度分别为c(H2S)=2.0×10-5mol·L-1、c(SO2)=5.0×10-5 mol·L-1、c(H2O)=4.0×10-3 mol·L-1,计算该温度下的平衡常数K=。
S8(s)+2H2O(g)。在某温度下达到平衡,测得密闭系统中各组分浓度分别为c(H2S)=2.0×10-5mol·L-1、c(SO2)=5.0×10-5 mol·L-1、c(H2O)=4.0×10-3 mol·L-1,计算该温度下的平衡常数K=。
答案 8×108
解析根据方程式可知该温度下平衡常数K=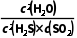 =
=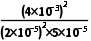 =8×108。
=8×108。
4.[2025·河南,17(6)]CaCO3的热分解与NixPy催化的CH4重整结合,可生产高纯度合成气(H2+CO),实现碳资源的二次利用。主要反应如下:
反应Ⅰ:CaCO3(s)CaO(s)+CO2(g) ΔH1=+178 kJ·mol-1
反应Ⅱ:CH4(g)+CO2(g)2H2(g)+2CO(g) ΔH2=+247 kJ·mol-1
反应Ⅲ:H2(g)+CO2(g)H2O(g)+CO(g) ΔH3=+41 kJ·mol-1
一定温度、100 kPa下,向体系中加入1.0 mol CaCO3和1.0 mol CH4,假设此条件下其他副反应可忽略,恒压反应至平衡时,体系中CaCO3转化率为80%,CH4转化率为60%,CO物质的量为1.3 mol,反应Ⅲ的平衡常数Kp=(保留小数点后一位),此时原位CO2利用率为。已知:原位CO2利用率= 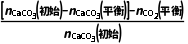 ×100%
×100%
答案 1.2 70%
解析 CaCO3平衡转化率为80%,则反应Ⅰ生成的n(CO2)=0.8mol,CH4平衡转化率为60%,则反应Ⅱ中CH4转化1mol×60%=0.6mol。列关系式:
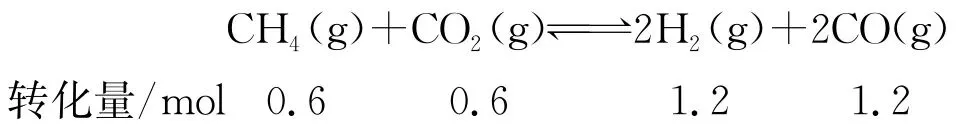
平衡时CO的物质的量为1.3mol,则反应Ⅲ生成0.1molCO,列关系式:
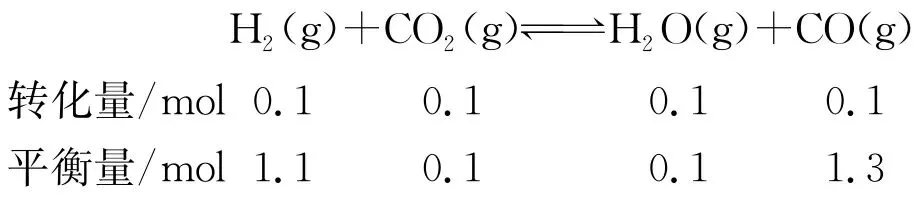
反应Ⅲ为气体分子数不变的反应,可用物质的量代替分压计算平衡常数,故反应Ⅲ的Kp=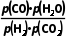 =
=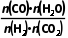 =
=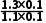 ≈1.2,原位CO2利用率=
≈1.2,原位CO2利用率=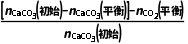 ×100%=
×100%=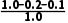 ×100%=70%。
×100%=70%。
5.[2025·河北,17(2)]煤化工路线中,利用合成气直接合成乙二醇,原子利用率可达100%,具有广阔的发展前景。反应如下:
2CO(g)+3H2(g)HOCH2CH2OH(g) ΔH
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享