
[分值:50分]
1.(18分)(2025·肇庆高三上多校联考)二氯化二硫(S2Cl2),沸点为138 ℃,常温下是一种金黄色液体,广泛应用于化工领域。
已知S2Cl2的性质:
ⅰ.热稳定性较差;
ⅱ.能被Cl2氧化为SCl2(沸点为59 ℃);
ⅲ.能与水发生剧烈反应:2S2Cl2+2H2O===3S↓+SO2↑+4HCl。
实验室制备S2Cl2。将氯气通入熔融硫黄(熔点为115 ℃,沸点为445 ℃)中反应制备S2Cl2。所用仪器(部分夹持、加热装置省略)如图所示:
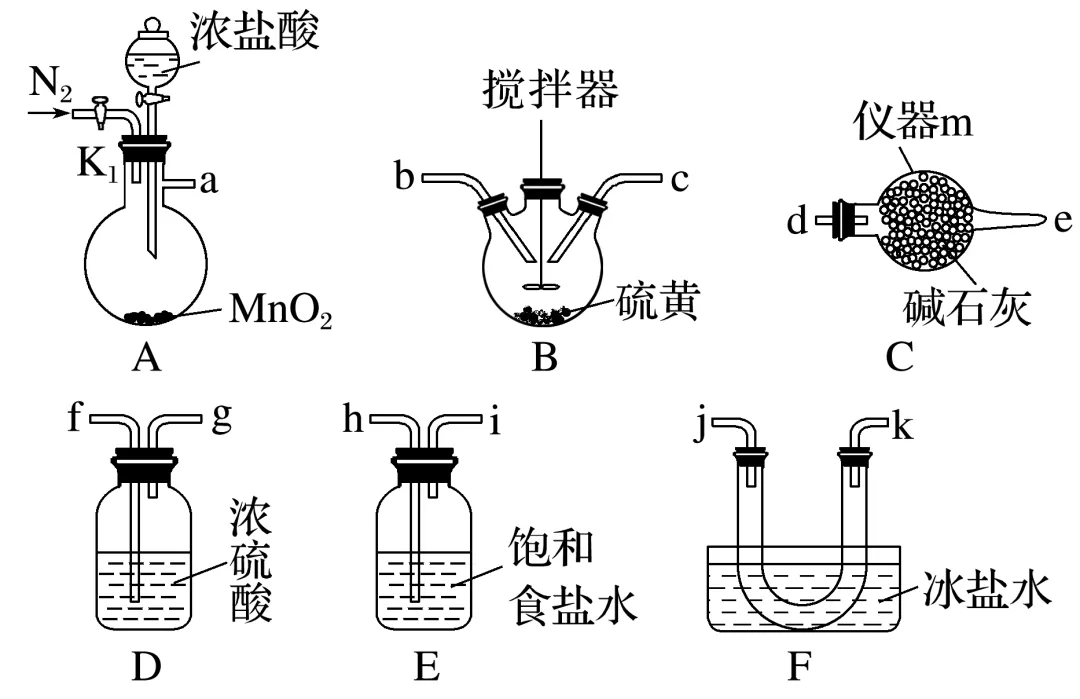
(1)仪器m的名称为。
(2)装置A中制备Cl2时反应的离子方程式为。
(3)E中饱和食盐水的作用是。
(4)制备过程实验装置的连接顺序为A→→C(填大写字母);装置C中所装碱石灰的作用有。
(5)组装仪器后,检查装置气密性,加入药品;打开K1,向装置中通一段时间N2,目的是排出装置内的空气,防止氧气与熔融的硫反应;再加热装置B至110~115 ℃之间使硫黄熔融,写出B中反应的化学方程式:。
(6)观察到F中出现金黄色液体时,可证明有S2Cl2生成。若实验产物中,经检验含有较多的SCl2,为提高产品纯度,减少SCl2的生成,可采取的措施为(任写一条即可)。
(7)测定S2Cl2样品的纯度(杂质不影响测定)。
称取a g样品于烧瓶中,加入足量的蒸馏水充分反应;用水蒸气将生成的SO2和HCl全部蒸出,并用足量的H2O2溶液充分吸收;然后向其中加入足量的BaCl2溶液,过滤、洗涤、干燥、称量,得到b g固体。样品中S2Cl2的质量百分含量为。
答案 (1)(球形)干燥管 (2)MnO2+4H++2Cl-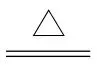 2++Cl2↑+2H2O (3)除去氯气中的HCl (4)E→D→B→F 吸收未反应的氯气,防止污染空气,同时吸收空气中的水蒸气,防止其进入装置F与S2Cl2反应 (5)Cl2+2SCl2S2 (6)减慢分液漏斗中浓盐酸的滴加速度(或打开K1通入适量N2等) (7)
2++Cl2↑+2H2O (3)除去氯气中的HCl (4)E→D→B→F 吸收未反应的氯气,防止污染空气,同时吸收空气中的水蒸气,防止其进入装置F与S2Cl2反应 (5)Cl2+2SCl2S2 (6)减慢分液漏斗中浓盐酸的滴加速度(或打开K1通入适量N2等) (7)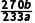 ×100%
×100%
解析由实验装置图可知,装置A中二氧化锰与浓盐酸共热反应制备氯气,浓盐酸具有挥发性,制得的氯气中混有氯化氢和水蒸气,装置E中的饱和食盐水用于除去氯化氢气体,装置D中盛有的浓硫酸用于干燥氯气,装置B中氯气与硫黄共热反应制备S2Cl2,装置F用于冷凝收集S2Cl2,装置C中盛有的碱石灰用于吸收未反应的氯气,防止污染空气,同时防止空气中的水蒸气进入装置F使S2Cl2水解。(7)根据反应2S2Cl2+2H2O===3S↓+SO2↑+4HCl、H2O2+SO2===H2SO4及H2SO4+BaCl2===BaSO4↓+2HCl可得关系:2S2Cl2~SO2~BaSO4,则样品中S2Cl2的含量为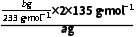 ×100%=
×100%=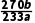 ×100%。
×100%。
2.(16分)(2025·广州一模)从含银废液中回收银是保护金属资源的有效途径。
(1)实验室用70% H2SO4和Na2SO3制取干燥的SO2,选择净化与收集SO2所需装置,接口连接顺序为。
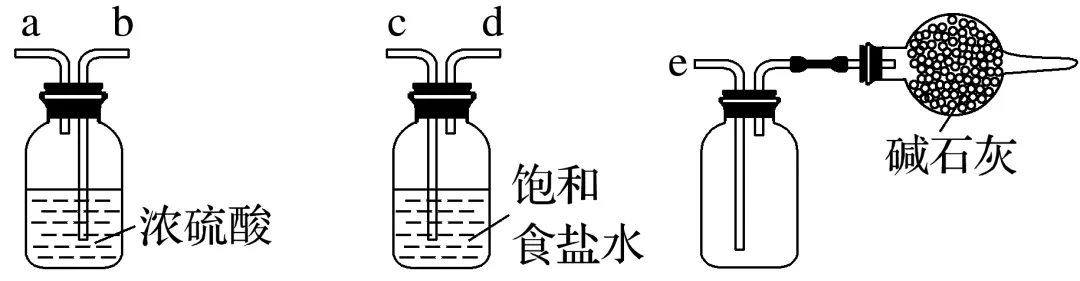
(2)兴趣小组探究从AgNO3溶液中回收银,将SO2通入一定体积0.1 mol·L-1的AgNO3溶液中(如图所示)。
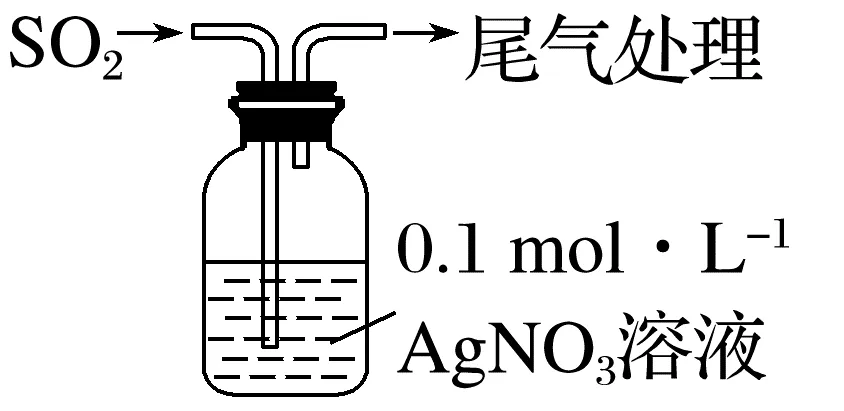
已知:a.25 ℃时,Ksp(Ag2SO3)=1.5×10-14,Ksp(Ag2SO4)=1.4×10-5。
b.Ag2SO3、Ag2SO4均能溶于浓氨水,生成[Ag(NH3)2]+。
ⅰ.实验现象
瓶内产生大量白色沉淀,瓶底沉淀略显灰色。
ⅱ.沉淀成分的分析
将瓶内混合物分离得到溶液和固体X。
①取固体X加入过量浓氨水中,固体大部分溶解,过滤,得到无色溶液和少量灰黑色固体:将灰黑色固体加入浓硝酸中,固体溶解,(填实验现象),说明沉淀中含有Ag。则SO2与AgNO3溶液反应生成银单质的离子方程式是。
②另取固体X加入过量盐酸中,充分反应后静置,取上层清液于试管中,(填实验操作和现象),说明沉淀中含有Ag2SO3,SO2与AgNO3溶液反应生成Ag2SO3的化学方程式是。
③实验进一步证明,沉淀中不含Ag2SO4原因是c2(Ag+)·c(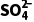 )1.4×10-5(填“>”“<”或“=”)。
)1.4×10-5(填“>”“<”或“=”)。
ⅲ.实验结论
SO2通入AgNO3溶液中同时发生复分解反应和氧化还原反应,Ag的回收率低。
④另取m1 g固体X进行定量分析,测得其中Ag的质量为m2 g,该条件下SO2与AgNO3溶液发生复分解反应和氧化还原反应的平均反应速率之比为。
(3)基于上述探究,兴趣小组重新设计了用SO2从AgNO3溶液中回收Ag的优化方案,避免了复分解反应的发生。该方案为。
答案 (1)b→a→e (2)①产生红棕色气体 SO2+2Ag++2H2O===2Ag↓+4H++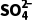 ②滴加品红溶液,溶液褪色 SO2+2AgNO3+H2O===Ag2SO3↓+2HNO3③< ④
②滴加品红溶液,溶液褪色 SO2+2AgNO3+H2O===Ag2SO3↓+2HNO3③< ④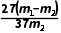 (3)将原溶液于试管中加入适量硫酸酸化,再向试管中通入SO2,过滤得到无色溶液和白色固体,将白色固体加入浓氨水,过滤得到的固体为Ag单质
(3)将原溶液于试管中加入适量硫酸酸化,再向试管中通入SO2,过滤得到无色溶液和白色固体,将白色固体加入浓氨水,过滤得到的固体为Ag单质
解析(1)70%的H2SO4和Na2SO3发生复分解反应生成Na2SO4、SO2、H2O,浓硫酸具有吸水性,且和SO2不反应,所以用浓硫酸干燥SO2;SO2的密度大于空气且能和碱石灰反应,所以用向上排空气法收集SO2,为防止污染空气,用碱石灰处理尾气,接口连接顺序为b→a→e。(2)①Ag和浓硝酸反应生成AgNO3、NO2和H2O,NO2为红棕色气体;SO2与AgNO3溶液反应生成银单质,Ag+被还原为Ag,则SO2被氧化为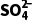 ,离子方程式为SO2+2Ag++2H2O===2Ag↓+4H++
,离子方程式为SO2+2Ag++2H2O===2Ag↓+4H++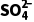 。②Ag2SO3和稀盐酸反应生成AgCl、SO2和H2O,SO2能使品红溶液褪色,则另取固体X加入过量盐酸中,充分反应后静置,取上层清液于试管中,滴加品红溶液,溶液褪色,说明沉淀中含有Ag2SO3;SO2与AgNO3溶液反应生成Ag2SO3和HNO3,反应的化学方程式为SO2+2AgNO3+H2O===Ag2SO3↓+2HNO3。③如果溶液中c2(Ag+)·c(
。②Ag2SO3和稀盐酸反应生成AgCl、SO2和H2O,SO2能使品红溶液褪色,则另取固体X加入过量盐酸中,充分反应后静置,取上层清液于试管中,滴加品红溶液,溶液褪色,说明沉淀中含有Ag2SO3;SO2与AgNO3溶液反应生成Ag2SO3和HNO3,反应的化学方程式为SO2+2AgNO3+H2O===Ag2SO3↓+2HNO3。③如果溶液中c2(Ag+)·c(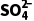 )<Ksp(Ag2SO4),则不含Ag2SO4沉淀,即沉淀中不含Ag2SO4,原因是c2(Ag+)·c(
)<Ksp(Ag2SO4),则不含Ag2SO4沉淀,即沉淀中不含Ag2SO4,原因是c2(Ag+)·c(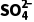 )<1.4×10-5。④另取m1g固体X进行定量分析,测得其中Ag的质量为m2g,该条件下SO2与AgNO3溶液发生复分解反应生成Ag2SO3的质量为(m1-m2)g,相同时间内其物质的量之比等于其反应速率之比,该条件下SO2与AgNO3溶液发生复分解反应(1molSO2生成1molAg2SO3)和氧化还原反应(1molSO2生成2molAg)的平均反应速率之比为
)<1.4×10-5。④另取m1g固体X进行定量分析,测得其中Ag的质量为m2g,该条件下SO2与AgNO3溶液发生复分解反应生成Ag2SO3的质量为(m1-m2)g,相同时间内其物质的量之比等于其反应速率之比,该条件下SO2与AgNO3溶液发生复分解反应(1molSO2生成1molAg2SO3)和氧化还原反应(1molSO2生成2molAg)的平均反应速率之比为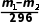 mol∶(
mol∶(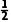 ×
×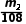 ) mol=
) mol=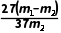 。
。
3.(16分)(2025·广东二模)Ⅰ.乙醇在化工、医疗、食品以及农业等领域都有广泛的用途。
(1)完成乙醇与酸性高锰酸钾溶液反应的离子方程式。
5C2H5OH+ +===5CH3COOH+Mn2++11H2O
+===5CH3COOH+Mn2++11H2O
(2)选择合适的装置验证乙醇的消去反应,装置的连接顺序为→g。溴的CCl4溶液中的现象为。

通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享