
[分值:50分]
1.(5分)[2024·浙江6月选考,17(3)]化合物HA、HB、HC和HD的结构如图。
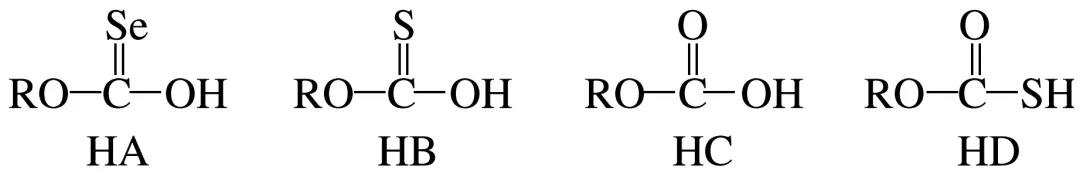
①HA、HB和HC中羟基与水均可形成氢键(—O—H…OH2),按照氢键由强到弱对三种酸排序:,请说明理由:。
②已知HC、HD钠盐的碱性:NaC>NaD,请从结构角度说明理由:。
答案①HC>HB>HA O、S、Se的电负性逐渐减小,键的极性:C==O>C==S>C==Se,使得HA、HB、HC中羟基的极性逐渐增大,羟基与H2O形成的氢键逐渐增强 ②原子半径:S>O,键长:S—H>O—H,S—H更易断键电离,因此HD酸性更强,酸根不易水解,故钠盐的碱性:NaC>NaD
2.(4分)[2021·河北,17(3)(4)](3)已知有关氮、磷的单键和三键的键能(kJ·mol-1)如表:
从能量角度看,氮以N2而白磷以P4(结构式可表示为)形式存在的原因是。
(4)已知KH2PO2是次磷酸的正盐,H3PO2的结构式为,其中P采取杂化方式。
答案 (3)在原子数目相同的条件下,N2比N4具有更低的能量,而P4比P2具有更低的能量,能量越低越稳定 (4) sp3
3.(3分)[2020·山东,17(2)]NH3、PH3、AsH3的沸点由高到低的顺序为(填化学式,下同),还原性由强到弱的顺序为,键角由大到小的顺序为。
答案 NH3、AsH3、PH3 AsH3、PH3、NH3 NH3、PH3、AsH3
4.(3分)碳和氧是构建化合物的常见元素。
某烃结构如图,带星号碳原子的杂化方式为;带星号碳原子与碳原子之间的键长比一般碳碳单键的键长要长,请从碳成键轨道的成分角度分析其原因:。
答案 sp2杂化 带星号的碳原子与碳原子之间是通过未杂化的两个p轨道形成的σ键,一般的碳碳单键是sp3杂化轨道“头碰头”形成,p轨道比sp3杂化轨道要伸展得更长,因此带星号碳原子与碳原子之间的键长更长
5.(3分)氨硼烷(NH3BH3)具有良好的储氢能力,分子中有配位键。则氨硼烷中H—N—H的键角(填“>”“<”或“=”)H—B—H的键角,理由是。
答案 > N和B的杂化方式相同,但N的电负性大于B,共用电子对偏向N,因此N附近电子对排斥力大,使得H—N—H的键角较大
6.(3分)S2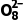 ()中的O —O比H2O2中的更(填“难”或“易”)断裂。其原因是。
()中的O —O比H2O2中的更(填“难”或“易”)断裂。其原因是。
答案 易 S2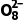 中的O —O与S相连,S的电负性大于H,即S对O —O中电子对的吸引力大于H对O —O中电子对的吸引力
中的O —O与S相连,S的电负性大于H,即S对O —O中电子对的吸引力大于H对O —O中电子对的吸引力
7.(3分)BF3形成的化合物中配位键的强度:BF3·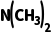 Cl(填“>”“<”或“=”)BF3·N(CH3)Cl2,理由是。
Cl(填“>”“<”或“=”)BF3·N(CH3)Cl2,理由是。
答案 > Cl电负性大,N(CH3)Cl2中Cl原子多,使N电子云密度降低,N的孤电子对不易给出,与BF3形成配位键,即形成的配位键稳定性低
8.(2分)常温下 AlCl3在四氯化碳中的溶解度大于MgCl2,理由是。
三乙基铝是一种金属有机物,结构简式为Al(C2H5)3,可作高能火箭燃料,原因是。
答案 AlCl3是非极性分子,极性比MgCl2小,四氯化碳是非极性溶剂,故AlCl3的溶解度更大 燃烧时释放出大量的热和大量气体
9.(2分)S2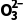 作为配体可提供孤电子对与Ag+形成
作为配体可提供孤电子对与Ag+形成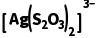 。分析判断S2
。分析判断S2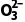 中的中心S原子和端基S原子能否作配位原子并说明理由:。
中的中心S原子和端基S原子能否作配位原子并说明理由:。
答案 S2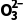 中的中心原子S的价层电子对数为4,无孤电子对,不能作配位原子;端基S原子含有孤电子对,能作配位原子
中的中心原子S的价层电子对数为4,无孤电子对,不能作配位原子;端基S原子含有孤电子对,能作配位原子
10.(4分)(1)已知HSCN的结构有两种,这两种分子结构中除氢外各原子均满足8电子稳定结构(无配位键),请画出沸点高的分子的结构式:。
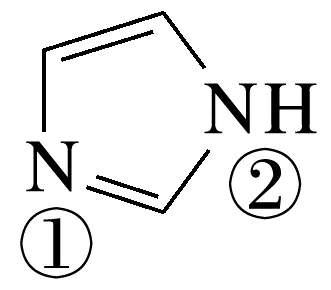
(2)杂环化合物咪唑结构如图,其分子中的大π键可表示为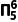 ,则其结合质子能力更强的氮原子是(填“①”或“②”),其原因是。
,则其结合质子能力更强的氮原子是(填“①”或“②”),其原因是。
答案 (1)H—N==C==S (2)①①号N原子的一个单电子和②号N原子的一个孤电子对参与形成大π键,①号N原子剩余1个孤电子对,使得①号N原子的电子云密度较大
11.(5分)(1)碘单质在CS2中的溶解度比在水中的大,解释原因:。
(2)HI主要用于药物合成,通常用I2和P反应生成PI3,PI3再水解制备HI。PI3的空间结构是,PI3水解生成HI的化学方程式是。
答案 (1)碘单质、CS2均为非极性分子,水为极性分子,所以根据相似相溶原理,碘单质在CS2中的溶解度比在水中的大 (2)三角锥形 PI3+3H2O===3HI+ H3PO3
12.(3分)同周期中第一电离能大于砷的元素有种。CH3As(OH)2与(CH3)2AsOH两种含砷有机酸中沸点较高的是(填化学式), 原因为。
答案 2 CH3As(OH)2 CH3As(OH)2与(CH3)2AsOH两种含砷有机酸均属于分子晶体,CH3As(OH)2含两个羟基,形成的氢键数目多,沸点高
13.(4分)(1)Mg和SiO2在高温下制备Si,同时生成MgO。MgO的熔点高于MgCl2的原因是。
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。EDTA可用于水的软化,软化水过程中形成的一种螯合物如图所示。1 mol该配合物中通过螯合作用形成的配位键有mol,配合物中碳原子的杂化方式为,键角1(填“>”“<”或“=”)键角2。
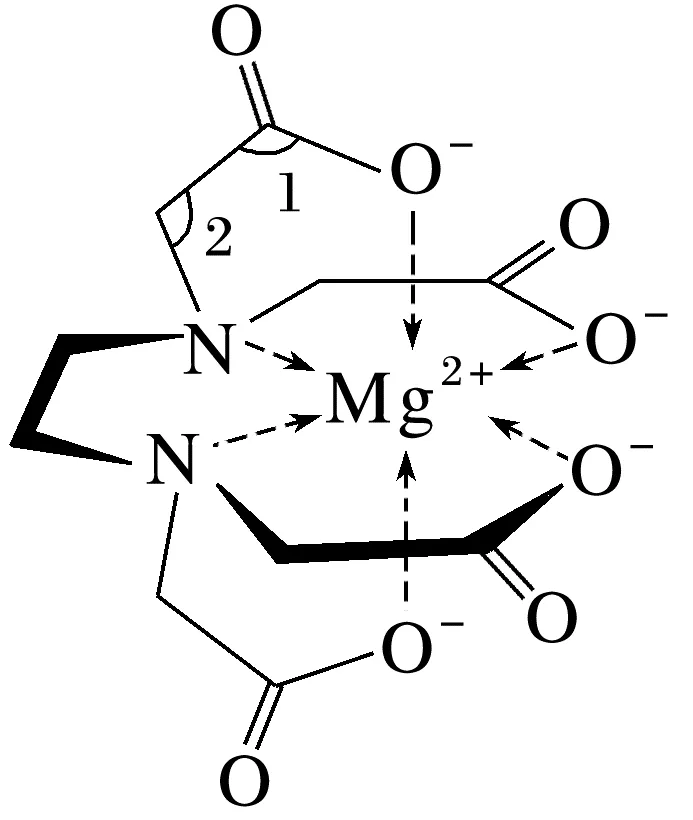
答案 (1)O2-半径小于Cl-半径,且O2-所带电荷数多,所以MgO的离子键较强,熔点较高 (2)6 sp2、sp3 >
解析(2)根据图中结构可知,1mol该配合物中通过螯合作用形成的配位键有6mol。配合物中饱和碳原子的杂化方式为sp3,C==O中碳原子的杂化方式为sp2。键角1的碳原子是sp2杂化,键角2的碳原子是sp3杂化,中心原子杂化轨道越多,形成的键角越小,故键角1>键角2。
14.(6分)向CuSO4溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含[Cu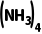 ]2+的铜氨溶液。
]2+的铜氨溶液。
(1)比较键角:NH3(填“大于”“小于”或“等于”,下同)N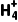 。
。
(2)该实验中,Cu2+与NH3结合能力Cu2+与H2O结合能力,解释原因:。
(3)经实验发现:金属铜与氨水和过氧化氢的混合溶液反应也可得到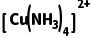 。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是, 反应的离子方程式为。
。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是, 反应的离子方程式为。
答案 (1)小于 (2)大于 电负性:O>N,因此Cu2+与H2O形成的配位键极性比Cu2+与NH3形成的配位键极性要强,更易断裂,即Cu2+与NH3的结合能力更强 (3)过氧化氢作氧化剂,可氧化Cu生成Cu2+,氨与Cu2+形成配离子,两者相互促进使反应进行 Cu+4NH3·H2O+H2O2===[Cu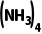 ]2++4H2O+2OH-
]2++4H2O+2OH-
解析(1)NH3中N原子的价层电子对数为4,有1个孤电子对,为sp3杂化,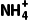 中N原子的价层电子对数为4,没有孤电子对,为sp3杂化,由于孤电子对对成键电子对的排斥力比成键电子对之间的排斥力大,因此
中N原子的价层电子对数为4,没有孤电子对,为sp3杂化,由于孤电子对对成键电子对的排斥力比成键电子对之间的排斥力大,因此 的键角更大。
的键角更大。
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享