
(一)配位键与配合物
1.配位键的形成
配位键是一种特殊的共价键,配体提供孤电子对,中心原子(或离子)提供空轨道形成配位键。
2.确定配体中配位原子的方法
(1)配体中有孤电子对的原子才可能成为配位原子。
(2)当配体中有多个原子含有孤电子对时,根据元素的电负性大小确定配位原子。元素的电负性越大,其原子越不容易提供孤电子对。如SCN-中C无孤电子对,S和N均有孤电子对,且电负性:N>S,所以形成配合物时,配位原子一般为S。
3.配位键的数目及配位数的判断
(1)单齿配体:只有一个配位原子的配体的配合物,中心离子的配位数=配体的数目。
指出下列配合物中的配位数:
K3[Fe(CN)6]配位数:6;[Co(NH3)5(H2O)]Cl3配位数:6。
(2)多齿配体:含有多个配位原子的配体。螯合物是由中心离子和多齿配体结合而成的具有环状结构的配合物,螯合物具有特殊的稳定性。
 例
例 。
。
答案 4
(2)[2019·全国卷Ⅲ,35(2)]FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为,其中Fe的配位数为。
答案 4
特别提醒配位数不一定等于中心原子(或离子)与配位原子形成的配位键数目,不一定等于配体的数目。当中心原子(或离子)同时形成共价键和配位键时,配位数不等于配位键数目;当中心原子(或离子)只形成配位键时,配位数等于配位键数目。
(二)超分子
1.由两种或两种以上的分子(包括离子)通过分子间相互作用形成的分子聚集体。
2.超分子内的作用力
主要是氢键、静电作用、范德华力、疏水作用以及一些分子与金属离子形成的弱配位键等。
3.重要特征及其应用
(1)分子识别,如“杯酚”分离C60和C70;“冠醚”识别碱金属离子。
(2)超分子自组装:在不受外力介入下,分子自行聚集、组织成规则结构的现象。超分子自组装过程是使超分子产生高度有序的过程。

1.(2025·浙江6月选考,13)能代表化合物(N2H5)2Zn(SO4)2的结构片段如图(氢原子未画出),下列有关该化合物的描述不正确的是( )
A.图中球①代表原子团NH2
B.该化合物易溶于水
C.作还原剂时,该化合物释放H+
D.氮原子上没有孤电子对,晶体中不存在氢键
答案 D
解析由结构片段和化合物化学式可知,各部分结构如图:
N2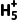 可表示为NH2—N
可表示为NH2—N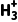 ,其中①号氮原子要提供孤电子对与Zn2+形成配位键,而—N
,其中①号氮原子要提供孤电子对与Zn2+形成配位键,而—N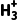 结构中无孤电子对,故①表示NH2,A正确;该化合物属于可溶性盐,且可与水形成氢键,因此易溶于水,B正确;作还原剂时,N2
结构中无孤电子对,故①表示NH2,A正确;该化合物属于可溶性盐,且可与水形成氢键,因此易溶于水,B正确;作还原剂时,N2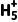 化合价升高,可能会发生反应释放H+,C正确;N2
化合价升高,可能会发生反应释放H+,C正确;N2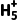 中①号氮原子与Zn2+形成配位键,旁边的氮原子与H+形成配位键,因此氮原子上没有孤电子对,但S
中①号氮原子与Zn2+形成配位键,旁边的氮原子与H+形成配位键,因此氮原子上没有孤电子对,但S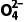 中含有氧原子,晶体中存在N—H…O氢键,D错误。
中含有氧原子,晶体中存在N—H…O氢键,D错误。
2.(2023·浙江1月选考,12)共价化合物Al2Cl6中所有原子均满足8电子稳定结构,一定条件下可发生反应:Al2Cl6+2NH3===2Al(NH3)Cl3,下列说法不正确的是( )
A.Al2Cl6的结构式为
B.Al2Cl6为非极性分子
C.该反应中NH3的配位能力大于氯
D.Al2Br6比Al2Cl6更难与NH3发生反应
答案 D
解析由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为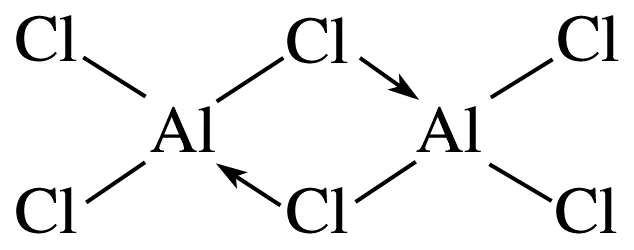 ,是结构对称的非极性分子,故A、B正确;由反应方程式可知,氨分子更易与具有空轨道的铝原子形成配位键,配位能力大于氯原子,故C正确;溴元素的电负性小于氯元素,溴原子半径大于氯原子,则铝溴键弱于铝氯键,所以双聚溴化铝的铝溴键更易断裂,比双聚氯化铝更易与氨气反应,故D错误。
,是结构对称的非极性分子,故A、B正确;由反应方程式可知,氨分子更易与具有空轨道的铝原子形成配位键,配位能力大于氯原子,故C正确;溴元素的电负性小于氯元素,溴原子半径大于氯原子,则铝溴键弱于铝氯键,所以双聚溴化铝的铝溴键更易断裂,比双聚氯化铝更易与氨气反应,故D错误。
3.(2025·诸暨高三一模)硼原子具有缺电子的特性,与N、H可形成,其中B—N为配位键。下列说法不正确的是( )
A.BCl3易水解,生成H3BO3和HCl
B.乙硼烷(B2H6)的结构为
C.H3BO3为一元弱酸,其电离方程式为B(OH)3+H2OB(OH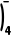 +H+
+H+
D.N(CH3)3为极性分子,空间结构与NH3相似;N(SiH3)3为非极性分子,故可推测其碱性(碱性:结构中有孤电子对,能接受H+)比N(CH3)3弱很多
答案 B
解析三氯化硼在溶液中易发生水解反应,水分子中的1个O—H断裂,B原子与3个—OH结合为硼酸B(OH)3,H原子与Cl原子结合为HCl,故A正确;由共价键的饱和性和硼原子具有缺电子的特性可知,乙硼烷的结构为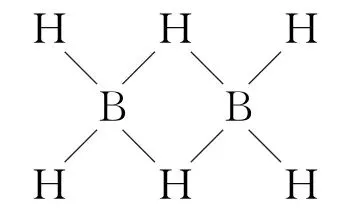 ,故B错误;一元弱酸硼酸在溶液中能与水电离出的氢氧根离子结合生成四羟基合硼酸根离子而使溶液呈酸性,电离方程式为B(OH)3+H2OB(OH
,故B错误;一元弱酸硼酸在溶液中能与水电离出的氢氧根离子结合生成四羟基合硼酸根离子而使溶液呈酸性,电离方程式为B(OH)3+H2OB(OH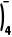 +H+,故C正确;N(CH3)3为极性分子,中心N原子采取sp3杂化,孤电子对占据sp3杂化轨道,方向性明确,空间位阻较小,易于接受H+,而N(SiH3)3为非极性分子,中心N原子采取sp2杂化,孤电子对占据p轨道,离—SiH3较近,且—SiH3基团体积远大于—CH3,使得3个—SiH3在N周围形成较大的空间位阻,孤电子对难以接受H+,所以N(SiH3)3的碱性比N(CH3)3弱很多,故D正确。
+H+,故C正确;N(CH3)3为极性分子,中心N原子采取sp3杂化,孤电子对占据sp3杂化轨道,方向性明确,空间位阻较小,易于接受H+,而N(SiH3)3为非极性分子,中心N原子采取sp2杂化,孤电子对占据p轨道,离—SiH3较近,且—SiH3基团体积远大于—CH3,使得3个—SiH3在N周围形成较大的空间位阻,孤电子对难以接受H+,所以N(SiH3)3的碱性比N(CH3)3弱很多,故D正确。
4.(2025·甘肃,9)我国化学家合成了一种带有空腔的杯状主体分子(结构式如图a),该分子和客体分子(CH3)4NCl可形成主客体包合物:(CH3)4N+被固定在空腔内部(结构示意图见图b)。下列说法错误的是( )
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享