
1.共价键、离子键、金属键的比较
| 共价键 | 离子键 | 金属键 |
存在 | 分子或物质内部 |
强弱判断 | 键长越短,键能越大,共价键越强 | ①电荷越大,离子键越强;②成键的阴、阳离子半径越小,离子键越强 | ①与金属阳离子所带电荷成正比; ②与阳离子半径成反比; ③与价电子数多少成正比 |
对物质性质的影响 | 化学性质 | 物理性质和化学性质 | 物理性质和化学性质 |
2.共价键
(1)共价键的类型
①按成键原子间共用电子对的数目分为单键、双键和三键。
②按共用电子对是否偏移分为极性键、非极性键。
③按原子轨道的重叠方式分为σ键和π键,σ键的电子云具有轴对称性,可以绕轴旋转;π键的电子云具有镜面对称性,不可以绕轴旋转。
(2)σ键、π键的判断
①由轨道重叠方式判断:“头碰头”重叠为σ键,“肩并肩”重叠为π键,重叠程度更大的是σ键。
②由共用电子对数判断:单键为σ键;双键或三键,其中一个为σ键,其余为π键。
③由成键轨道类型判断:s轨道形成的共价键全部是σ键;杂化轨道形成的共价键全部为σ键。
(3)键参数与物质性质的关系

一般情况:元素非金属性越强原子半径越小共价键键长越短键能越大。
(4)共价键的极性对物质性质的影响
①共价键的极性由成键两原子的电负性(吸引电子能力)差异决定,电负性差值越大,键的极性越大。
②共价键的极性还与周围化学环境有关(诱导效应),连有推电子基团的极性减弱,连有吸电子基团的极性增强。

考向一键长、键能与物质的化学性质
1.黑火药爆炸时发生的反应为S+2KNO3+3CK2S+N2↑+3CO2↑。该反应涉及元素中,比较属于同一主族的元素的气态氢化物的稳定性强弱:,从原子结构角度分析原因:。
答案 H2O>H2S 原子半径:O <S,键长:H—OH—S,所以稳定性:H </S,键长:H—O2O>H2S
2.从不同角度解释分子的稳定性。
(1)氮原子易形成N2,不易形成N4,而磷原子易形成P4(结构式可表示为),不易形成P2。
化学键 | N—N | N≡N | P—P | P≡P |
键能/(kJ·mol-1) | 193 | 946 | 197 | 489 |
从键能的角度解释原因:。
答案 在原子数目相同的条件下,形成N2比N4释放出更多能量,N2能量更低、更能稳定存在;而形成P4比P2释放出更多能量,P4能量更低、更能稳定存在
(2)F2比O2更容易与H2反应
化学键 | F—F | O==O | H—F | H—O |
键能/(kJ·mol-1) | 158 | 498 | 567 | 463 |
①从非金属性的角度解释原因:。
答案 F比O的非金属性强,对电子的吸引力更强,更容易与H2化合形成高稳定性的HF
②从键能的角度解释:。
答案 O2分子内形成共价双键,而F2分子内形成共价单键,而键能:O==O>F—F,F2断裂化学键吸收的能量低,且F2与H2反应生成HF时,形成的H—F的键能比O2与H2反应生成的H—O的键能大,体系能量降低更显著,反应更易进行
考向二共价键的极性与含氧酸的酸性
3.[2024·浙江6月选考,17(3)]化合物HA、HB、HC和HD的结构如图。
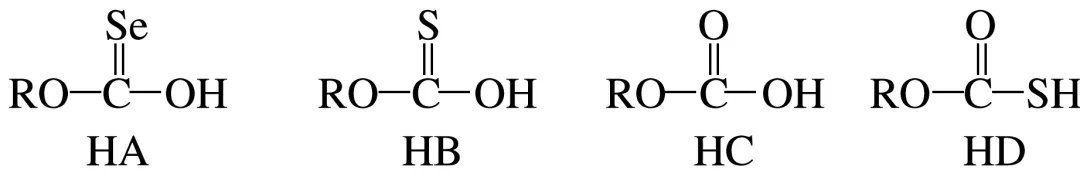
①HA、HB和HC中羟基与水均可形成氢键(—O—H…OH2),按照氢键由强到弱对三种酸排序:,请说明理由:。
②已知HC、HD钠盐的碱性:NaC>NaD,请从结构角度说明理由:。
答案①HC>HB>HA O、S、Se的电负性逐渐减小,键的极性:C==O>C==S>C==Se,使得HA、HB、HC中羟基的极性逐渐增大,羟基与H2O形成的氢键逐渐增强 ②原子半径:S>O,键长:S—H>O—H,S—H更易断键电离,因此HD酸性更强,碱性:NaC>NaD
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享