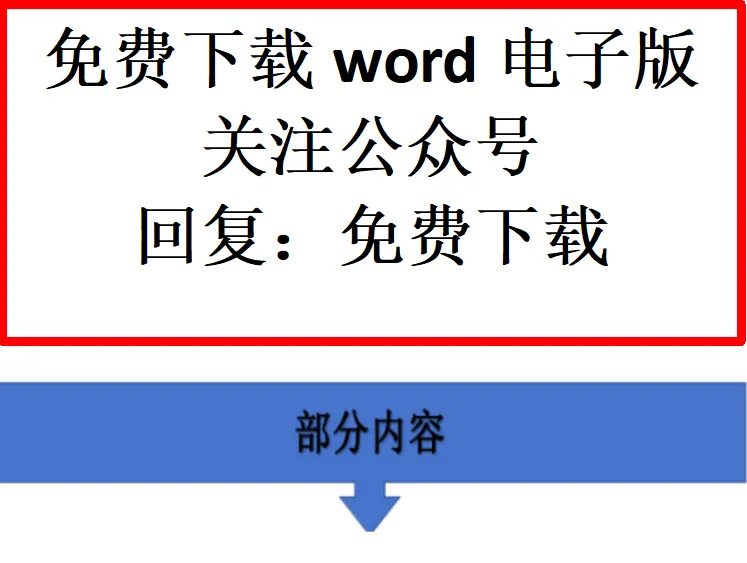

1.判断分子(离子)空间结构的思维模型
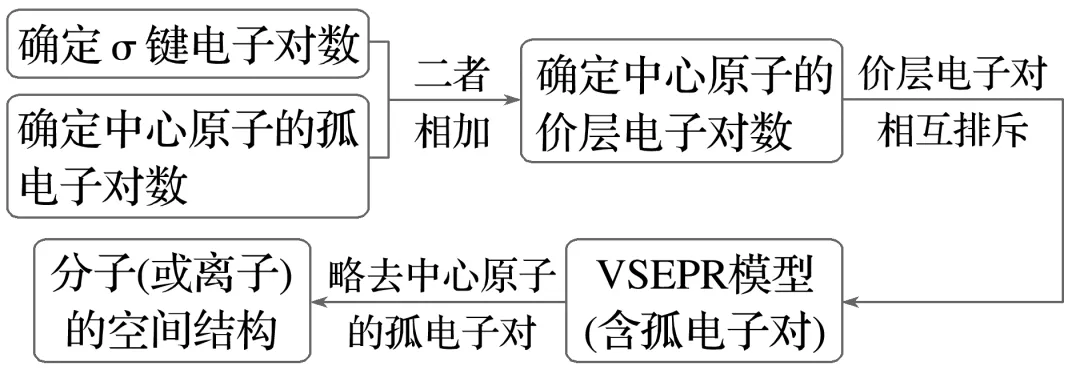
2.价层电子对数、杂化轨道类型、空间结构的关系
实例 | σ键电子 对数 | 孤电子 对数 | 价层电 子对数 | 中心原子杂 化轨道类型 | VSEPR 模型 | 分子(离子) 空间结构 |
BeCl2、CS2 | 2 | 0 | 2 | sp | 直线形 | 直线形 |
BF3、SO3、C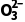 | 3 | 0 | 3 | sp2 | 平面 三角形 | 平面三角形 |
O3、SO2 | 2 | 1 | sp2 | V形 |
SnCl4、P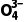 、N 、N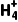 | 4 | 0 | 4 | sp3 | 四面 体形 | 正四面体形 |
PH3、S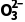 | 3 | 1 | sp3 | 三角锥形 |
H2S、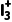 | 2 | 2 | sp3 | V形 |
注原子总数相同、价电子总数相同的分子(或离子)互为等电子体。等电子体具有相同的结构特征(空间结构和化学键类型)。
3.判断中心原子杂化轨道类型的“三方法”
(1)根据中心原子的价层电子对数判断
中心原子价层电子对数 | 2 | 3 | 4 | 5 | 6 |
杂化轨道类型 | sp | sp2 | sp3 | sp3d | sp3d2 |
(2)根据分子的结构式判断(一般用于有机物分子中C、N的杂化轨道类型判断)
杂化轨道类型 | sp3 | sp2 | sp |
C的成键方式 | 4个单键 | 1个双键和2个单键 | 2个双键或1个三键和1个单键 |
N的成键方式 | 3个单键 | 1个双键和1个单键 | 1个三键 |
注意当C、N形成平面结构的大π键时,均为sp2杂化。
(3)根据键角判断
若键角为109°28'或接近109°28',则为sp3杂化;若键角为120°或接近120°,则为sp2杂化;若键角为180°,则为sp杂化。
4.键角大小比较方法
(1)杂化轨道类型不同:键角sp>sp2>sp3。
(2)杂化轨道类型相同
①孤电子对数越多,键角越小。
②孤电子对数相同,中心原子电负性越大,键角越大。
③孤电子对数相同,中心原子相同,配位原子电负性越大,键角越小。
(3)单键、双键、三键之间的排斥力大小顺序:三键—三键>三键—双键>双键—双键>双键—单键>单键—单键。
5.大π键
(1)条件:参与原子共面或共线,有未杂化的p轨道(s轨道和杂化轨道不能参与,氢原子不参与)。
(2)表示: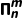 ,其中n代表成键的原子数(或参与的p轨道数),m代表形成大π键的电子数,原则m≤2n。
,其中n代表成键的原子数(或参与的p轨道数),m代表形成大π键的电子数,原则m≤2n。
(3)判断:①题给信息认定;②空间结构原子共面(或直线);③有未杂化p轨道(主要是sp2、sp杂化的原子,非sp3杂化的原子)。
(4)大π键的性质
①导电性:在大π键形成的高聚物中,电子能在大π键中移动,在电场作用下形成电流,成为导电聚合物。如聚乙炔和石墨的导电。
②稳定性:形成大π键后,结构稳定,能量趋于降低。
③平均键:形成大π键后,键长介于单键和双键之间,趋于平均化。如苯环为正六边形。

1.(2025·黑吉辽蒙,3)Cl2O可用于水的杀菌消毒,遇水发生反应:Cl2O+H2O===2HClO。下列说法正确的是( )
A.反应中各分子的σ键均为p⁃p σ键
B.反应中各分子的VSEPR模型均为四面体形
C.Cl—O键长小于H—O键长
D.HClO分子中Cl的价电子层有2个孤电子对
答案 B
解析水分子中的H—Oσ键和HClO中的H—Oσ键均为s⁃pσ键,A错误;Cl2O中O的价层电子对数为4,H2O中O的价层电子对数为4,HClO中O的价层电子对数为4,故反应中各分子的VSEPR模型均为四面体形,B正确;原子半径:H <Cl,故Cl—O键长大于H—O键长,C错误;HClO的电子式为< span>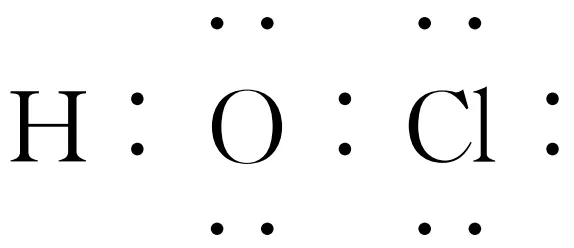 ,故Cl的价电子层有3个孤电子对,D错误。</Cl,故Cl—O键长大于H—O键长,C错误;HClO的电子式为<>
,故Cl的价电子层有3个孤电子对,D错误。</Cl,故Cl—O键长大于H—O键长,C错误;HClO的电子式为<>
2.(2024·河北,9)NH4ClO4是火箭固体燃料重要的氧载体,与某些易燃物作用可全部生成气态产物,如:NH4ClO4+2C===NH3↑+2CO2↑+HCl↑。下列有关化学用语或表述正确的是( )
A.HCl的形成过程可表示为
B.NH4ClO4中的阴、阳离子有相同的VSEPR模型和空间结构
C.在C60、石墨、金刚石中,碳原子有sp、sp2和sp3三种杂化方式
D.NH3和CO2都能作制冷剂是因为它们有相同类型的分子间作用力
答案 B
解析 HCl是共价化合物,其电子式为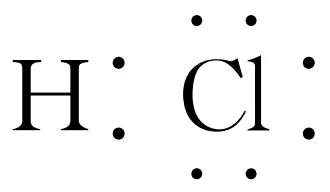 的形成过程可表示为
的形成过程可表示为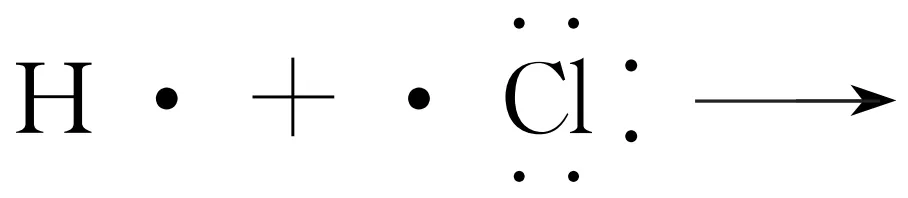 错误;NH4ClO4中
错误;NH4ClO4中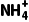 的中心N原子的孤电子对数为
的中心N原子的孤电子对数为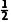 ×(5-1-4)=0,价层电子对数为4,的中心Cl原子的孤电子对数为
×(5-1-4)=0,价层电子对数为4,的中心Cl原子的孤电子对数为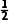 ×(7+1-2×4)=0,价层电子对数为4,则二者的VSEPR模型和空间结构均为正四面体形,B正确;C60、石墨、金刚石中碳原子的杂化方式分别为sp2、sp2、sp3,C错误;NH3易液化,液氨汽化时吸收大量热量,可作制冷剂,干冰易升华,升华时吸收大量热量,也可作制冷剂,NH3分子间作用力为氢键和范德华力,CO2分子间作用力为范德华力,D错误。
×(7+1-2×4)=0,价层电子对数为4,则二者的VSEPR模型和空间结构均为正四面体形,B正确;C60、石墨、金刚石中碳原子的杂化方式分别为sp2、sp2、sp3,C错误;NH3易液化,液氨汽化时吸收大量热量,可作制冷剂,干冰易升华,升华时吸收大量热量,也可作制冷剂,NH3分子间作用力为氢键和范德华力,CO2分子间作用力为范德华力,D错误。
3.[2024·浙江1月选考,17(3)]氮和氧是构建化合物常见元素
已知:
 2O
2O
①H2N—NH2+H+ 2N—N
2N—N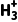 ,其中—NH2的N原子杂化方式为;比较键角∠HNH:H2N—NH2中的—NH2(填“>”“<”或“=”)H2N—N
,其中—NH2的N原子杂化方式为;比较键角∠HNH:H2N—NH2中的—NH2(填“>”“<”或“=”)H2N—N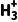 中的—N
中的—N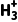 ,请说明理由。
,请说明理由。
②将HNO3与SO3按物质的量之比1∶2发生化合反应生成A,测得A由2种微粒构成,其中之一是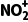 。比较氧化性强弱:N
。比较氧化性强弱:N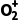 HNO3(填“>”“<”或“=”);写出A中阴离子的结构式。
HNO3(填“>”“<”或“=”);写出A中阴离子的结构式。
答案①sp3 < —NH2中心原子上有孤电子对,孤电子对对成键电子对排斥力大,键角变小 ②> 
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享