
1.物质分离提纯的化学方法总结
方法 | 原理 | 杂质成分 |
沉淀法 | 将杂质离子转化为沉淀 | 如Cl-、S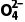 、C 、C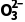 及能形成沉淀的阳离子 及能形成沉淀的阳离子 |
气化法 | 将杂质离子转化为气体 | 如C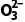 、HC 、HC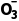 、S 、S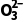 、HS 、HS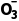 、S2-、N 、S2-、N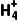 |
杂转纯法 | 将杂质转化为需要提纯的物质 | 如杂质中含不同价态的相同元素(用氧化剂或还原剂)、同一种酸的正盐与酸式盐(用酸、酸酐或碱) |
氧化还原法 | 用氧化剂(还原剂)除去具有还原性(氧化性)的杂质 | 如用酸性KMnO4溶液除去CO2中的SO2、用灼热的铜网除去N2中的O2 |
热分解法 | 加热使不稳定的物质分解除去 | 如除去NaCl中的NH4Cl |
酸碱溶解法 | 利用物质与酸或碱溶液混合后的差异进行分离 | 如用过量的NaOH溶液除去Fe2O3中的Al2O3 |
2.工艺流程中条件控制方法总结
(1)固体原料粉碎或研磨:减小颗粒直径,增大反应物接触面积,增大浸取时的反应速率,提高浸取率。
(2)煅烧或灼烧:①除去硫、碳单质;②有机物转化、除去有机物;③高温下原料与空气中的氧气反应;④除去热不稳定的杂质等。
(3)酸浸:①溶解转变成可溶物进入溶液中,以达到与难溶物分离的目的;②去氧化物(膜)。
(4)碱溶:①除去金属表面的油污;②溶解铝、氧化铝等。
(5)加热:①加快反应速率或溶解速率;②促进平衡向吸热反应方向移动;③除杂,除去热不稳定的杂质,如NaHCO3、Ca(HCO3)2、KMnO4、NH4Cl等物质;④使沸点相对较低或易升华的原料变为气体;⑤煮沸时促进溶液中的气体(如氧气)逸出等。
(6)反应物用量或浓度:①酸浸时提高酸的浓度可提高矿石中某金属元素的浸取率;②增大便宜、易得的反应物的浓度,可以提高其他物质的转化率,使反应充分进行;③增大物质浓度可以加快反应速率,使平衡发生移动等。
(7)控温(常用水浴、冰浴或油浴):①控制反应速率(升温加快反应速率)、适宜的温度使催化剂的活性最大,防止副反应的发生;②控制化学反应进行的方向,使化学平衡移动;③升温:使溶液中的气体逸出,使易挥发物质挥发,使易分解的物质分解;煮沸:使气体逸出;促进水解,聚沉后利于过滤分离;④控制固体的溶解与结晶。
(8)加入氧化剂(或还原剂):①转化为目标产物的价态;②除去杂质离子[如把Fe2+氧化成Fe3+,而后调溶液的pH,使其转化为Fe(OH)3沉淀除去]。
(9)加入沉淀剂:①生成硫化物沉淀(如加入硫化钠、硫化铵、硫化亚铁等);②加入可溶性碳酸盐,生成碳酸盐沉淀;③加入氟化钠,除去Ca2+、Mg2+。
(10)pH控制:①使某种或几种金属离子转化为氢氧化物沉淀,而目标离子不生成沉淀,以达到分离的目的(常利用题给金属离子开始沉淀和完全沉淀的pH信息,选择pH范围,使杂质离子以氢氧化物形式沉淀出来);②“酸作用”还可以除去氧化物(膜)、抑制某些金属离子的水解等;③“碱作用”还可以除去油污、除去铝片表面的氧化铝、溶解铝等;④金属离子的萃取率与溶液的pH密切相关;⑤调节溶液pH常用试剂:a.调节溶液呈酸性:稀盐酸、稀硫酸、稀硝酸(注意氧化性)、金属氧化物、酸性气体(二氧化硫)等。b.调节溶液呈碱性:氢氧化钠、氨水、碳酸钠、碳酸氢铵等。

1.(2025·浙江6月选考,4)下列实验原理或方法不正确的是( )
A.可用CCl4萃取碘水中的I2
B.可用重结晶法提纯含有少量NaCl的苯甲酸
C.可用浓NaOH溶液除去乙酸乙酯中的乙酸
D.可用浓Na2CO3溶液将CaSO4转化为CaCO3
答案 C
解析 I2在CCl4中的溶解度比在水中大,且CCl4和水不互溶,因此可用CCl4萃取碘水中的I2,A正确;苯甲酸的溶解度随温度升高而显著增大,而NaCl的溶解度受温度影响较小,可通过重结晶的方法达到提纯的目的,B正确;NaOH溶液与乙酸乙酯和乙酸均反应,不能达到目的,C错误;CaSO4的Ksp大于CaCO3,用浓Na2CO3溶液可将CaSO4转化为CaCO3,D正确。
2.(2024·浙江1月选考,6)为回收利用含I2的CCl4废液,某化学兴趣小组设计方案如下所示,下列说法不正确的是( )
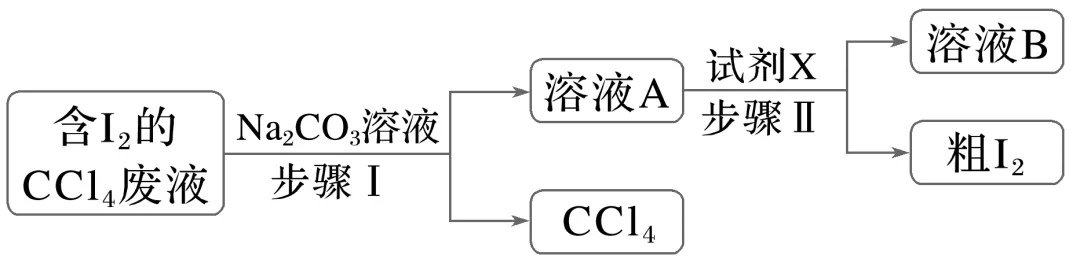
A.步骤Ⅰ中,加入足量Na2CO3溶液充分反应后,上下两层均为无色
B.步骤Ⅰ中,分液时从分液漏斗下口放出溶液A
C.试剂X可用硫酸
D.粗I2可用升华法进一步提纯
答案 B
解析步骤Ⅰ中,加入足量碳酸钠溶液与碘反应得到含有碘化钠和碘酸钠的混合溶液,则充分反应后,上下两层均为无色,上层为含有碘化钠和碘酸钠的混合溶液,下层为四氯化碳,分液时应从分液漏斗上口倒出溶液A,故A正确、B错误;向溶液A中加入硫酸溶液的目的是使碘化钠和碘酸钠在硫酸溶液中发生归中反应生成硫酸钠、碘和水,则试剂X可用硫酸,故C正确;碘受热会发生升华,所以实验制得的粗碘可用升华法进一步提纯,故D正确。
3.(2025·浙江1月选考,10)提纯NaCl粗品(含少量的Mg2+、Ca2+、K+和S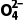 )得到NaCl纯品的方案如下,所用试剂为BaCl2溶液、Na2CO3溶液、盐酸和NaOH溶液。
)得到NaCl纯品的方案如下,所用试剂为BaCl2溶液、Na2CO3溶液、盐酸和NaOH溶液。
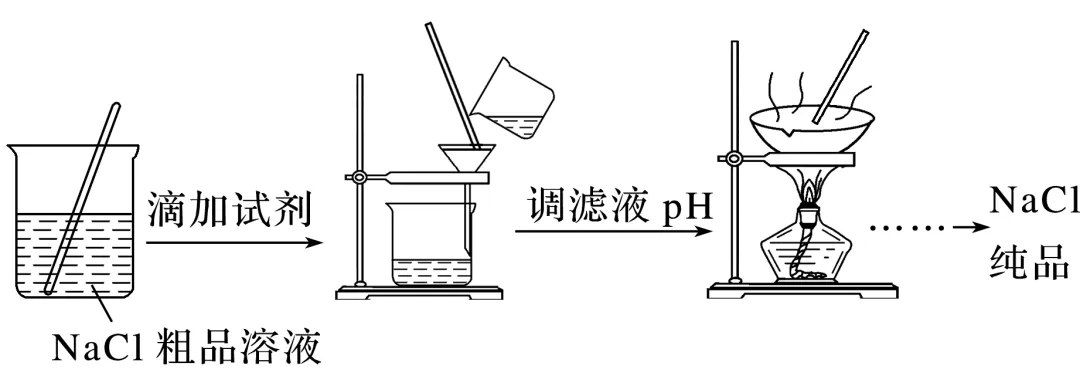
下列说法不正确的是( )
A.用过量的BaCl2溶液除去S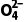
B.Mg2+、Ca2+、S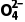 通过生成沉淀后过滤除去
通过生成沉淀后过滤除去
C.4种试剂的使用顺序为BaCl2溶液、Na2CO3溶液、盐酸、NaOH溶液
D.调pH后的滤液蒸发至大量固体析出,趁热过滤、洗涤、干燥后即得NaCl纯品
答案 C
解析粗盐溶液中的Ca2+用Na2CO3溶液除去,Mg2+用NaOH溶液除去,S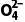 用BaCl2溶液除去,Na2CO3溶液要放到BaCl2溶液之后,还可以除去多余的Ba2+,过滤后再加HCl调节pH除去多余的Na2CO3和NaOH,最后再将滤液蒸发至大量固体析出,趁热过滤,让K+留在母液中,对沉淀进行洗涤、干燥后即得NaCl纯品,故A、B、D正确,C错误。
用BaCl2溶液除去,Na2CO3溶液要放到BaCl2溶液之后,还可以除去多余的Ba2+,过滤后再加HCl调节pH除去多余的Na2CO3和NaOH,最后再将滤液蒸发至大量固体析出,趁热过滤,让K+留在母液中,对沉淀进行洗涤、干燥后即得NaCl纯品,故A、B、D正确,C错误。
4.(2023·浙江6月选考,12)苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下:
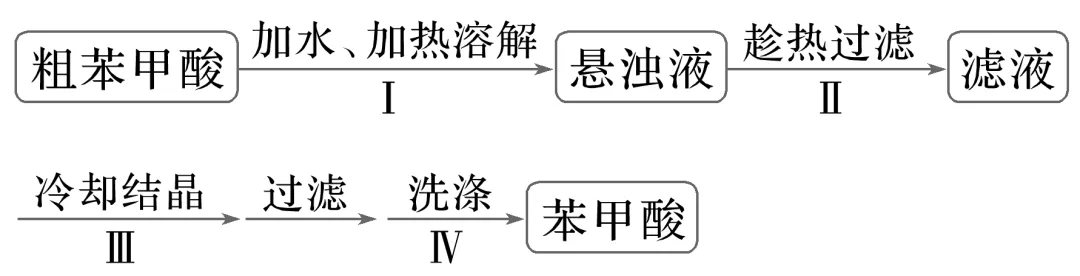
下列说法不正确的是( )
A.操作Ⅰ中依据苯甲酸的溶解度估算加水量
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.操作Ⅲ缓慢冷却结晶可减少杂质被包裹
D.操作Ⅳ可用冷水洗涤晶体
答案 B
解析操作Ⅰ中,为减少能耗、减少苯甲酸的溶解损失,溶解所用水的量需加以控制,可依据苯甲酸的溶解度估算加水量,A正确;操作Ⅱ趁热过滤的目的是除去泥沙,同时防止苯甲酸结晶析出,NaCl的溶解度
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享