
题型突破1 原子核外电子排布规范解答及原因解释
1.(2024·广东卷)酸在多种反应中具有广泛应用,其性能通常与酸的强度密切相关。
(1)酸催化下NaNO2与NH4Cl混合溶液的反应(反应a),可用于石油开采中油路解堵。
基态N原子价层电子的轨道表示式为。
答案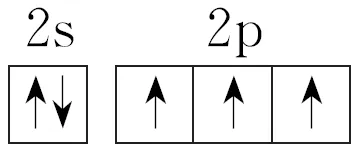
解析 N的原子序数为7,位于第二周期第ⅤA族,基态N原子价层电子的轨道表示式为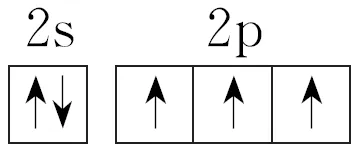 。
。
2.(2023·广东卷)配合物广泛存在于自然界,且在生产和生活中都发挥着重要作用。
基态Fe2+的3d电子轨道表示式为。
答案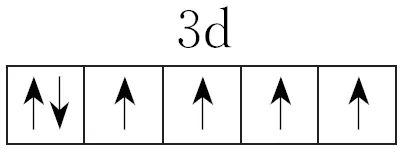
解析基态Fe2+的3d电子轨道表示式为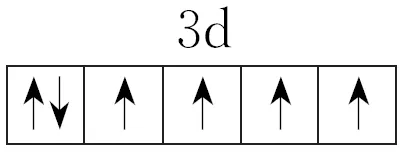 。
。
3.(2022·广东卷)Se与S同族,基态硒原子价电子排布式为。
答案 4s24p4
解析基态S价电子排布式为3s23p4,Se与S同族,Se为第四周期元素,因此基态Se价电子排布式为4s24p4。
4.(2021·广东卷)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。
基态硫原子价电子排布式为。
答案 3s23p4
解析硫为16号元素,基态硫原子的价电子排布式为3s23p4。
5.(2024·新课标卷)Ni基态原子价电子的轨道表示式为。
答案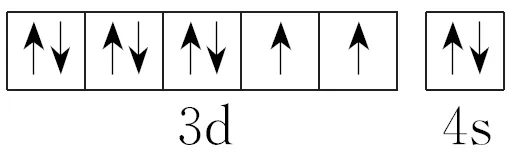
解析 Ni为28号元素,基态Ni原子的价电子排布式为3d84s2,价电子的轨道表示式为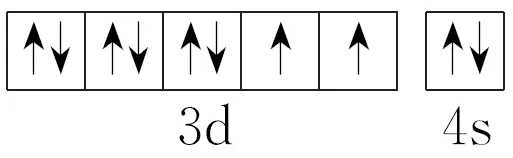 。
。
6.(2024·全国甲卷)ⅣA族元素具有丰富的化学性质,其化合物有着广泛的应用。回答下列问题:
该族元素基态原子核外未成对电子数为,在与其他元素形成化合物时,呈现的最高化合价为。
答案 2 +4
解析基态ⅣA族元素的价电子排布式为ns2np2,核外未成对电子数为2;在形成化合物时,呈现的最高化合价为+4。
7.(2024·浙江1月选考)氮和氧是构建化合物的常见元素。
请回答:
下列说法正确的是。
A.电负性:B>N>O
B.离子半径:P3- <S< span>2- <Cl< span>- </Cl<> </S<>
C.第一电离能:Ge <Se<As< span> </Se<As<>
D.基态Cr2+的简化电子排布式:[Ar]3d4
答案 CD
解析同一周期,从左到右,电负性依次增强,故顺序为O>N>B,A错误;核外电子排布相同,核电荷数越大,半径越小,故顺序为P3->S2->Cl-,B错误;同一周期,从左到右,电离能呈增大的趋势,第ⅤA族和第ⅥA族相反,故顺序为Ge <Se<As,C< span>正确;基态Cr的简化电子排布式:[Ar]3d54s1,Cr2+的简化电子排布式为[Ar]3d4,D正确。 </Se<As,C<>
考情分析:物质结构与性质广东高考采用“分散”命题方式,各小题之间相对独立,其中原子结构与性质是必考内容。
考查角度:微粒电子排布式、电子排布图、价电子排布、电子数判断等。
1.原子核外电子排布的“三”规律
能量最 低原理 | 原子核外电子总是先占据能量最低的原子轨道 |
泡利原理 | 每个原子轨道上最多只能容纳2个自旋状态相反的电子 |
洪特规则 | 当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,而且自旋状态相同 |
2.特殊基态原子的价电子排布
(1)7个主族和0族元素价电子排布
| 价电子排布式 |
ⅠA | ns1 |
ⅡA | ns2 |
ⅢA | ns2np1 |
ⅣA | ns2np2 |
ⅤA | ns2np3 |
ⅥA | ns2np4 |
ⅦA | ns2np5 |
0 | ns2np6 |
(2)第四周期副族和第Ⅷ族元素价电子排布
族 | 元素名称 | 元素符号 | 价电子排布式 |
ⅢB | 钪 | 21Sc | 3d14s2 |
ⅣB | 钛 | 22Ti | 3d24s2 |
ⅤB | 钒 | 23V | 3d34s2 |
ⅥB | 铬 | 24Cr | 3d54s1 |
ⅦB | 锰 | 25Mn | 3d54s2 |
ⅧB | 铁 | 26Fe | 3d64s2 |
钴 | 27Co | 3d74s2 |
镍 | 28Ni | 3d84s2 |
ⅠB | 铜 | 29Cu | 3d104s1 |
ⅡB | 锌 | 30Zn | 3d104s2 |
3.Cr、Cu原子的核外电子排布式
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享