
微点突破1 溶液中三大平衡的分析及应用

1.三大平衡的比较
平衡类型 | 电离平衡CH3COOHCH3COO-+H+ | 水解平衡CH3COO-+H2OCH3COOH+OH- | 沉淀溶解平衡AgCl(s)Ag+(aq)+Cl-(aq) |
研究对象 | 弱电解质溶液 | 能水解的盐溶液 | 难溶电解质 |
影 响 因 素 | 升温 | 促进电离 | Ka增大 | 促进水解 | Kh增大 | 若难溶物的溶解度与温度成正比,促进溶解;反之,则抑制溶解 | 若难溶物的溶解度与温度成正比,Ksp增大;反之,则Ksp减小 |
加水 | 促进电离 | Ka不变 | 促进水解 | Kh不变 | 促进溶解 | Ksp不变 |
加入相 应离子 (或物质) | 加入CH3COONa或HCl,抑制电离 | Ka不变 | 加入CH3COOH或NaOH,抑制水解 | Kh不变 | 加入AgNO3或NaCl,抑制溶解 | Ksp不变 |
加入反应 离子(或 物质) | 加入OH-,促进电离 | Ka不变 | 加入H+,促进水解 | Kh不变 | 加入氨水,促进溶解 | Ksp不变 |
 应试技巧
应试技巧
①盐的电离是完全的,电离方程式用===表示,溶质大量存在;盐的弱离子的水解、弱酸弱碱的电离,均为可逆过程,用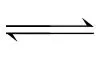 表示。
表示。
②盐的水溶液加水稀释,平衡向粒子数目增大的方向移动,pH向7靠拢。例如稀释CCl3COONa溶液,CCl3COO-+H2OCCl3COOH+OH-,稀释时,不是所有离子浓度都减小,c(H+)增大。
③升温,促进电离和水解,但pH变化取决于原溶液酸碱性。
2.三大守恒式的书写
(1)电荷守恒
①含义:阳离子所带的正电荷总数与阴离子所带的负电荷总数相等。
②系数:电荷数。
③特点:只有离子,没有分子。
④判断:先看系数是否正确,再看离子是否齐全。
如Na2S与NaHS的混合溶液中存在电荷守恒:。
答案c(Na+)+c(H+)=2c(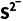 )+c(HS-)+c(OH-)
)+c(HS-)+c(OH-)
(2)元素守恒
①含义:原始物质中某些微粒间存在特定的比例关系;溶液中所有含某元素或原子团的微粒的浓度之和等于某一特定的数值。
②系数:按照比例确定。
③特点:一定没有H+和OH-,与比例有关,与是否反应无关。
④判断:先看比例是否正确,再看微粒是否齐全。
a.0.1 mol·L-1 Na2CO3溶液中存在的元素守恒:。
答案c(Na+)=2c(HC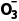 )+2c(C
)+2c(C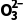 )+2c(H2CO3)=0.2 mol·L-1
)+2c(H2CO3)=0.2 mol·L-1
b.物质的量浓度1∶1的HA、NaA的混合溶液中存在元素守恒:。
答案 2c(Na+)=c(A-)+c(HA)
(3)质子守恒
①含义:失质子总数=游离质子数+得质子总数。
②系数:变化量。
③特点:一定有H+和OH-,还有分子。
如Na2CO3溶液的质子守恒:。
答案c(OH-)=c(H+)+c(HC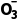 )+2c(H2CO3)
)+2c(H2CO3)
解析方法一:由电荷守恒式和元素守恒式联立消去阳离子(Na+)得到。
方法二:框图法快速求Na2CO3溶液的质子守恒。

[真题精练]
1.(2021·广东,8)鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用GHCl表示)。已知GHCl水溶液呈酸性,下列叙述正确的是( )
A.0.001 mol·L-1 GHCl水溶液的pH=3
B.0.001 mol·L-1 GHCl水溶液加水稀释,pH升高
C.GHCl在水中的电离方程式为GHCl===G+HCl
D.GHCl水溶液中:c(OH-)+c(Cl-)=c(GH+)+ c(G)
答案 B
解析 GHCl为强酸弱碱盐,电离出的GH+会发生水解,但水解较为微弱,因此0.001mol·L-1GHCl水溶液的pH>3,故A错误;稀释GHCl溶液时,GH+的水解程度将增大,根据勒夏特列原理可知,溶液中c(H+)将减小,溶液pH将升高,故B正确;GHCl为强酸弱碱盐,在水中的电离方程式为GHCl===GH++Cl-,故C错误;根据电荷守恒可知,GHCl水溶液中c(OH-)+c(Cl-)=c(H+)+c(GH+),故D错误。
2.(2025·广东,12)CuCl微溶于水,但在Cl-浓度较高的溶液中因形成[CuCl2]-和[CuCl3]2-而溶解。将适量CuCl完全溶于盐酸,得到含[CuCl2]-和[CuCl3]2-的溶液,下列叙述正确的是( )
A.加水稀释,[CuCl3]2-浓度一定下降
B.向溶液中加入少量NaCl固体,[CuCl2]-浓度一定上升
C.H[CuCl2]的电离方程式为H[CuCl2]===H++Cu2++2Cl-
D.体系中,c(Cu+)+c(H+)=c(Cl-)+c([CuCl2]-)+c([CuCl3]2-)+c(OH-)
答案 A
解析加水稀释,体积影响程度较大,溶液中[CuCl3]2-的浓度一定下降,A正确;向溶液中加入少量NaCl固体,CuCl+Cl-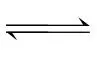 [CuCl2]-、[CuCl2]-+Cl-
[CuCl2]-、[CuCl2]-+Cl-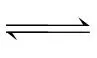 [CuCl3]2-平衡均正向移动,[CuCl2]-的浓度不一定上升,B错误;[CuCl2]-不能拆分,H[CuCl2]应电离为H+和[CuCl2]-,C错误;体系中存在电荷守恒:c(Cu+)+c(H+)=c(Cl-)+c(OH-)+c([CuCl2]-)+2c([CuCl3]2-),D错误。
[CuCl3]2-平衡均正向移动,[CuCl2]-的浓度不一定上升,B错误;[CuCl2]-不能拆分,H[CuCl2]应电离为H+和[CuCl2]-,C错误;体系中存在电荷守恒:c(Cu+)+c(H+)=c(Cl-)+c(OH-)+c([CuCl2]-)+2c([CuCl3]2-),D错误。
[模拟预测]
3.(2025·广州一模)C6H5NH2是一种有机弱碱,可与盐酸反应生成盐酸盐C6H5NH3Cl,下列叙述正确的是( )
A.常温下,0.001 mol·L-1 C6H5NH2水溶液的pH=11
B.0.001 mol·L-1 C6H5NH3Cl水溶液加水稀释,pH升高
C.C6H5NH3Cl水溶液的电离方程式为C6H5NH3Cl===C6H5NH2+HCl
D.C6H5NH3Cl水溶液中:c(OH-)+c(Cl-)=c(C6H5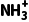 )+c(C6H5NH2)
)+c(C6H5NH2)
答案 B
解析苯胺(C6H5NH2)是一种有机弱碱,其水溶液的碱性较弱,0.001mol·L-1的C6H5NH2水溶液的pH应小于11,A错误;0.001mol·L-1的C6H5NH3Cl水溶液加水稀释,由于其为强酸弱碱盐,水解显酸性,稀释后酸性减弱,溶液中H+浓度减小,pH升高,B正确;C6H5NH3Cl是盐酸盐,为强电解质,电离产生Cl-,故
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享