
微点突破1 焓变计算和热化学方程式书写

1.焓变计算

2.利用盖斯定律计算焓变思维模型
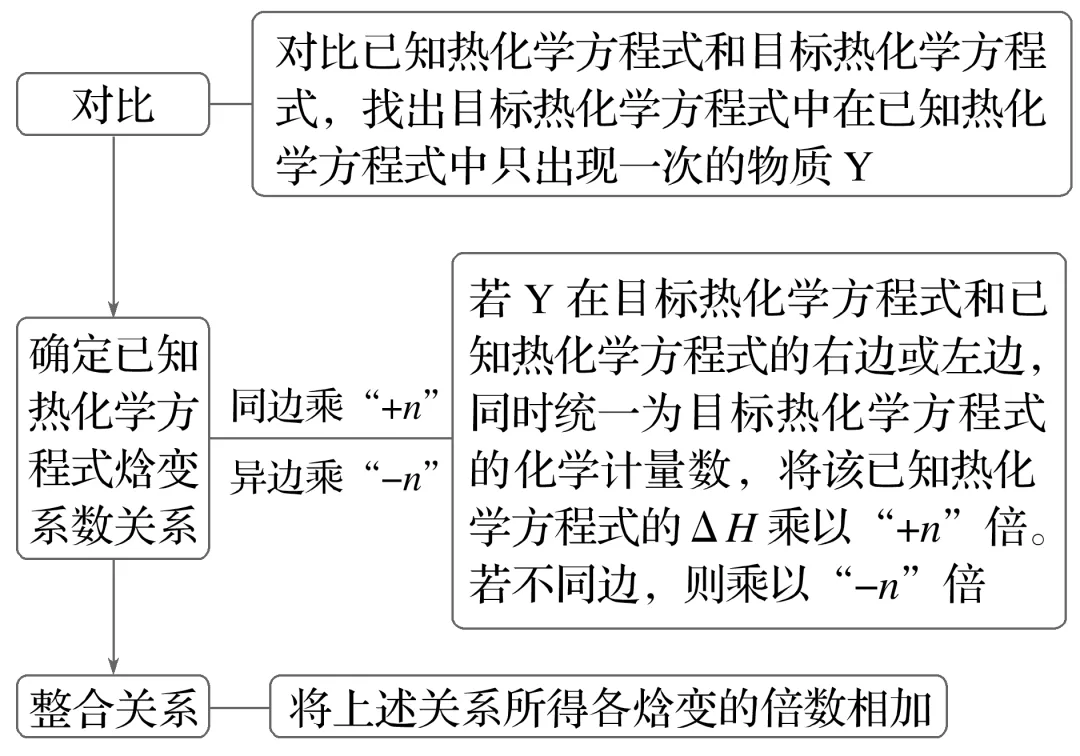
3.书写热化学方程式的“五环节”


1.[2025·云南,17(2)①]我国科学家研发出一种乙醇(沸点78.5 ℃)绿色制氢新途径,并实现高附加值乙酸(沸点118 ℃)的生产,主要反应为:
Ⅰ.C2H5OH(g)+H2O(g)===2H2(g)+CH3COOH(g) ΔH1Kp1
Ⅱ.C2H5OH(g)===CH3CHO(g)+H2(g) ΔH2=+68.7 kJ·mol-1
对于反应Ⅰ:
已知CH3CHO(g)+H2O(g)===H2(g)+CH3COOH(g) ΔH=-24.3 kJ·mol-1则ΔH1= kJ·mol-1。
答案 +44.4
2.[2025·湖北,19(1)]CaH2(s)粉末可在较低温度下还原Fe2O3(s)。回答下列问题:
已知一定温度下:
CaH2(s)+6Fe2O3(s)===Ca(OH)2(s)+4Fe3O4(s) ΔH1=m kJ·mol-1
2CaH2(s)+Fe3O4(s)===2Ca(OH)2(s)+3Fe(s) ΔH2=n kJ·mol-1
则3CaH2(s)+2Fe2O3(s)===3Ca(OH)2(s)+4Fe(s)的ΔH3=kJ·mol-1(用m和n表示)。
答案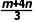
3.[2024·河北,17(1)①]硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:SO2(g)+Cl2(g)SO2Cl2(g) ΔH=-67.59 kJ·mol-1。
若正反应的活化能为E正 kJ·mol-1,则逆反应的活化能E逆= kJ·mol-1(用含E正的代数式表示)。
答案E正+67.59
解析根据反应热与活化能E正和E逆关系:ΔH=E正-E逆 可知,该反应的E逆=[E正-(-67.59)]kJ·mol-1=(E正+67.59) kJ·mol-1。
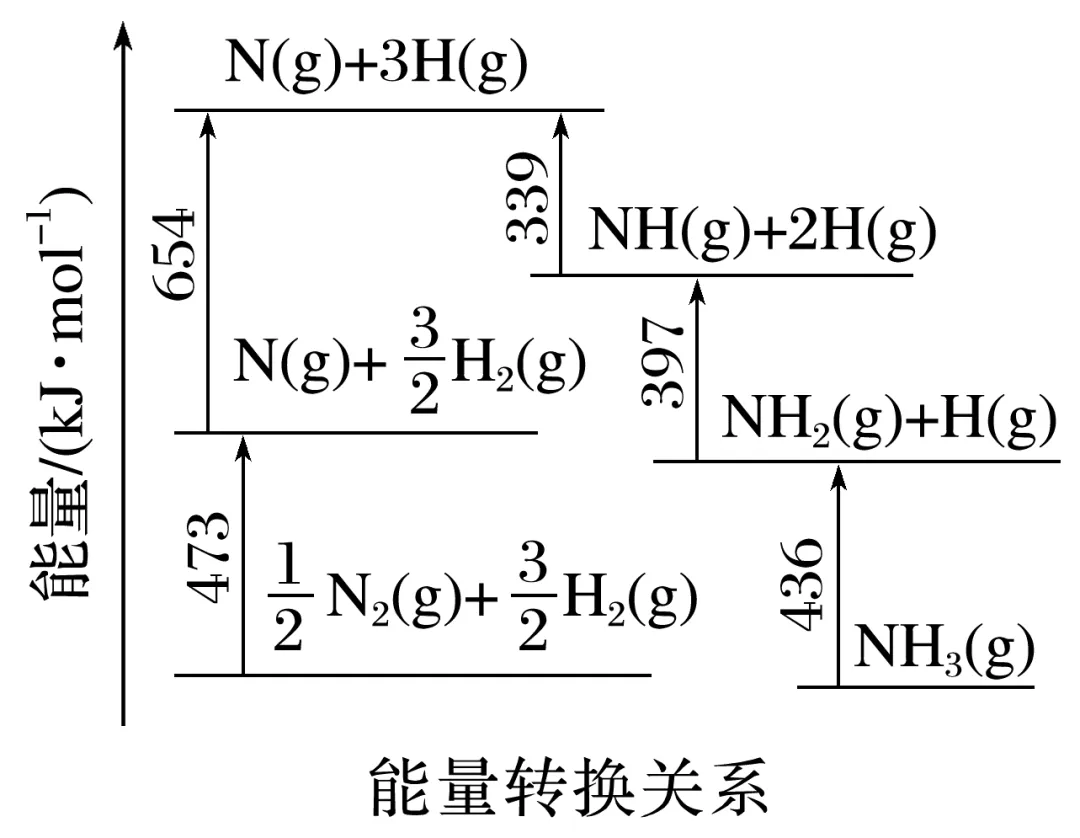
4.[2023·新课标卷,29(1)]根据图示数据计算反应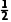 N2(g)+H2(g)===NH3(g)的ΔH=kJ·mol-1。
N2(g)+H2(g)===NH3(g)的ΔH=kJ·mol-1。
答案 -45
解析在化学反应中,断开化学键要吸收能量,形成化学键要释放能量,反应的焓变等于反应物的键能总和与生成物的键能总和的差,因此,由图中数据可知,反应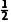 N2(g)+
N2(g)+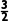 H2(g)===NH3(g)的ΔH=(473+654-436-397-339) kJ·mol-1=-45kJ·mol-1。
H2(g)===NH3(g)的ΔH=(473+654-436-397-339) kJ·mol-1=-45kJ·mol-1。
5.[2023·河北,17(1)]已知:1 mol物质中的化学键断裂时所需能量如下表。
物质 | N2(g) | O2(g) | NO(g) |
能量/kJ | 945 | 498 | 631 |
恒温下,将1 mol空气(N2和O2的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容密闭容器中,假设体系中只存在如下两个反应:
ⅰ.N2(g)+O2(g)2NO(g) K1 ΔH1
ⅱ.2NO(g)+O2(g)2NO2(g) K2 ΔH2=-114 kJ·mol-1
ΔH1=kJ·mol-1。
答案 +181
解析 ΔH1=反应物总键能-生成物总键能=(945kJ·mol-1+498kJ·mol-1)-2×631kJ·mol-1=+181kJ·mol-1。
6.[2025·北京,18(1)]已知:
H2S(g)+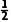 O2(g)===S(s)+H2O(g) ΔH=-221.2 kJ·mol-1
O2(g)===S(s)+H2O(g) ΔH=-221.2 kJ·mol-1
S(s)+O2(g)===SO2(g) ΔH=-296.8 kJ·mol-1
由H2S制SO2的热化学方程式为。
答案 H2S(g)+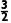 O2(g)===SO2(g)+H2O(g) ΔH=-518 kJ·mol-1
O2(g)===SO2(g)+H2O(g) ΔH=-518 kJ·mol-1
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享