
1.交换膜类型及特点
交换膜类型 | 阳膜 | 阴膜 | 双极膜 | 特定的交换膜 |
允许通过的离子及移动方向 | 阳离子移向原电池的正极(电解池的阴极) | 阴离子移向原电池的负极(电解池的阳极) | 中间层中的H2O解离出H+和OH-,H+移向原电池的正极(电解池的阴极),OH-移向原电池的负极(电解池的阳极) | 只允许特定的离子或分子通过,如质子交换膜只允许H+通过,氯离子交换膜只允许Cl-通过 |
通性 | 无论是原电池还是电解池中,阳离子均移向得电子的一极,阴离子均移向失电子的一极 |
2.离子交换膜的作用
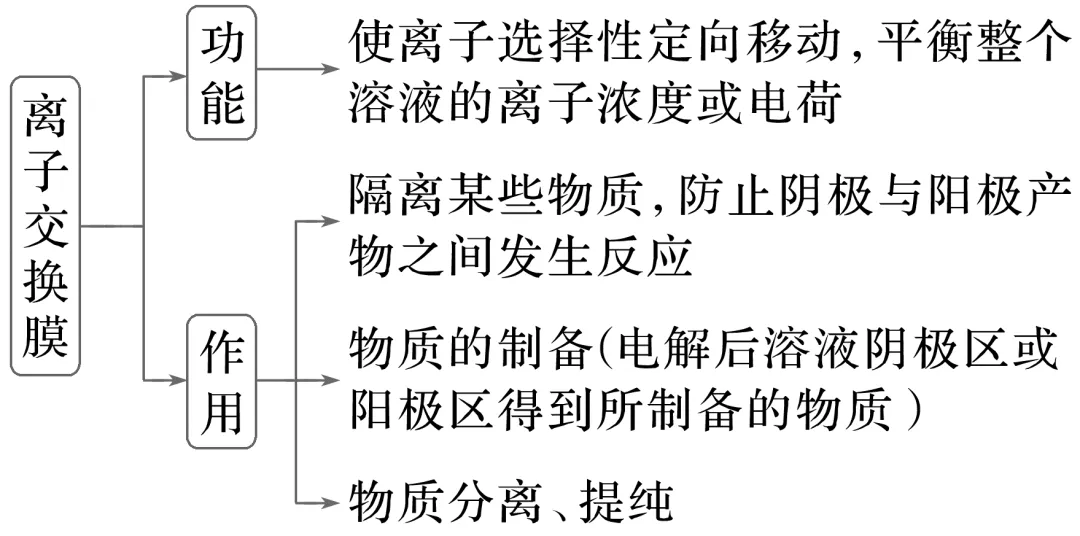
3.离子交换膜的判断
判断方法 | 首先判断隔膜的用途是制取物质还是避免电极产物之间发生反应,然后根据电解质溶液呈电中性的原则判断膜的类型。方法如下:先明确电极产物,写出阴、阳两极上的电极反应式;再依据电极反应式判断该电极附近哪种离子有剩余,结合溶液呈电中性的原则,判断离子移动的方向,确定离子交换膜的类型 |
锌碘单液流电池,其原理如图所示 | 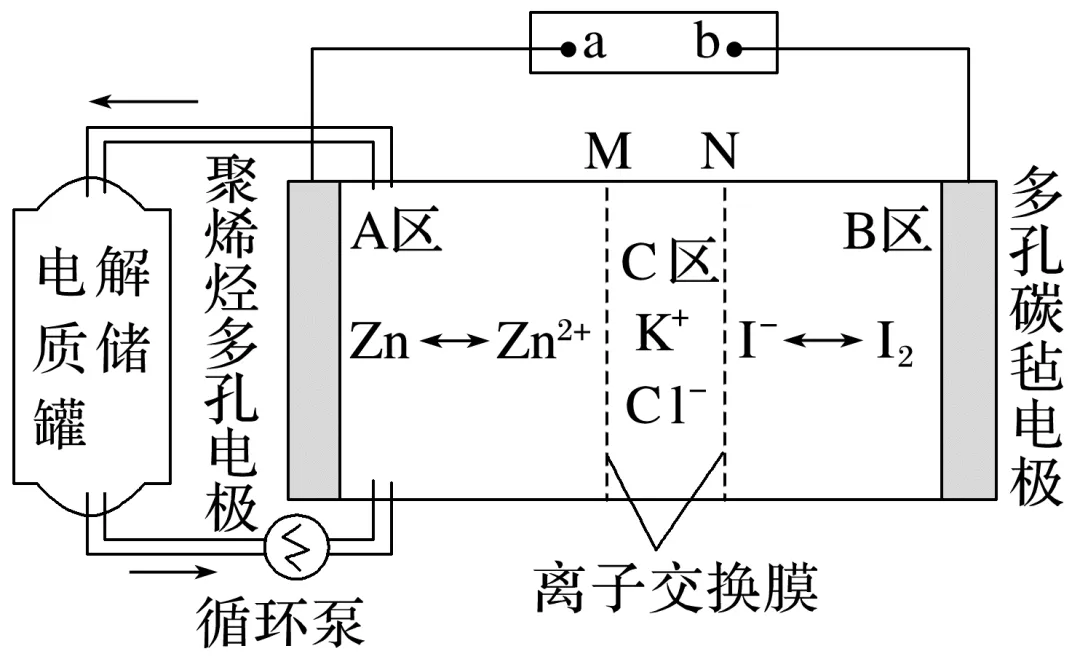
|
分析 | 负极:Zn-2e-===Zn2+,阳离子浓度增大,为平衡电荷,Cl-移向A区,M为阴离子交换膜; 正极:I2+2e-===2I-,阴离子浓度增大,为平衡电荷,K+移向B区,N为阳离子交换膜 |
4.多膜电解池方程式的书写及分析
(1)双膜三室处理吸收液(吸收了烟气中的SO2)(或污水)
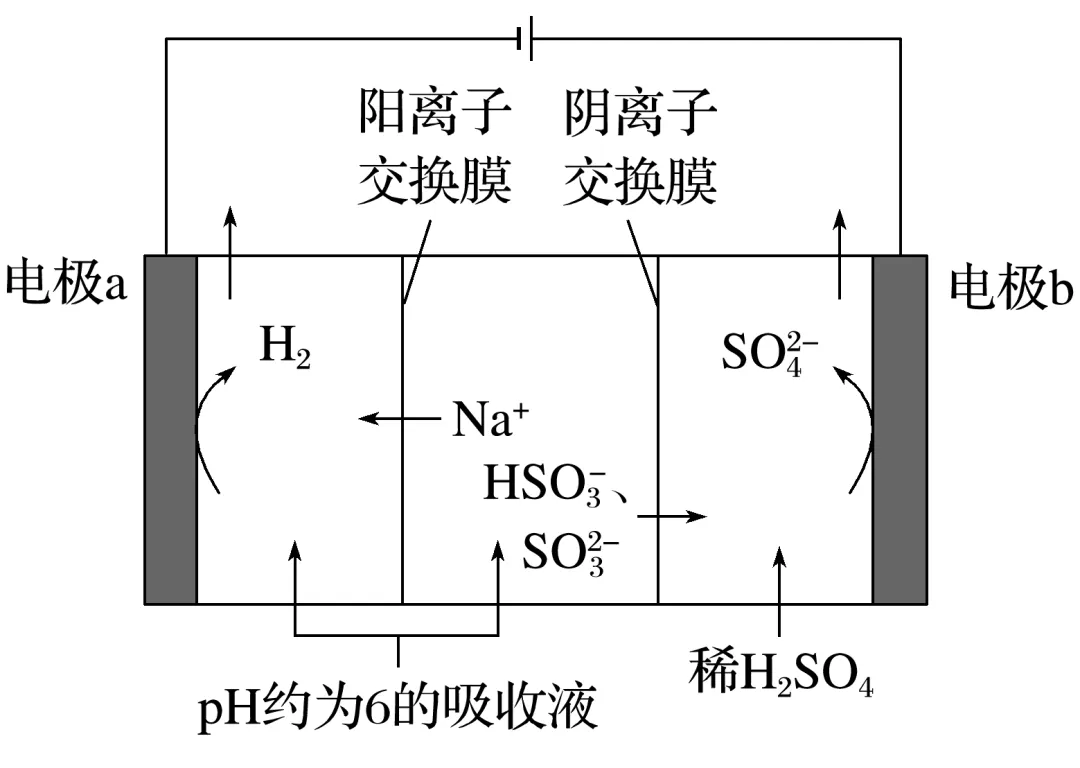
阳极室 | HS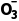 -2e-+H2O===S -2e-+H2O===S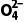 +3H+或S +3H+或S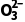 -2e-+H2O===S -2e-+H2O===S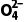 +2H+ +2H+ |
吸收液(或污水) | Na+穿过阳离子交换膜进入阴极室(左室);HS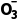 和S 和S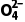 穿过阴离子交换膜进入阴极室(右室) 穿过阴离子交换膜进入阴极室(右室) |
阴极室 | 2H2O+4e-===2OH-+H2↑、HS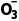 +OH-===S +OH-===S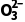 +H2O +H2O |
产品 | 阳极室:较浓的硫酸;阴极室:亚硫酸钠 |
(2)三膜四室制备硼酸[H3BO3(一元弱酸)]
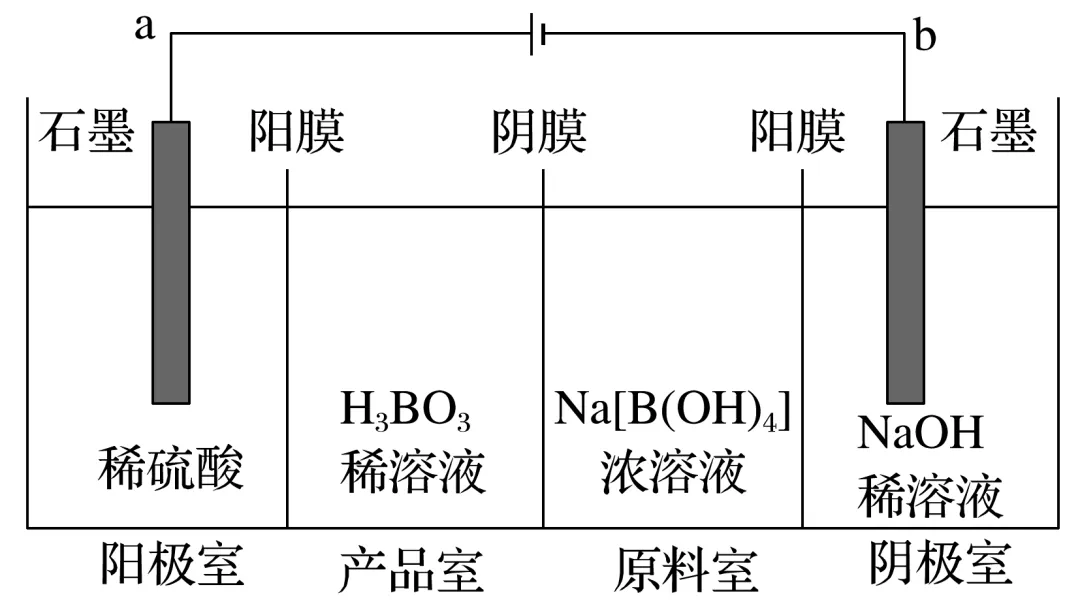
阳极室 | 2H2O-4e-===O2↑+4H+ |
阴极室 | 2H2O+2e-===H2↑+2OH- |
原料室 | [B(OH)4]-穿过阴膜进入产品室,Na+穿过阳膜进入阴极室 |
产品室 | H++[B(OH)4]-===H3BO3+H2O |
5.解答含膜电池题的思维模板
(1)第一步:判断装置类型。根据有无外加电源,判断是电解池还是原电池。
(2)第二步:分清隔膜类型。即交换膜属于阳膜、阴膜或质子膜中的哪一种,判断隔膜允许哪种离子通过。
(3)第三步:分析隔膜作用。根据题给信息分析隔膜的作用是平衡电荷,还是让离子选择性通过避免副反应,或为了生成特定物质。
(4)第四步:写出电极反应式。根据电极类型、交换膜两侧离子变化、电荷变化或离子迁移方向等综合信息书写电极反应式,最后做出综合推断或计算。

1.次磷酸钴[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图:
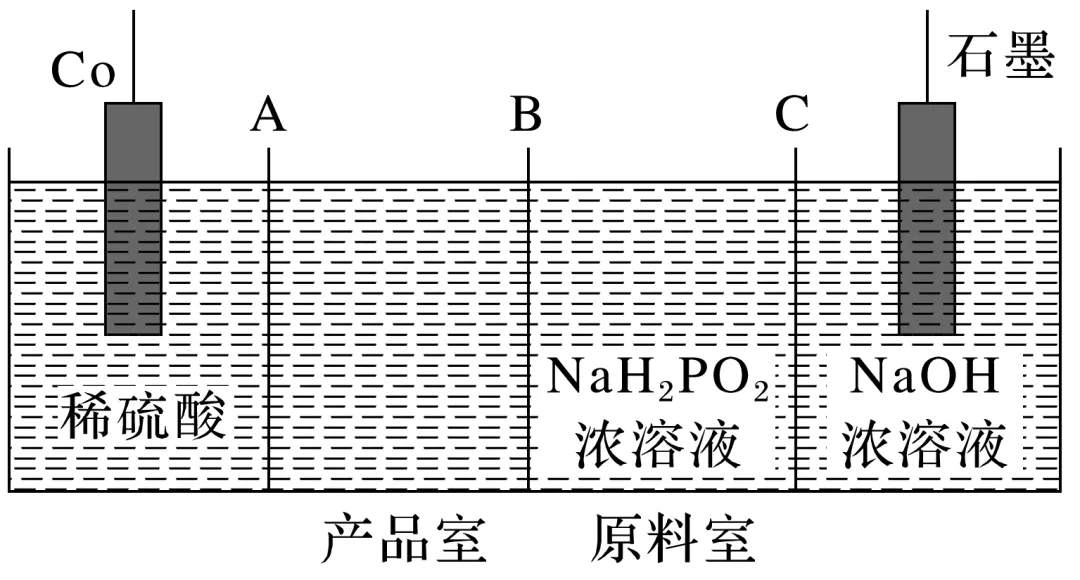
(1)A是阳离子交换膜,判断方法:根据产物Co(H2PO2)2确定离子移动方向;Co2+向产品室移动,则A是阳离子交换膜。
(2)B是阴离子交换膜,判断方法:H2P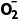 向产品室移动。
向产品室移动。
(3)Co为阳极,阳极反应式为Co-2e-===Co2+。
(4)石墨为阴极,阴极反应式为2H2O+2e-===H2↑+2OH-,C是阳离子交换膜。
2.(2025·湖南,9)一种电化学处理硝酸盐产氨的工作原理如图所示。下列说法错误的是( )
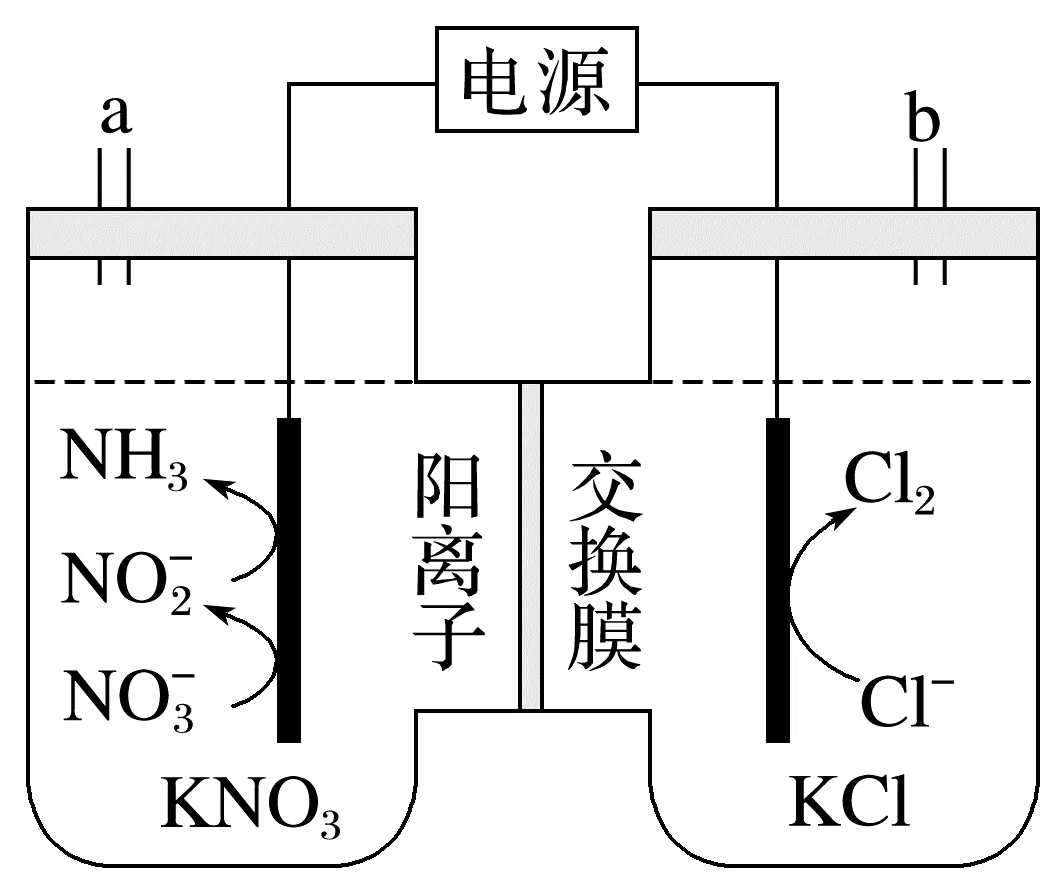
A.电解过程中,K+向左室迁移
B.电解过程中,左室中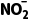 的浓度持续下降
的浓度持续下降
C.用湿润的蓝色石蕊试纸置于b处,试纸先变红后褪色
D.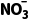 完全转化为NH3的电解总反应:
完全转化为NH3的电解总反应: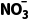 +8Cl-+6H2ONH3↑+9OH-+4Cl2↑
+8Cl-+6H2ONH3↑+9OH-+4Cl2↑
答案 B
解析电解池中,阳离子向阴极移动,则K+向左室迁移,A正确;电解过程中,N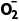 先生成,再消耗,是中间产物,其浓度增大还是减小,取决于其生成速率与消耗速率,无法得出其浓度持续下降的结论,B错误;b处生成氯气,与水反应生成盐酸和次氯酸,盐酸能使蓝色石蕊试纸变红,次氯酸能使变红的试纸褪
先生成,再消耗,是中间产物,其浓度增大还是减小,取决于其生成速率与消耗速率,无法得出其浓度持续下降的结论,B错误;b处生成氯气,与水反应生成盐酸和次氯酸,盐酸能使蓝色石蕊试纸变红,次氯酸能使变红的试纸褪
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享