
1.分析电化学装置的物质变化,书写电极反应式
(1)确定装置类型
原电池:外接用电器、电流表、负载等;
电解池:外接电源或题干给出信息;
二次电池:放电为原电池、充电为电解池。
(2)“四步法”书写电极反应式
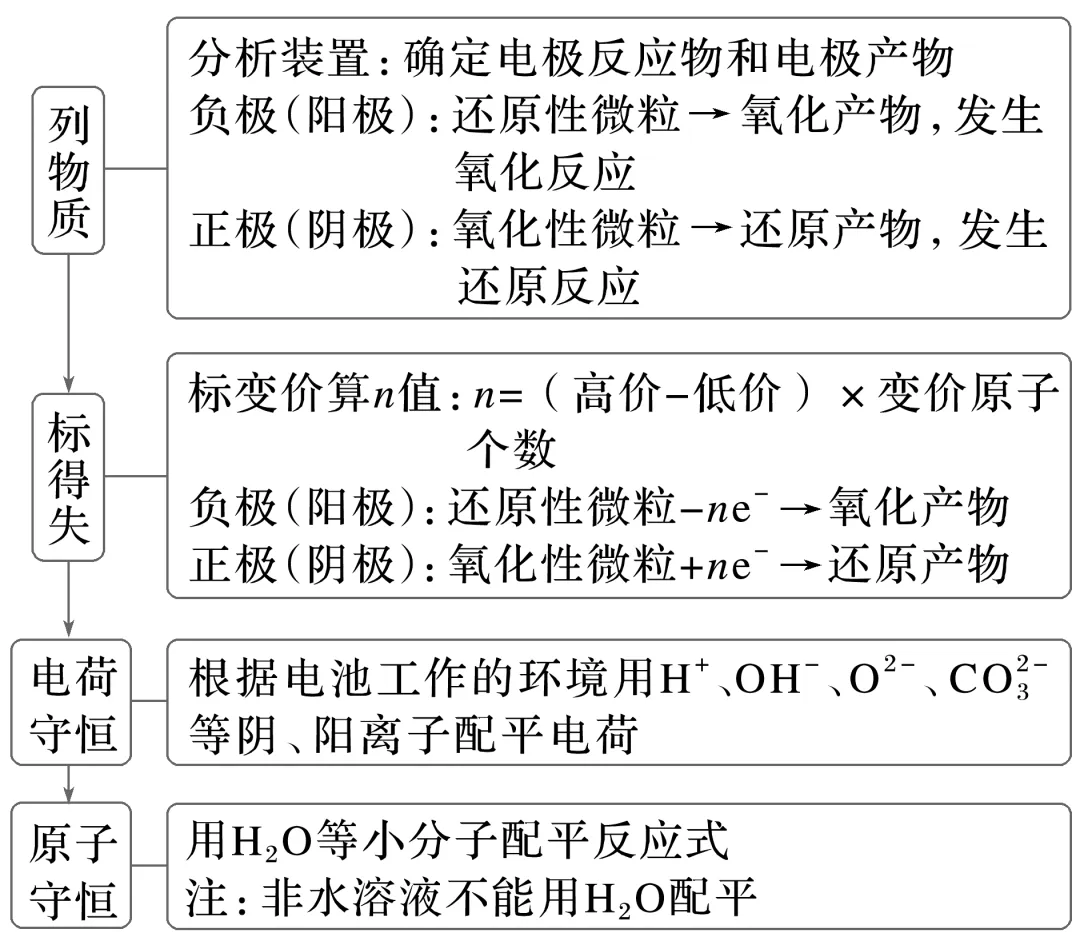
2.已知总反应式,书写电极反应式
(1)书写三步骤
步骤一:根据电池总反应式,标出电子转移的方向和数目(ne-)。
步骤二:找出正(阴)、负(阳)极,失电子的电极为负(阳)极;确定溶液的酸碱性。
步骤三:写电极反应式。
负(阳)极反应:还原剂-ne-===氧化产物
正(阴)极反应:氧化剂+ne-===还原产物
(2)书写技巧
若某电极反应式较难写出时,可先写出较易的电极反应式,然后根据得失电子守恒,用总反应式减去较易的电极反应式,即可得出较难写出的电极反应式。
3.守恒法在电化学计算中的应用
(1)电子守恒和电荷守恒列关系式
①电子守恒:两极得失电子数相等。
②电荷守恒:1个电子对应1个正电荷(或负电荷)。
③常用关系式:O2~4e-~4Ag~2Cu~2H2~2Cl2~4OH-~4H+~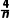 Mn+。
Mn+。
(2)几个注意问题
①涉及气体体积相关计算时,必须注明标准状况。
②计算含交换膜电化学装置中某一区域的质量变化时,注意离子的迁移。

1.[2024·浙江1月选考,19(1)]某研究小组采用电化学方法将CO2转化为HCOOH,装置如图。电极B上的电极反应式是。
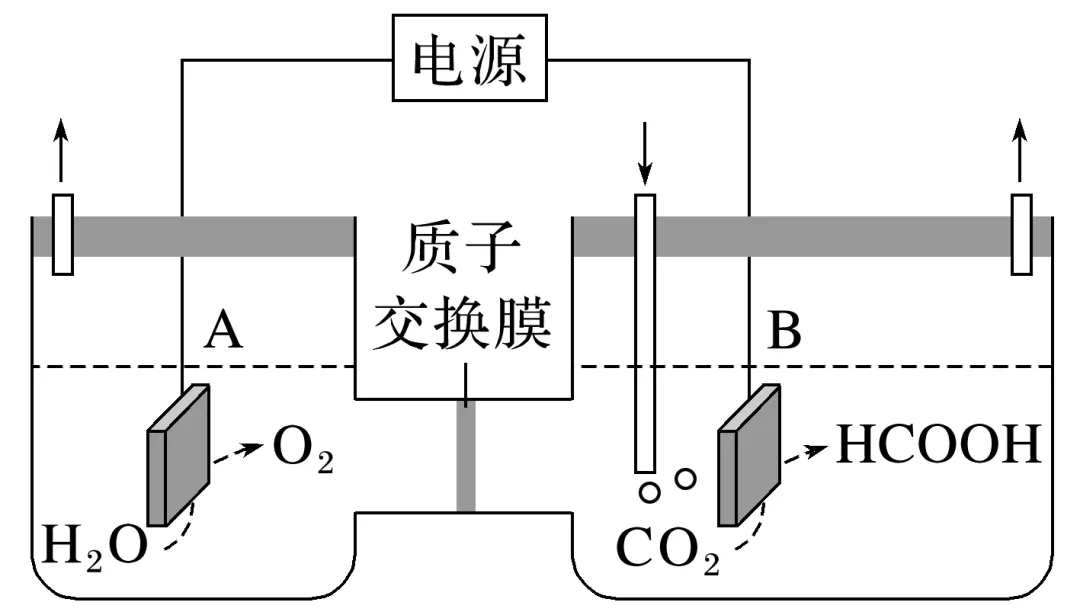
答案 CO2+2e-+2H+===HCOOH
解析电极B是阴极,则电极反应式是CO2+2e-+2H+===HCOOH。
2.[2023·北京,16(3)]近年研究发现,电催化CO2和含氮物质(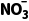 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示:
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示:
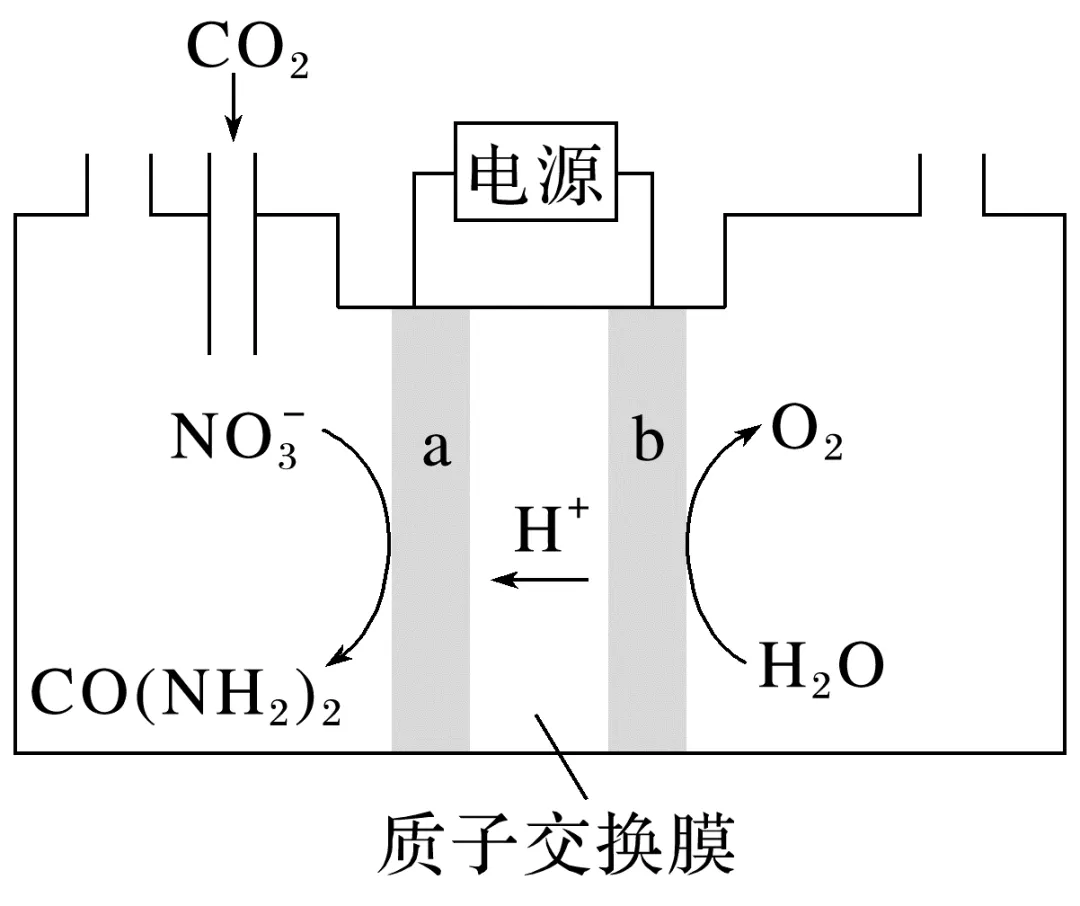
①电极b是电解池的极。
②电解过程中生成尿素的电极反应式是。
答案①阳 ②2N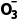 +16e-+CO2+18H+===CO(NH2)2+7H2O
+16e-+CO2+18H+===CO(NH2)2+7H2O
解析①电极b上发生H2O失电子生成O2的氧化反应,是电解池的阳极。②a极硝酸根离子得电子转化为尿素,再结合酸性环境可分析出电极反应式。
3.[2023·湖南,17(2)]工业上以粗镓为原料,制备超纯Ga(CH3)3的工艺流程如下:
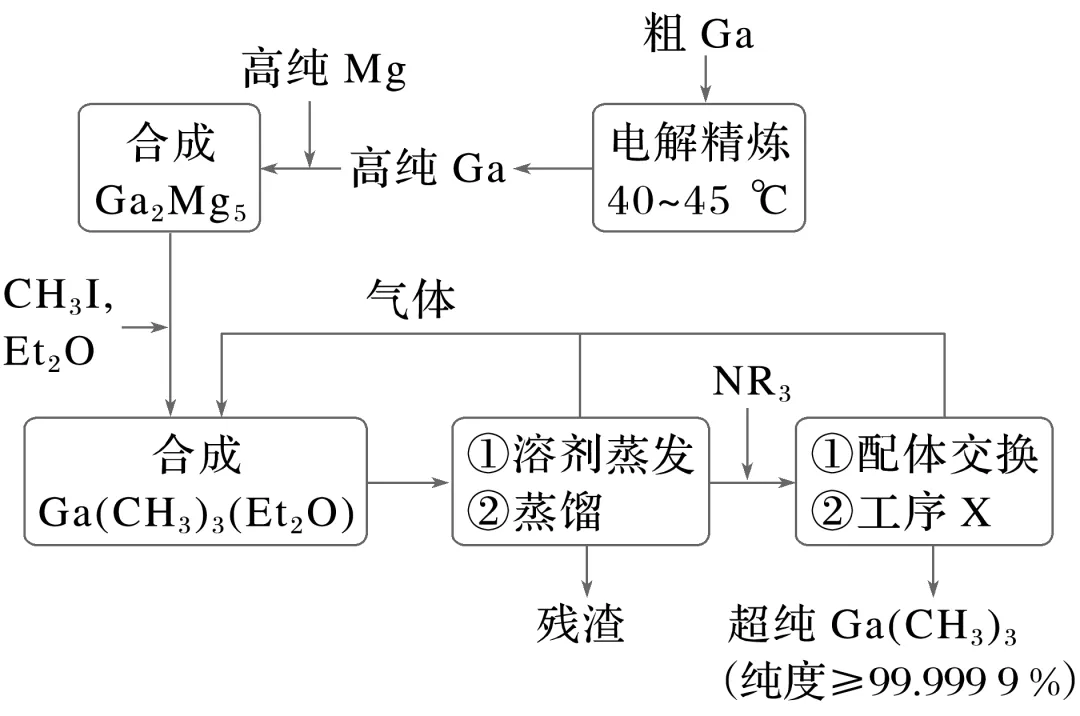
已知:金属Ga的化学性质和Al相似,Ga的熔点为29.8 ℃。
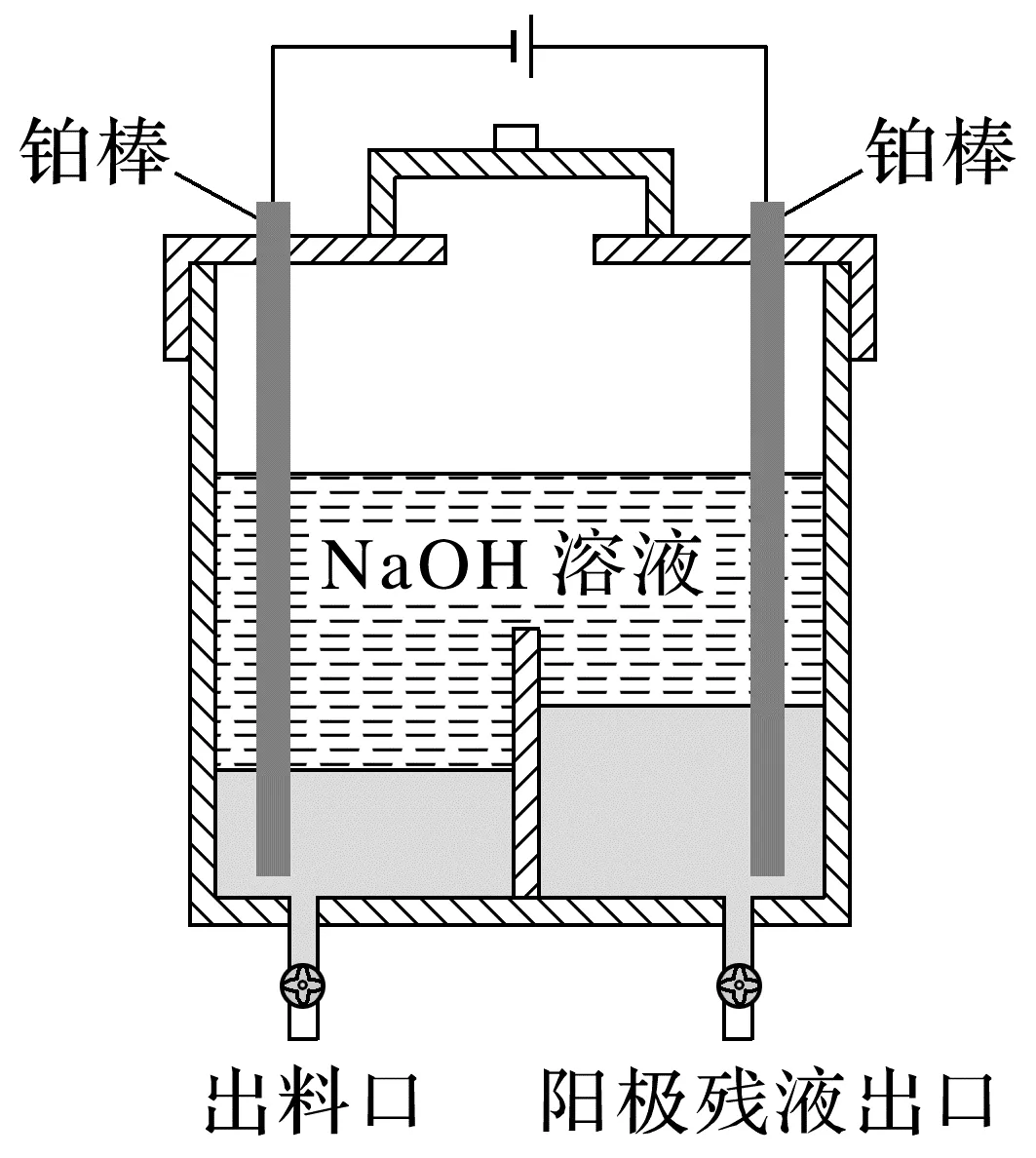
“电解精炼”装置如图所示,电解池温度控制在40~45 ℃的原因是, 阴极的电极反应式为。
答案 确保生成的Ga为液体,便于从出料口流出 [Ga(OH)4]-+3e-===Ga+4OH-
解析镓的熔点为29.8℃,电解精炼温度需高于镓的熔点,因此电解池温度控制在40~45℃。Ga和Al性质相似,电解精炼过程中粗镓在阳极失电子产生的Ga3+在NaOH溶液中形成[Ga(OH)4]-,[Ga(OH)4]-在阴极得电子被还原为Ga,故阴极反应为[Ga(OH)4]-+3e-===Ga+4OH-。
4.[2024·北京,16(3)]研究表明可以用电解法以N2为氮源直接制备HNO3,其原理示意图如下。
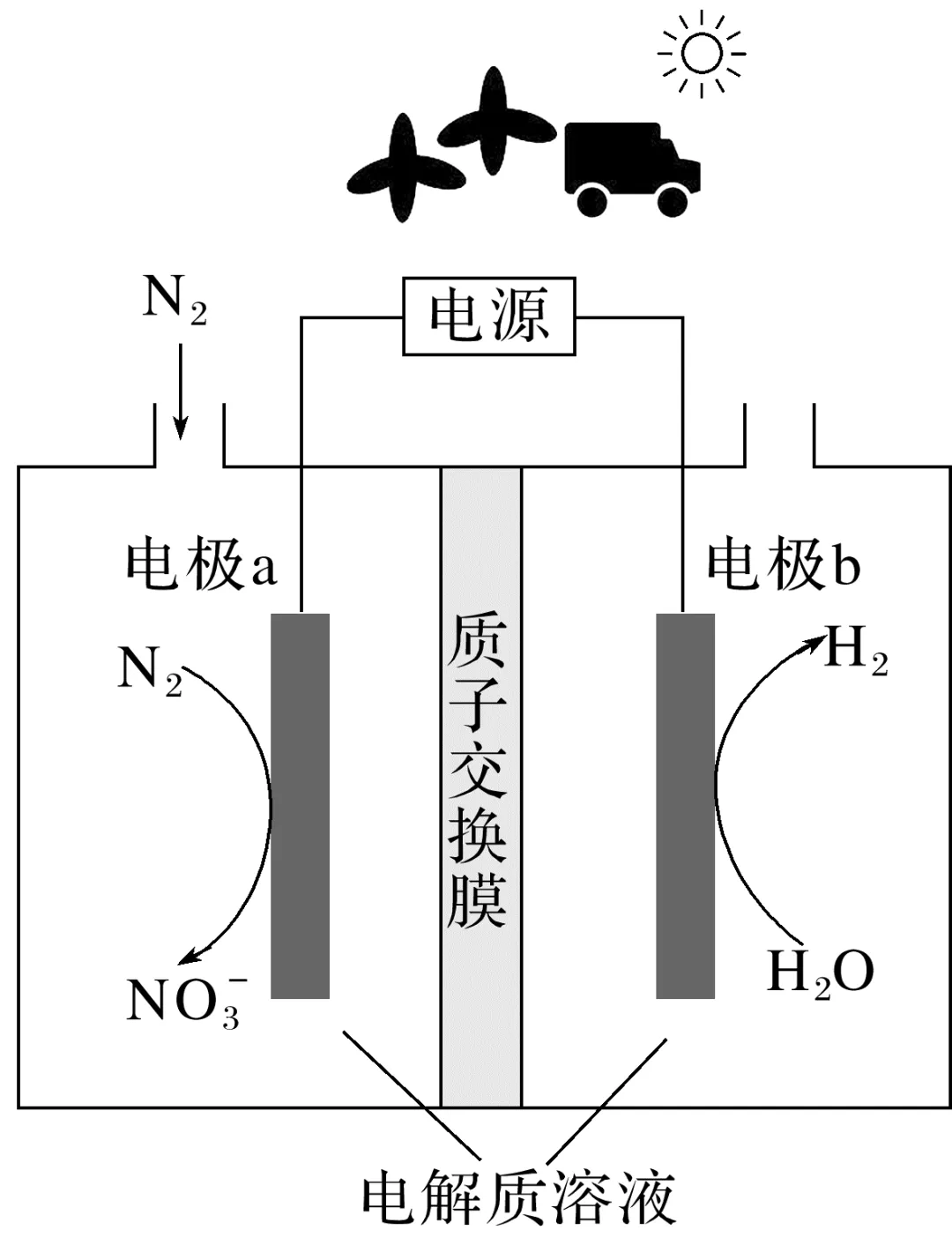
①电极a表面生成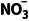 的电极反应式:。
的电极反应式:。
②研究发现:N2转化可能的途径为N2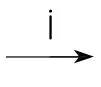
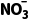 。电极a表面还发生ⅲ.H2O→O2。ⅲ的存在,有利于途径ⅱ,原因是。
。电极a表面还发生ⅲ.H2O→O2。ⅲ的存在,有利于途径ⅱ,原因是。
答案①N2+6H2O-10e-===2N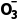 +12H+②反应ⅲ生成O2,O2将NO氧化成NO2,NO2更易转化成
+12H+②反应ⅲ生成O2,O2将NO氧化成NO2,NO2更易转化成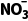
解析①电极a上N2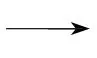
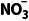 ,氮元素化合价升高,发生氧化反应,电极a为阳极,电极反应式为N2+6H2O-10e-===2N
,氮元素化合价升高,发生氧化反应,电极a为阳极,电极反应式为N2+6H2O-10e-===2N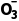 +12H+。
+12H+。
5.[2024·浙江6月选考,19(4)]氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如图所示,正极上的电极反应式是。
该电池以3.2 A恒定电流工作14分钟,消耗H2体积为0.49 L,故可测得该电池将化学能转化为电能的转化率为。[已知:该条件下H2的摩尔体积为24.5 L·mol-1;电荷量q(C)=电流I(A)×时间(s);NA=6.0×1023 mol-1;e=1.60×10-19C。] 
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享