
微点突破1 原电池工作原理及燃料电池
1.原电池的工作原理
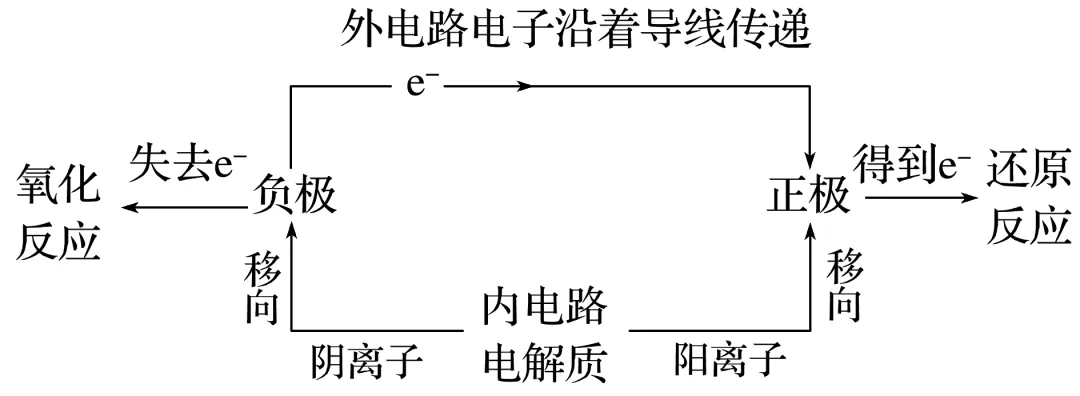
2.燃料电池
以CH3OH燃料电池为例,体会不同介质对电极反应的影响。
电池类型 | 导电介质 | 反应式 |
酸性燃料电池 | H+ | 总反应:2CH3OH+3O2===2CO2+4H2O |
正极 | O2+4e-+4H+===2H2O |
负极 | CH3OH-6e-+H2O===CO2+6H+ |
碱性燃料电池 | OH- | 总反应:2CH3OH+3O2+4OH-===2C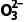 +6H2O +6H2O |
正极 | O2+4e-+2H2O===4OH- |
负极 | CH3OH-6e-+8OH-===C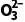 +6H2O +6H2O |
熔融碳酸盐燃料电池 | C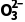 | 总反应:2CH3OH+3O2===2CO2+4H2O |
正极 | O2+4e-+2CO2===2C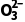 |
负极 | CH3OH-6e-+3C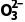 ===4CO2+2H2O ===4CO2+2H2O |
固态氧化物燃料电池 | O2- | 总反应:2CH3OH+3O2===2CO2+4H2O |
正极 | O2+4e-===2O2- |
负极 | CH3OH-6e-+3O2-===CO2+2H2O |
质子交换膜燃料电池 | H+ | 总反应:2CH3OH+3O2===2CO2+4H2O |
正极 | O2+4e-+4H+===2H2O |
负极 | CH3OH-6e-+H2O===CO2+6H+ |

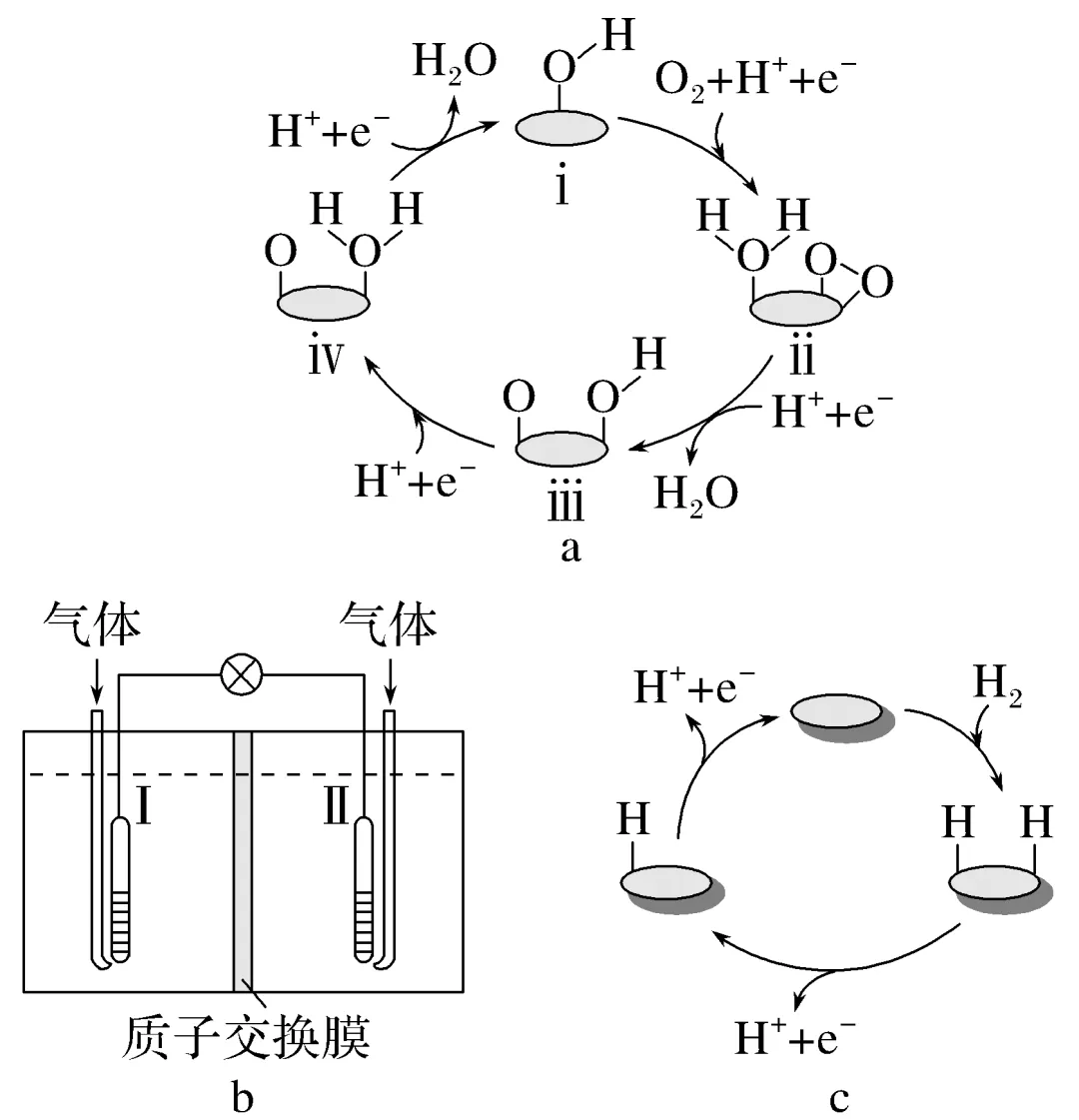
1.(2025·广东,16)某理论研究认为:燃料电池(图b)的电极Ⅰ和Ⅱ上所发生反应的催化机理示意图分别如图a和图c,其中O2获得第一个电子的过程最慢。由此可知,理论上( )
A.负极反应的催化剂是ⅰ
B.图a中,ⅰ到ⅱ过程的活化能一定最低
C.电池工作过程中,负极室的溶液质量保持不变
D.相同时间内,电极Ⅰ和电极Ⅱ上的催化循环完成次数相同
答案 C
解析由图a知,电极Ⅰ发生的反应为O2+4H++4e-===2H2O,故电极Ⅰ作正极,由图c知,电极Ⅱ发生的反应为H2-2e-===2H+,故电极Ⅱ作负极。结合上述分析知,正极反应的催化剂是ⅰ,A错误;由O2获得第一个电子的过程最慢知,ⅰ到ⅱ过程的活化能最高,B错误;H2进入负极失电子生成H+,为保持溶液呈电中性,H+通过质子交换膜向正极迁移,故负极室的溶液质量保持不变,C正确;根据正、负极的电极反应式及得失电子守恒知,相同时间内电极Ⅱ上催化循环完成次数为电极Ⅰ上的2倍,D错误。
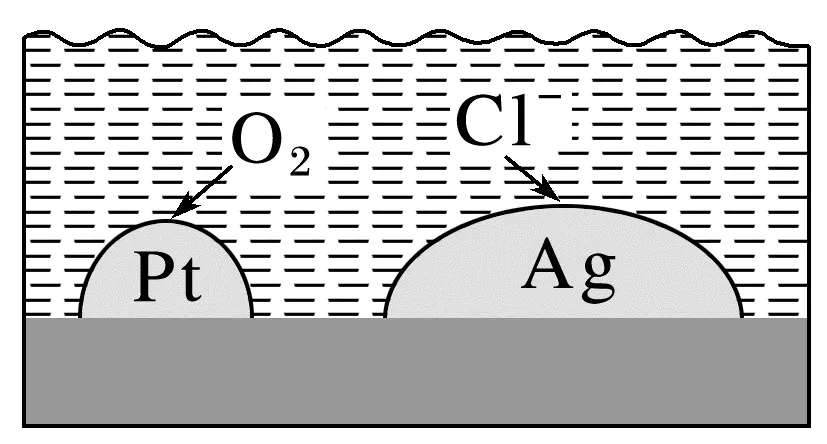
2.(2023·广东,6)负载有Pt和Ag的活性炭,可选择性去除Cl-实现废酸的纯化,其工作原理如图。下列说法正确的是( )
A.Ag作原电池正极
B.电子由Ag经活性炭流向Pt
C.Pt表面发生的电极反应:O2+2H2O+4e-===4OH-
D.每消耗标准状况下11.2 L的O2,最多去除1 mol Cl-
答案 B
解析由题图分析可知,Cl-在Ag极失去电子发生氧化反应,Ag为负极,A错误;电子由负极Ag经活性炭流向正极Pt,B正确;溶液为酸性,故Pt表面发生的电极反应为O2+4H++4e-===2H2O,C错误;每消耗标准状况下11.2L的O2,转移2mol电子,最多去除2molCl-,D错误。
3.(2021·广东,9)火星大气中含有大量CO2,一种有CO2参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时( )
A.负极上发生还原反应
B.CO2在正极上得电子
C.阳离子由正极移向负极
D.将电能转化为化学能
答案 B
解析根据题干信息可知,放电时总反应为4Na+3CO2===2Na2CO3+C。放电时负极上Na失去电子发生氧化反应生成Na+,故A错误;放电时正极上CO2得到电子生成C,故B正确;放电时阳离子移向正极,故C错误;放电时该装置为原电池,将化学能转化为电能,故D错误。
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/1VcNxeHXgbJfoVMtA3SnQAg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享