
(一)钠及其化合物
1.钠及其重要化合物的转化
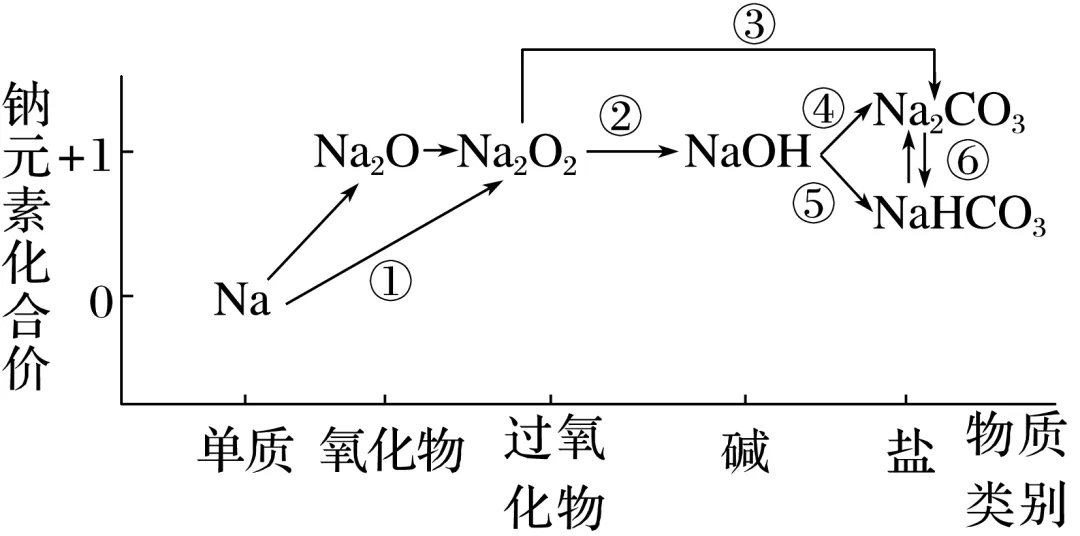
写出图中标号的化学方程式:
①2Na+O2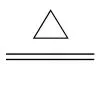 Na2O2;
Na2O2;
②2Na2O2+2H2O===4NaOH+O2↑;
③2Na2O2+2CO2===2Na2CO3+O2;
④2NaOH+CO2(少量) ===Na2CO3+H2O;
⑤NaOH+CO2(过量) ===NaHCO3;
⑥Na2CO3+H2O+CO2===2NaHCO3。
2.重要实验再现
(1)钠与水的反应
实验装置 | 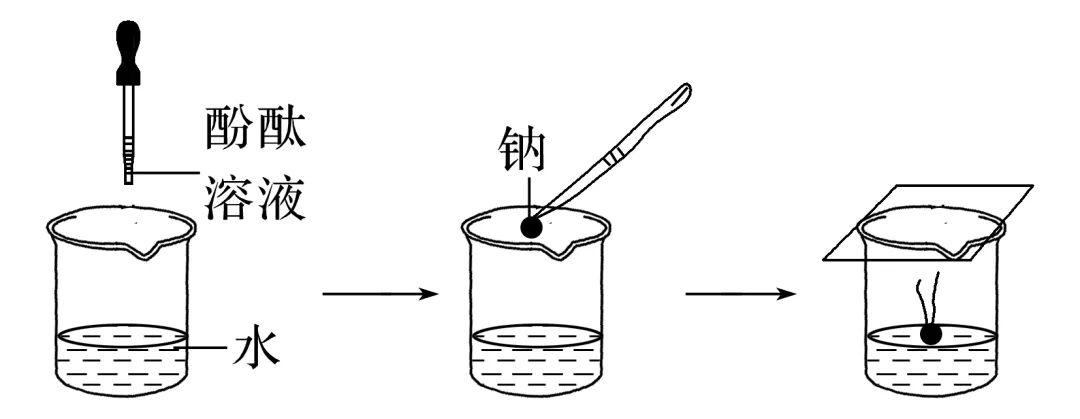
|
实验原理 | 2Na+2H2O===2NaOH+H2↑ |
实验现象 | 钠浮在水面,熔成光亮的小球,在水面上迅速游动,发出“嘶嘶”的响声,钠球在反应中逐渐变小,最后消失,滴有酚酞的溶液变成红色 |
实验结论 | 钠的密度比水小,反应放热且钠的熔点低,反应剧烈,产生H2和NaOH |
实验说明 | ①钠通常保存在煤油中,防止与氧气、水等反应; ②未用完的钠必须放回原试剂瓶; ③金属钠着火,不能用水灭火,可使用专用灭火剂或干砂来灭火 |
(2)过氧化钠与水的反应
实验装置 | 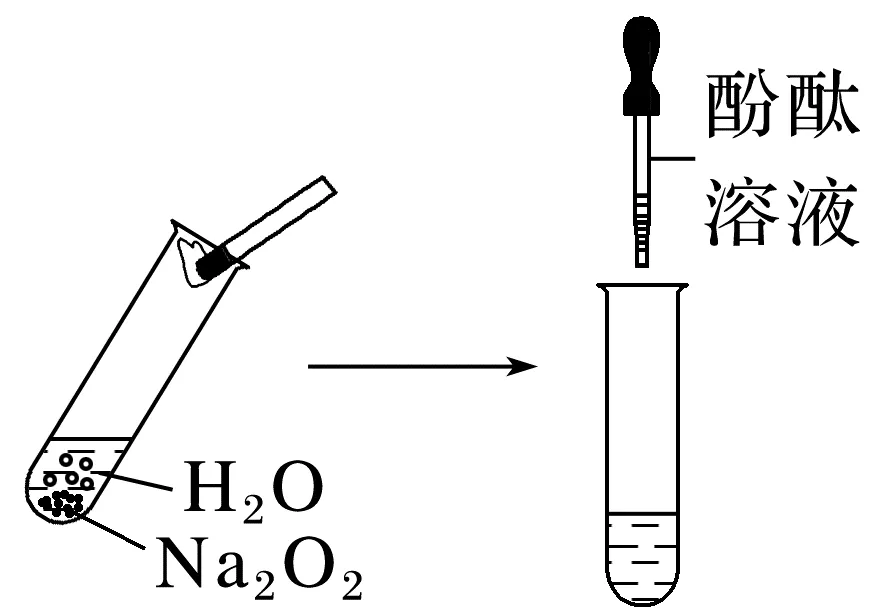
|
实验原理 | 2Na2O2+2H2O===4NaOH+O2↑ |
实验现象 | ①试管中有大量气泡产生,带火星的木条复燃;②试管外壁发热;③滴入酚酞溶液,溶液先变红,后褪色 |
实验结论 | 过氧化钠与水反应产生O2和碱性物质,同时放热,反应生成的物质有漂白性 |
实验说明 | ①向反应后的溶液中加入少量MnO2,产生使带火星的木条复燃的气体,证明反应后的溶液中还有H2O2; ②Na2O2、H2O2均有强氧化性,可作漂白剂,可杀菌消毒,也可使有机色素(酸碱指示剂、花草等)褪色; ③可以利用Na2O2与水反应或H2O2与MnO2反应制备少量氧气 |
(3)探究碳酸钠与碳酸氢钠的溶解性及水溶液的酸碱性
实验 原理 | Na2CO3+H2ONaHCO3+NaOH,NaHCO3+H2OH2CO3+NaOH |
实验 步骤 | 在两支试管里分别加入少量Na2CO3和NaHCO3固体(各约1 g), ①观察二者外观上的细小差别。分别滴入几滴水,振荡试管,将温度计分别插入其中,观察现象; ②继续向①的试管内加入5 mL水,用力振荡,观察现象; ③分别向②所得溶液中滴入1~2滴酚酞溶液,观察现象 |
实验 现象 | Na2CO3为白色粉末,NaHCO3为细小的白色晶体;盛放Na2CO3的试管中温度计示数升高,盛放NaHCO3的试管中温度计示数降低;Na2CO3完全溶解,溶液变红色;NaHCO3部分溶解,溶液变浅红色 |
实验 结论 | ①溶解性:Na2CO3和NaHCO3都能溶于水;溶解度:Na2CO3大于NaHCO3;Na2CO3溶于水放热,NaHCO3溶于水吸热; ②水溶液酸碱性:Na2CO3、NaHCO3水溶液都呈碱性,且碱性:Na2CO3>NaHCO3 |
(4)碳酸钠、碳酸氢钠热稳定性对比实验
实验装置 | 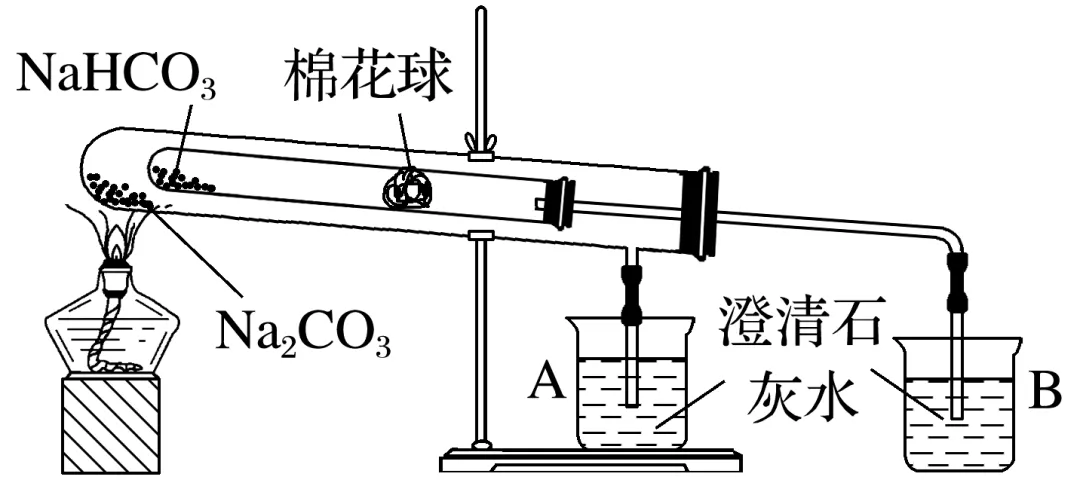
|
实验原理 | 2NaHCO3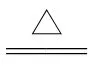 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O |
实验现象 | A烧杯中澄清石灰水变浑浊,B烧杯中澄清石灰水不变浑浊 |
实验结论 | Na2CO3受热不分解;NaHCO3受热易分解,生成物中有CO2 |
3.碱金属的特性及其应用
(1)碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度,所以将锂保存在石蜡油中。由于锂的密度小,制成的锂电池比能量高,所以金属锂是很好的电极材料。
(2)试剂瓶中的药品取出后,一般不能放回原试剂瓶,但Na、K等与水反应的活泼金属需放回原试剂瓶。
(3) Li和O2反应不存在温度的量变引起质变,只生成Li2O。碳酸锂微溶于水,且溶解度随温度升高而降低。
(二)铁及其化合物
1.铁及其重要化合物的转化

写出图中标号的化学方程式:
①2Fe+3Cl2 2FeCl3;
2FeCl3;
②Fe2O3+3CO 2Fe+3CO2或Fe2O3+2Al2Fe+Al2O3;
2Fe+3CO2或Fe2O3+2Al2Fe+Al2O3;
③2FeCl3+Cu===2FeCl2+CuCl2或2FeCl3+Fe===3FeCl2;

通过网盘分享的文件:word讲义【更新联系lymsummers】等2个文件
链接: https://pan.baidu.com/s/1RCL2uLZQuQ-rZUf2_ekrWg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享