
[分值:50分]
(1~10题,每小题5分)
[真题专练]
1.(2025·江苏,8)以稀H2SO4为电解质溶液的光解水装置如图所示,总反应为2H2O2H2↑+O2↑。下列说法正确的是( )
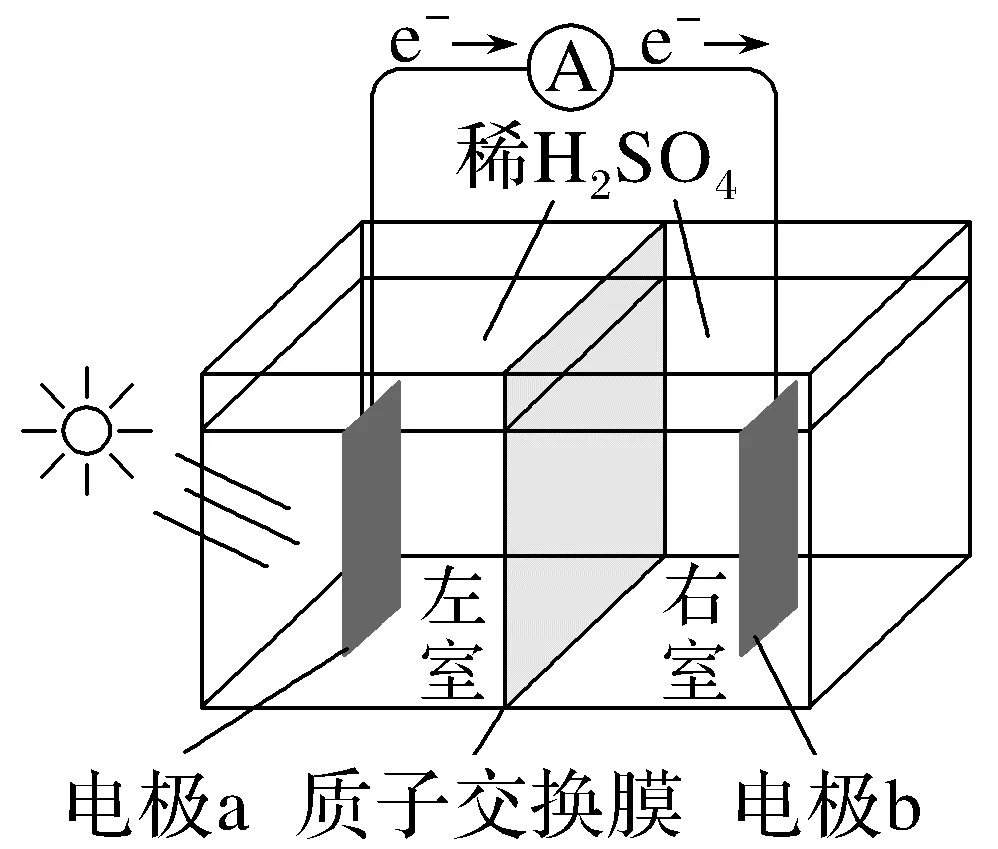
A.电极a上发生氧化反应生成O2
B.H+通过质子交换膜从右室移向左室
C.光解前后,H2SO4溶液的pH不变
D.外电路每通过0.01 mol电子,电极b上产生0.01 mol H2
答案 A
解析由图可知,该原电池中电子由电极a向电极b移动, 故电极a失电子作负极,电极反应式为2H2O-4e-===4H++O2↑;电极b得电子作正极,电极反应式为2H++2e-===H2↑;H+由负极向正极移动。由上述分析可知,电极a上发生氧化反应生成O2,A正确;H+由负极向正极移动,即通过质子交换膜由左室向右室移动,B错误;由总反应可知,光解时消耗水,电解质溶液中硫酸浓度逐渐增大,故溶液pH减小, C错误;由正极反应式可知,电路中每通过0.01mole-,电极b上产生 0.005molH2,D错误。
2.(2025·安徽,13)研究人员开发出一种锂⁃氢可充电电池(如图所示),使用前需先充电,其固体电解质仅允许Li+通过。下列说法正确的是( )
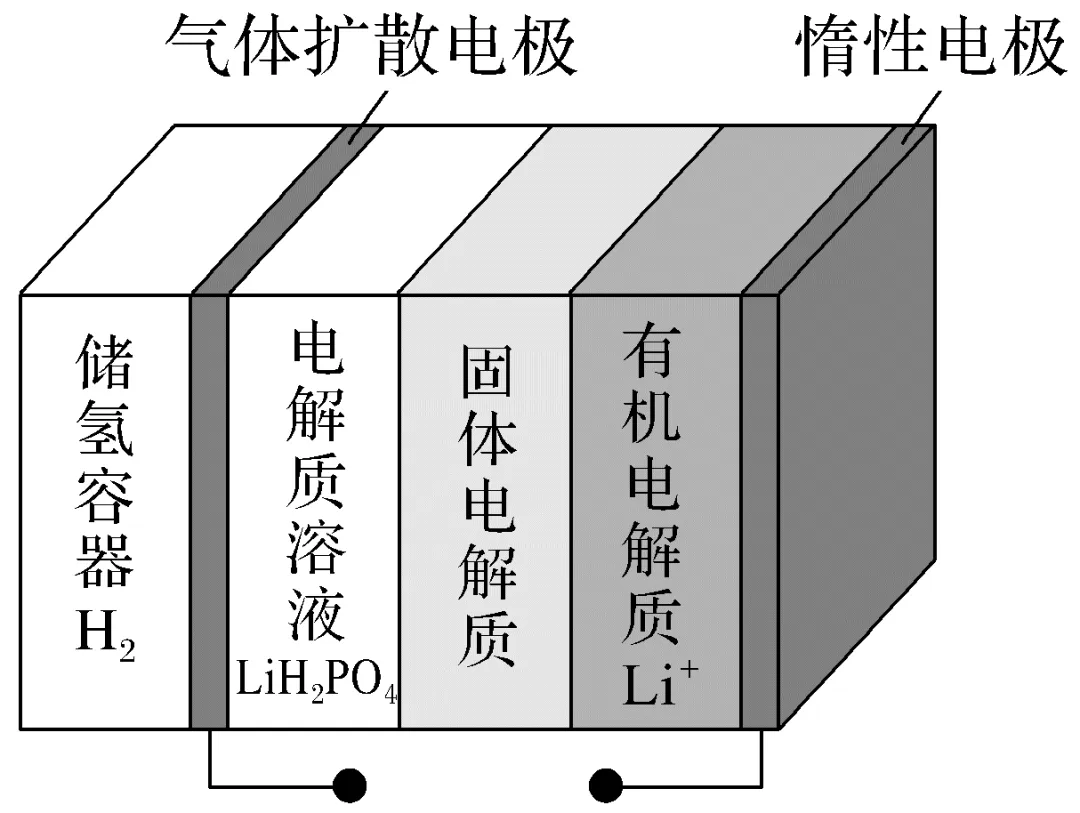
A.放电时电解质溶液质量减小
B.放电时电池总反应为H2+2Li===2LiH
C.充电时Li+移向惰性电极
D.充电时每转移1 mol电子,c(H+)降低1 mol·L-1
答案 C
解析结合锂⁃氢可充电电池装置,再结合题中信息“使用前需先充电”可知,先充电的目的是将惰性电极附近的有机电解质中的Li+转化为Li,故充电时,惰性电极为阴极,其电极反应式为Li++e-===Li;气体扩散电极为阳极,其电极反应式为H2-2e-+2H2P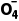 ===2H3PO4。放电时,惰性电极为负极,其电极反应式为Li-e-===Li+;气体扩散电极为正极,其电极反应式为2H3PO4+2e-===H2↑+2H2P
===2H3PO4。放电时,惰性电极为负极,其电极反应式为Li-e-===Li+;气体扩散电极为正极,其电极反应式为2H3PO4+2e-===H2↑+2H2P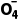 。由放电时正极发生的反应知,每2mol(14g)Li+进入电解质溶液,有1mol(2g)H2扩散到储氢容器,故电解质溶液质量增加,A错误;由正、负极发生的反应知,放电时电池总反应为2Li+2H3PO4===H2↑+2Li++2H2P
。由放电时正极发生的反应知,每2mol(14g)Li+进入电解质溶液,有1mol(2g)H2扩散到储氢容器,故电解质溶液质量增加,A错误;由正、负极发生的反应知,放电时电池总反应为2Li+2H3PO4===H2↑+2Li++2H2P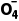 错误;电解池中阳离子移向阴极,故充电时Li+移向惰性电极,C正确;电解质溶液体积未知,且H3PO4是弱酸,故c(H+)不能判断,D错误。
错误;电解池中阳离子移向阴极,故充电时Li+移向惰性电极,C正确;电解质溶液体积未知,且H3PO4是弱酸,故c(H+)不能判断,D错误。
3.(2025·湖南,9)一种电化学处理硝酸盐产氨的工作原理如图所示。下列说法错误的是( )
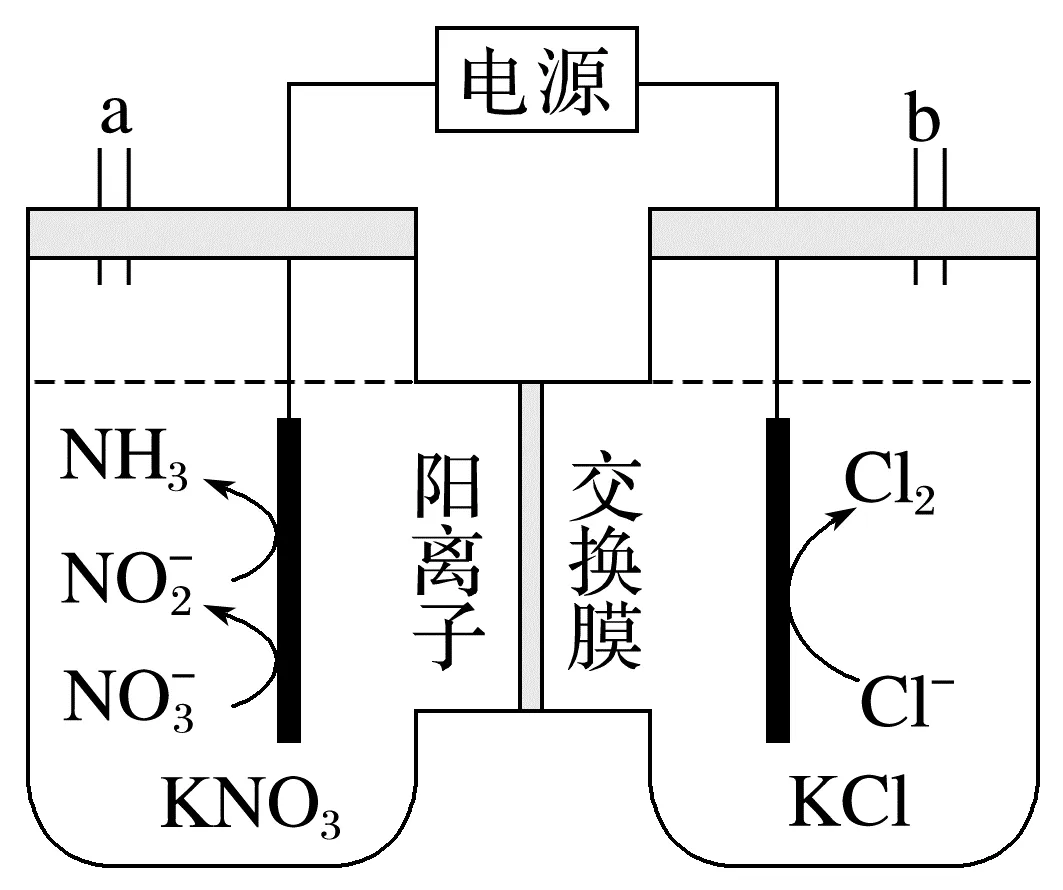
A.电解过程中,K+向左室迁移
B.电解过程中,左室中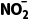 的浓度持续下降
的浓度持续下降
C.用湿润的蓝色石蕊试纸置于b处,试纸先变红后褪色
D.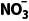 完全转化为NH3的电解总反应:
完全转化为NH3的电解总反应: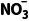 +8Cl-+6H2ONH3↑+9OH-+4Cl2↑
+8Cl-+6H2ONH3↑+9OH-+4Cl2↑
答案 B
解析电解池中,阳离子向阴极移动,则K+向左室迁移,A正确;电解过程中,N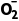 先生成,再消耗,是中间产物,其浓度增大还是减小,取决于其生成速率与消耗速率,无法得出其浓度持续下降的结论,B错误;b处生成氯气,与水反应生成盐酸和次氯酸,盐酸能使蓝色石蕊试纸变红,次氯酸能使变红的试纸褪色,故能看到试纸先变红后褪色,C正确;左侧阴极总反应是
先生成,再消耗,是中间产物,其浓度增大还是减小,取决于其生成速率与消耗速率,无法得出其浓度持续下降的结论,B错误;b处生成氯气,与水反应生成盐酸和次氯酸,盐酸能使蓝色石蕊试纸变红,次氯酸能使变红的试纸褪色,故能看到试纸先变红后褪色,C正确;左侧阴极总反应是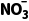 +8e-+6H2O===NH3↑+9OH-,右侧阳极总反应是2Cl--2e-===Cl2↑,将两电极反应相加即可得到总反应,D正确。
+8e-+6H2O===NH3↑+9OH-,右侧阳极总反应是2Cl--2e-===Cl2↑,将两电极反应相加即可得到总反应,D正确。
4.(2025·湖北,15)某电化学制冷系统的装置如图所示。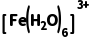 和
和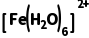 在电极上发生相互转化,伴随着热量的吸收或释放,经由泵推动电解质溶液的循环流动(①→②→③→④→①)实现制冷。装置只通过热交换区域Ⅰ和Ⅱ与环境进行传热,其他区域绝热。下列描述错误的是( )
在电极上发生相互转化,伴随着热量的吸收或释放,经由泵推动电解质溶液的循环流动(①→②→③→④→①)实现制冷。装置只通过热交换区域Ⅰ和Ⅱ与环境进行传热,其他区域绝热。下列描述错误的是( )
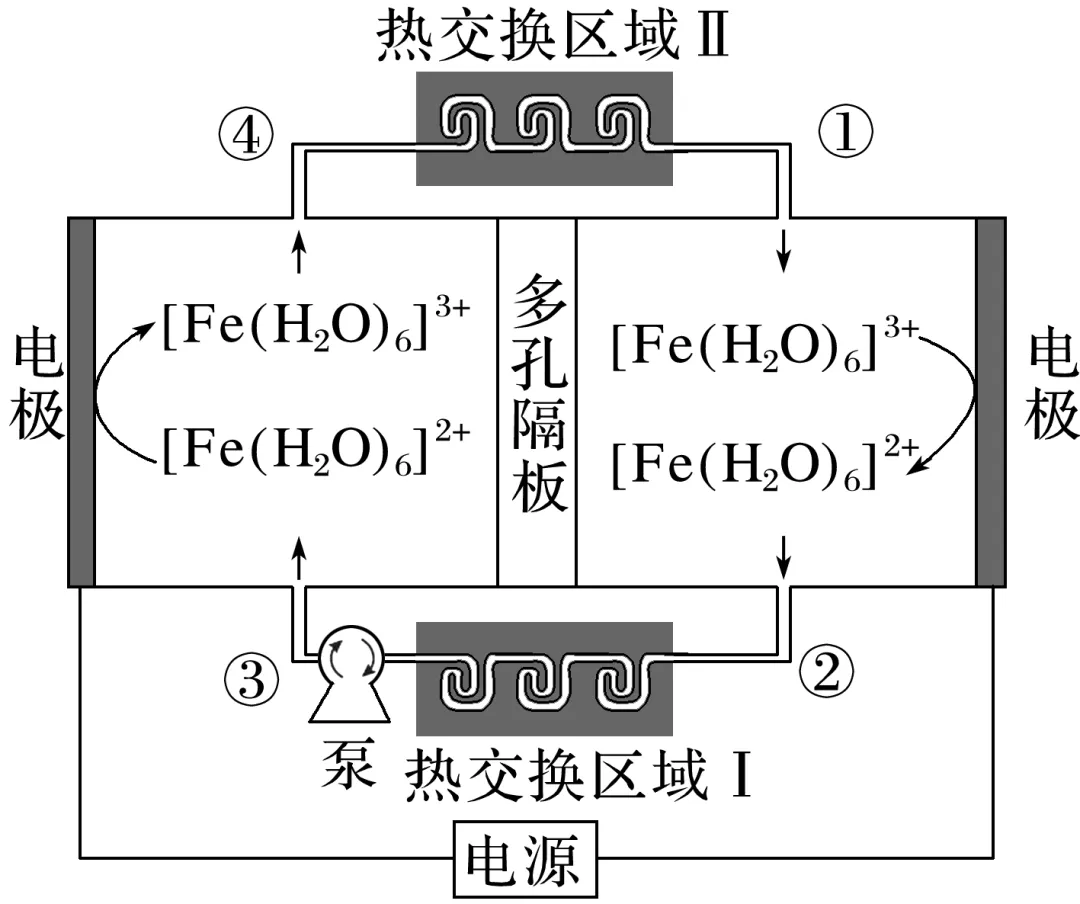
A.阴极反应为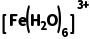 +e-===
+e-===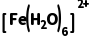
B.已知②处的电解液温度比①处的低,可推断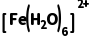 比
比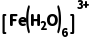 稳定
稳定
C.多孔隔膜可以阻止阴极区和阳极区间的热交换
D.已知电子转移过程非常快,物质结构来不及改变。热效应主要来自于电子转移后[Fe(H2O)6]2+和[Fe(H2O)6]3+离子结构的改变
答案 B
解析由图可知,左侧电极发生反应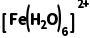 -e-===
-e-===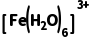 ,则左侧为阳极,右侧电极反应为
,则左侧为阳极,右侧电极反应为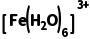 +e-===
+e-===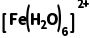 ,则右侧电极为阴极,A正确;②处的电解液温度比①处的低,则可推断
,则右侧电极为阴极,A正确;②处的电解液温度比①处的低,则可推断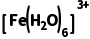 +e-===
+e-===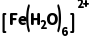 是吸热反应,但无法推断
是吸热反应,但无法推断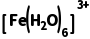 和
和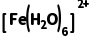 的稳定性,B错误;多孔隔膜可以阻止两电极区的溶液对流,可阻止热交换,C正确;题干明确指出电子转移过程非常快,物质结构来不及改变,这意味着电子转移(即氧化还原反应)本身不会直接导致结构变化,热效应实际上来源于电子转移完成后,新生成的离子
的稳定性,B错误;多孔隔膜可以阻止两电极区的溶液对流,可阻止热交换,C正确;题干明确指出电子转移过程非常快,物质结构来不及改变,这意味着电子转移(即氧化还原反应)本身不会直接导致结构变化,热效应实际上来源于电子转移完成后,新生成的离子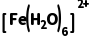 和
和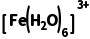 因配位环境或电荷分布变化引起的结构重组导致的热量变化,D正确。
因配位环境或电荷分布变化引起的结构重组导致的热量变化,D正确。
[模拟演练]
5.(2025·南京二模)暖贴是一种便捷的自发热保暖产品,具有发热快、持续时间久等优点。它主要由铁粉、活性炭、食盐、水等成分组成,如图所示。下列有关说法不正确的是( )
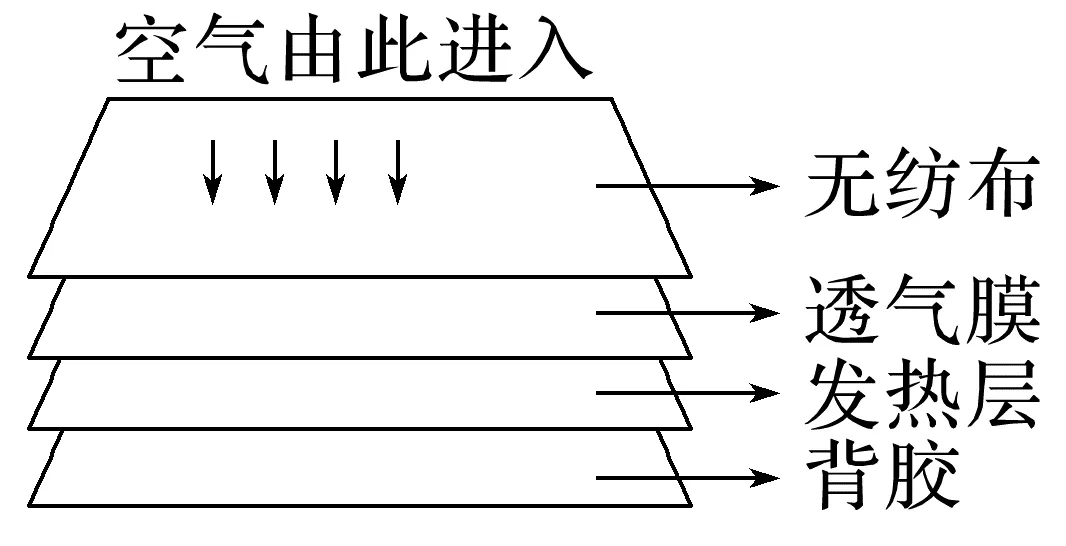
A.暖贴生效时,将化学能转化为热能
B.水与食盐、活性炭共同作用可加快铁粉的腐蚀速率
C.正极反应式为2H2O+2e-===H2↑+2OH-
D.透气膜的透氧速率可控制暖贴的发热时间和温度
答案 C
解析暖贴发热料中的铁粉、活性炭、食盐及水之间能形成数目庞大的微型原电池,铁作负极,氧气作正极,可加快铁粉的腐蚀速率,正极反应式为2H2O+4e-+O2===4OH-,B正确、C错误;透气膜的透氧速率可控制氧气浓度,故可控制暖贴的发热时间和温度,D正确。
通过网盘分享的文件:word讲义【更新联系lymsummers】等2个文件
链接: https://pan.baidu.com/s/1RCL2uLZQuQ-rZUf2_ekrWg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享