
1.元素金属性、非金属性强弱定性判断
(1)比较元素的金属性
本质 | 元素原子越易失电子,元素的金属性越强 |
判断依据 | 单质与水或酸反应置换出H2越容易(反应越剧烈) | 元素的金属性越强 |
最高价氧化物对应水化物(即氢氧化物)的碱性越强 |
单质的还原性越强(或对应阳离子的氧化性越弱) |
一般来说在金属活动性顺序中位置越靠前 |
(2)比较元素的非金属性
本质 | 元素原子越易得电子,元素的非金属性越强 |
判断依据 | 单质与H2化合越容易,生成的简单气态氢化物越稳定 | 元素的非金属性越强 |
最高价氧化物对应水化物(即最高价含氧酸)的酸性越强 |
单质的氧化性越强(或对应阴离子的还原性越弱) |
特别提醒只有最高价氧化物对应水化物的酸、碱性强弱才可用于比较元素非金属性和金属性强弱。
2.原子(离子)半径比较方法
(1)一看电子层数,最外层电子数相同时,电子层数越多半径越大,例如, r(Li)<r(Na)<r(K)<r(Rb)<r(Cs),r(O2-)<r(S2-)<r(Se2-)。
(2)二看核电荷数,电子层数相同时,核电荷数越小半径越大,例如,r(Na)>r(Mg)>r(Al),r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)。
(3)三看电子数,核电荷数相同时,电子数越多半径越大,例如, r(Fe)>r(Fe2+)>r(Fe3+),r(Cl-)>r(Cl)。
3.元素的电离能
(1)1~36号元素的第一电离能(I1)变化规律
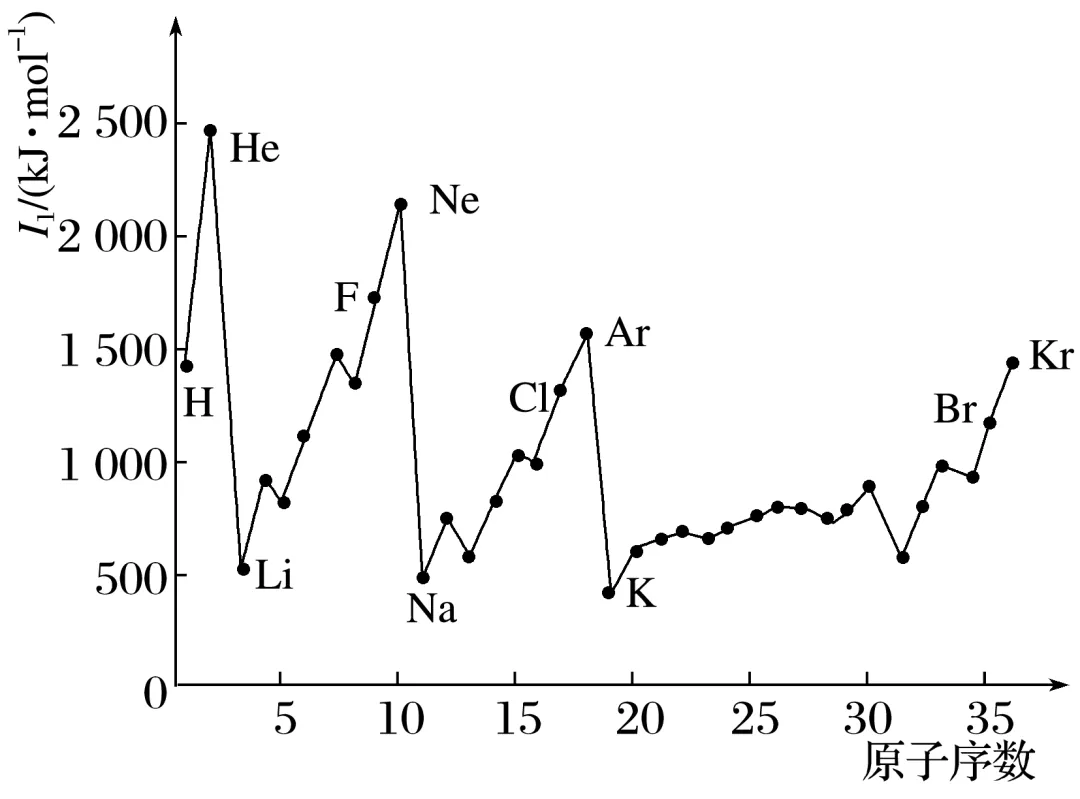
说明①同周期元素从左到右,第一电离能呈增大趋势,第ⅡA、第ⅤA族反常;
②同主族元素从上到下,第一电离能逐渐减小。
(2)应用
①判断元素金属性的强弱
电离能越小,金属越容易失去电子,金属性越强;反之越弱。
②判断元素的化合价
如果某元素的In+1≫In,则该元素的常见化合价为+n价,如钠元素I2≫I1,所以钠元素的常见化合价为+1价。
4.元素的电负性
(1)电负性是描述元素的原子在化合物中吸引电子能力的标度。元素的电负性越大,表示其原子在化合物中吸引电子的能力越强。
(2)变化规律:一般来说,同周期主族元素,从左到右电负性逐渐增大;同主族元素,从上到下电负性逐渐减小。

1.(2025·浙江6月选考,3)根据元素周期律推测,下列说法不正确的是( )
A.原子半径:Mg>Na
B.电负性:C>Si
C.非金属性:Br>I
D.热稳定性:NH3>PH3
答案 A
解析同周期主族元素,从左往右原子半径依次减小,则原子半径:Mg <Na,A< span>错误;C和Si位于第ⅣA族,同主族元素从上到下电负性逐渐减小,则电负性:C>Si,B正确;Br和I位于第ⅦA族,同主族元素从上到下非金属性逐渐减弱,则非金属性:Br>I,C正确;N和P位于第ⅤA族,非金属性:N>P,故热稳定性:NH3>PH3,D正确。 </Na,A<>
2.(2025·浙江1月选考,4)根据元素周期律,下列说法不正确的是( )
A.第一电离能:N>O>S
B.化合物中键的极性:SiCl4>PCl3
C.碱性:LiOH>KOH
D.化合物中离子键百分数:MgO>Al2O3
答案 C
解析同一周期从左往右元素的第一电离能呈增大趋势,但第ⅡA与ⅤA族反常,故第一电离能:N>O>S,A正确;同一周期从左往右元素的电负性依次增大,电负性:Si <P<Cl< span>,电负性差值越大,键的极性越大,故化合物中键的极性:SiCl4>PCl3,B正确;同一主族从上往下元素的金属性依次增大,金属性:Li <K< span>,故碱性:LiOH <KOH,C< span>错误;电负性:Mg <Al< span>,故Mg与O的电负性差值>Al与O的电负性差值,电负性差值越大离子键百分数越大,故化合物中离子键百分数:MgO>Al2O3,D正确。</Al<> </KOH,C<> </K<> </P<Cl<>
3.(2023·天津,11)下表列出25 ℃时不同羧酸的pKa(即-lg Ka)。根据表中的数据推测,结论正确的是( )
羧酸 | CH3COOH | CH2FCOOH | CH2ClCOOH | CH2BrCOOH |
pKa | 4.76 | 2.59 | 2.87 | 2.90 |
A.酸性强弱:CH2ICOOH>CH2BrCOOH
B.对键合电子的吸引能力强弱:F <Cl<Br< span> </Cl<Br<>
C.25 ℃时的pKa大小:CHF2COOH <CH< span>2FCOOH </CH<>
D.25 ℃时0.1 mol·L-1溶液的碱性强弱:CH3COONa <CH< span>2ClCOONa </CH<>
答案 C
解析根据电负性:F>Cl>Br>I,CH2FCOOH、CH2ClCOOH、CH2BrCOOH的酸性逐渐减弱,则酸性:CH2ICOOH <CH< span>2BrCOOH,A错误;电负性越大,对键合电子的吸引能力越强,电负性:F>Cl>Br,对键合电子的吸引能力强弱:F>Cl>Br,B错误;F是吸电子基团,F原子个数越多,吸电子能力越强,使得羧基中O—H极性增强,更易电离,酸性增强,则25℃时的pKa大小:CHF2COOH <CH< span>2FCOOH,C正确;根据pKa知,相同浓度下酸性:CH3COOH <CH< span>2ClCOOH,酸性越强,其对应盐的水解程度越弱,碱性越弱,则相同浓度下碱性:CH2ClCOONa <CH< span>3COONa,D错误。 </CH<> </CH<> </CH<> </CH<>
4.[Zn(CN)4]2-含有配位键,其中参与配位的原子是(填“碳原子”或“氮原子”),理由是。
答案 碳原子 CN-中碳、氮原子都含有孤电子对,但碳原子的电负性比氮原子小,更易提供孤电子对形成配位键
5.NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是。
答案 N>H>B
解析 NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),说明N的电负性强于H,B的电负性弱于H,故电负性:N>H>B。
通过网盘分享的文件:word讲义【更新联系:lymsummers】等2个文件
链接: https://pan.baidu.com/s/10SY5y2aMVnchrA2xx-JUuQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享