堪比“作弊”的复习资料!26济南中考化学高频考点+必背方程式,想拿满分赶紧打印!
- 2026-05-11 19:08:35
堪比“作弊”的复习资料!26济南中考化学高频考点+必背方程式,想拿满分赶紧打印!

02 化学用语 1. 元素名称及符号 (1)前二十号元素(5个一组,记忆更方便) 



(2)补充元素9种 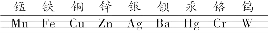
【注意事项】 书写元素符号时,元素符号由一个字母表示的必须大写,由两个字母表示的第一个必须大写,第二个必须小写。 2. 离子名称及符号 (1)常见的离子 氢离子:H+ 钠离子:Na+ 钾离子:K+ 钙离子:Ca2+ 镁离子:Mg2+ 铜离子:Cu2+ 亚铁离子:Fe2+ 铁离子:Fe3+ 铝离子:Al3+ 氯离子:Cl- (2)常见的原子团 
3. 化学式的书写 (1)固态非金属单质 硅:Si 磷:P 硫:S 碘:I2 碳:C 硼:B (2)气态非金属单质 氢气:H₂ 氮气:N₂ 氧气:O₂ 氦气:He (3)金属氧化物 氧化镁:MgO 氧化铜:CuO 氧化汞:HgO 氧化钙:CaO 氧化铝:Al₂O₃ 二氧化锰:MnO₂ 氧化铁:Fe₂O₃ 四氧化三铁:Fe3O4 (4)非金属氧化物 水:H₂O 一氧化碳:CO 二氧化碳:CO₂ 二氧化氮:NO₂ 二氧化硫:SO₂ 五氧化二磷:P2O5 过氧化氢:H₂O₂ (5)酸 盐酸:HCl 硫酸:H2SO4 硝酸:HNO3 碳酸:H2CO3 (6)碱 氢氧化钠:NaOH 氢氧化钙:Ca(OH)₂ 氢氧化钾:KOH 氢氧化镁:Mg(OH)₂ 氢氧化铜:Cu(OH)₂ 氢氧化铁:Fe(OH)₃ 氨水:NH₃·H₂O (7)盐 氯化盐氯化钠:NaCl 氯化钾:KCl 氯化银:AgCl 氯化铵:NH4Cl 氯化钙:CaCl₂ 氯化钡:BaCl₂ 氯化铜:CuCl₂ 氯化亚铁:FeCl₂ 氯化铁:FeCl₃ 氯化铝:AlCl₃ 硫酸盐硫酸钠:Na2SO4 硫酸钡:BaSO4 硫酸铜:CuSO4 硫酸亚铁:FeSO4 硫酸镁:MgSO4 碳酸(氢)盐碳酸钠:Na₂CO₃ 碳酸钙:CaCO₃ 碳酸钾:K₂CO₃ 碳酸钡:BaCO₃ 碳酸氢钠:NaHCO₃ 硝酸盐硝酸银:AgNO₃ 硝酸钡:Ba(NO₃)₂ 硝酸铵:NH4NO₃ 硝酸铁:Fe(NO₃)₃ 其他盐高锰酸钾:KMnO4 锰酸钾:K2MnO4 (8)有机物 甲烷:CH4 乙醇:C2H5OH 4. 化合价的标注 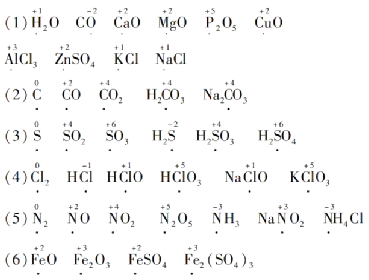
5. 化学式的意义及相关计算 (1)化学式的意义 ①由分子构成的物质(以C2H5OH为例) 宏观意义: a.表示一种物质 (表示乙醇这种物质) b.表示物质的元素组成(表示乙醇是由碳、氢、氧三种元素组成的) 微观意义: a.表示该物质的一个分子(表示一个乙醇分子) b.表示该物质一个分子的构成 [表示一个乙醇分子由9个原子(或2个碳原子、6个氢原子和1个氧原子)构成] ②由原子构成的物质(以Fe为例) 宏观意义: a.表示一种物质(表示铁这种物质) b.表示物质的元素组成(表示铁由铁元素组成) 微观意义:表示该物质的一个原子 (表示一个铁原子) (2)化学式的相关计算 
以C2H5OH为例 ①计算相对分子质量C2H5OH的相对分子质量为12×2+1×6+16×1=46 ②计算物质中各元素的原子个数比C2H5OH中碳、氢、氧三种元素的原子个数比为2∶6∶1 ③计算物质中各元素的质量比C2H5OH中,mC:mH:mO=(12×2)∶(1×6)∶(16×1)=12∶3∶8 ④计算某元素的质量分数如:求C2H5OH中碳元素的质量分数= 
⑤计算物质中某元素的质量如100 g C2H5OH中碳元素的质量=100 g×52.2%=52.2 g 6. 化学符号周围数字的含义 (1)符号前数字的含义:nM ①M为元素符号,一般表示n个M原子 ②M为化学式,除由原子直接构成的物质外,一般表示n个M分子 ③M为离子符号,一般表示n个M离子如:2H中的“2”表示2个氢原子;8H2O中的“8”表示8个水分子;2Fe3+中的“2”表示2个铁离子。 (2)下角标数字的含义 表示一个分子中含有该原子的个数如:H2O中的“2”表示1个水分子中含有2个氢原子;P2O5中的“5”表示1个五氧化二磷分子中含有5个氧原子。 (3)符号右上角数字的含义 表示离子或原子团所带的电荷数如:Fe²+中的“2”表示1个亚铁离子带2个单位的正电荷;S²﹣=﹣中的“2”表示1个硫离子带2个单位的负电荷;CO₃²﹣中的“2”表示1个碳酸根离子带2个单位的负电荷。 (4)符号正上方数字的含义 表示某元素在该微粒中所显的化合价 
03 基本实验操作 1. 常见仪器的识别 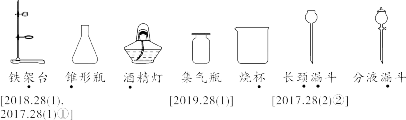
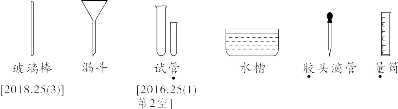
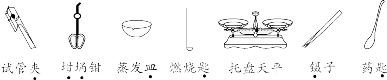
2. 基本实验操作 (1) 药品的取用原则 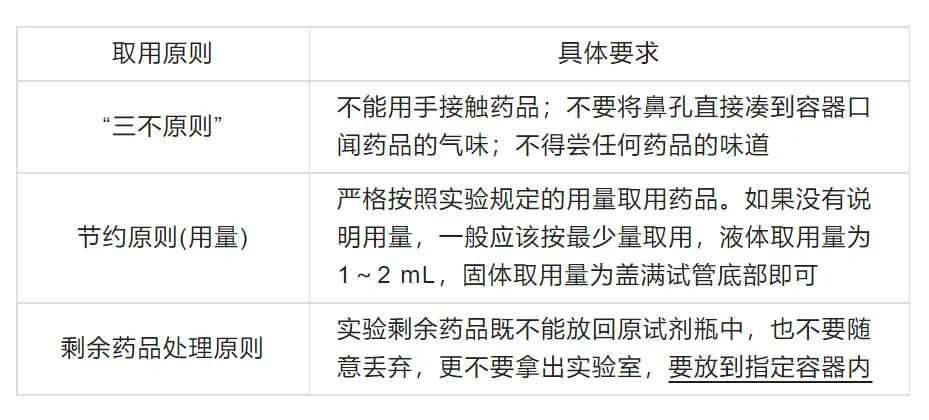
(2)闻药品的气味 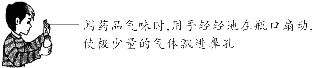
(3)固体药品的取用 
(4)天平的使用 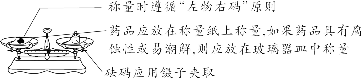
【特别提醒】 ①托盘天平的称量值只能精确到小数点后一位;若称量时药品与砝码位置放反且使用了游码,则药品的实际质量=砝码质量-游码读数。 ②称量一定质量的固体时,天平指针偏右,接下来的操作是继续加固体至天平平衡;称量某物质的质量时,天平指针偏左,接下来的操作是加砝码或移动游码。 (5)倾倒液体 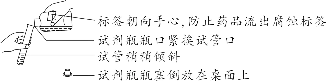
(6)用滴管滴加液体 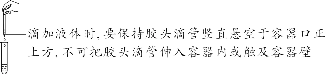
【注意事项】 ①取液后的胶头滴管应保持橡胶胶帽在上,不要平放或倒放,防止液体倒流,污染试剂或腐蚀橡胶胶帽; ②用过的胶头滴管要立即用清水冲洗干净(滴瓶上的滴管不用冲洗),严禁用未经清洗的胶头滴管再吸取其他试剂。 (7)用量筒量取一定量的液体 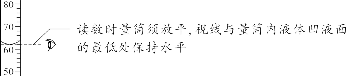
【注意事项】 ①量筒的选择:a.选择比量取液体体积稍大的量筒,且越接近越好,减少误差;b.保证只量取一次; ②量筒不能用作反应容器或配制溶液的容器。 (8)酒精灯的使用 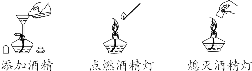
【注意事项】 ①绝对禁止向燃着的酒精灯里添加酒精,以免引起失火; ②绝对禁止用燃着的酒精灯引燃另一只酒精灯; ③用完酒精灯后,必须用灯帽盖灭,不可用嘴吹灭。 (9)固体的加热 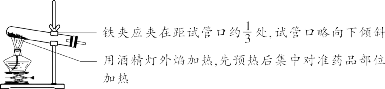
【补充】 可能导致试管炸裂的操作有: ①加热完药品的试管,立即用冷水冲洗; ②加热液体药品时,用酒精灯直接对准药品部位进行加热; ③加热药品前,没有擦干试管外壁的水。 (10)液体的加热 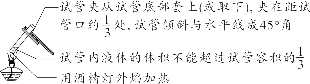
(11)仪器的连接 
(12)检查装置的气密性 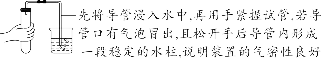
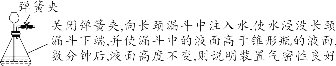
【特别提醒】 检查装置的气密性一般在组装仪器之后,装入药品之前。 (13)仪器的洗涤 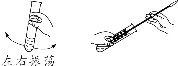

【特别提醒】 刷洗时须转动或上下移动试管刷,但不能用力过猛,以防损坏试管。洗净的标准:洗过的仪器内壁附着的水既不聚成水滴,也不成股流下时,表明仪器已洗干净。 (14)稀释浓硫酸 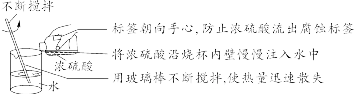
(15)过滤 ①目的:用于固态与液态混合物的分离 ②主要仪器:漏斗、烧杯、玻璃棒、铁架台(带铁圈) 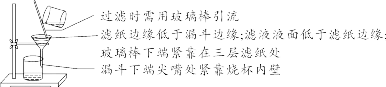
【注意事项】 若两次过滤后滤液仍然浑浊,原因可能是滤纸破损或过滤时漏斗内液面高于滤纸边缘等。 (16)蒸发 ①目的:将溶液进行浓缩,提取溶质。 ②主要仪器:蒸发皿、酒精灯、玻璃棒、铁架台、坩埚钳 ③操作要点 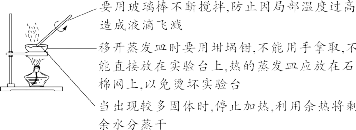
(17)测定溶液的pH 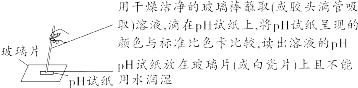
【特别提醒】 若要测定固体物质的酸碱性,应先取适量固体物质于烧杯中,加蒸馏水、搅拌、静置得到其饱和溶液,然后用测定溶液pH的方法进行测定。 (18)实验室意外事故的处理措施 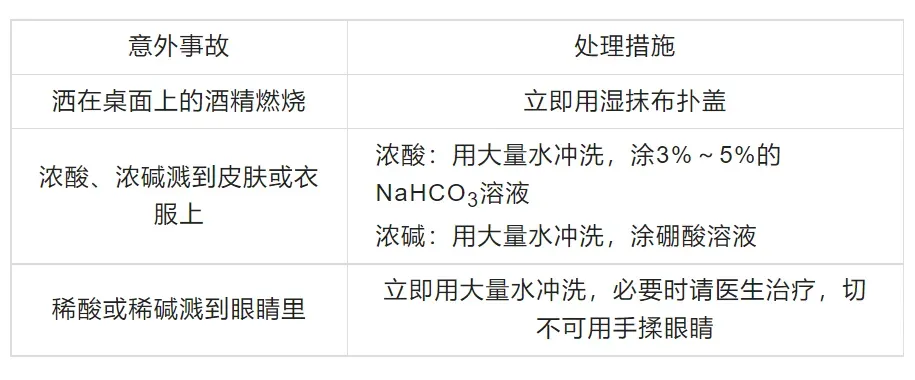
04 氧气和二氧化碳的实验室制取 1. 实验原理 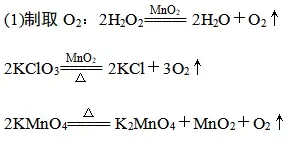
【巧记】 谁含“Mn”不加“MnO₂”,不含“Mn”加“MnO₂”;固体要“加热”,液体“不加热”。 (2)制取CO2:CaCO3+2HCl=== CaCl2+H2O+CO2↑ 2. 发生装置 (1)固体加热型 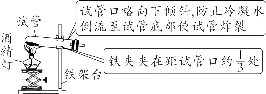
举例:实验室用高锰酸钾或氯酸钾制O2。 【注意事项】 用KMnO4制取氧气时,试管口要塞一团棉花,以防止加热时高锰酸钾粉末随氧气流进入导管,堵塞导管。 (2)固液不加热型 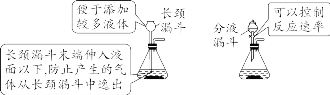
举例:实验室用大理石或石灰石与稀盐酸反应制CO2;用双氧水制O2。 3.收集装置 (1)排空气法:操作简单,收集到的气体比较干燥但纯度不高。 
适用范围 ①无毒无害,不与空气中各成分发生反应,且密度与空气密度相差较大的气体 ②密度比空气大的气体(如O₂、CO₂),用向上排空气法(如图1) ③密度比空气小的气体(如H₂、NH₃),用向下排空气法(如图2) (2)排水法:难溶或不易溶于水,且不与水反应的气体,排水法收集的气体纯度较高,但含有一定量的水蒸气。 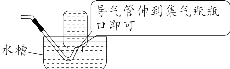
【注意事项】 a.排水法收集氧气的最佳时机:当导管口有气泡连续均匀冒出时开始收集; b.用加热装置制取气体时,实验结束后要先从水槽中取出导管再熄灭酒精灯,以防止水倒流造成试管炸裂; c.用排水法收集氧气时,观察到有大气泡从瓶口冒出,应该在水面下用玻璃片盖住瓶口,把集气瓶移出水槽,再将集满氧气的集气瓶正放在桌面上。 4.检验和验满 (1)O2的检验和验满 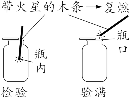
(2)CO2的检验和验满 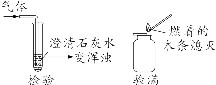
5. 气体的净化与干燥 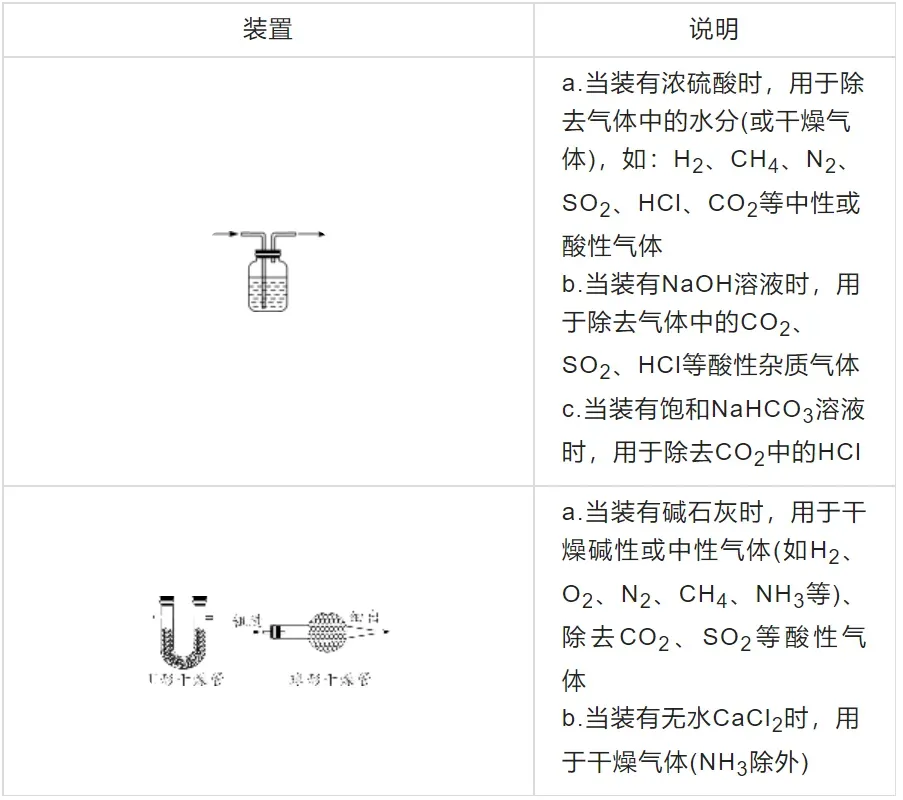
6.多功能瓶 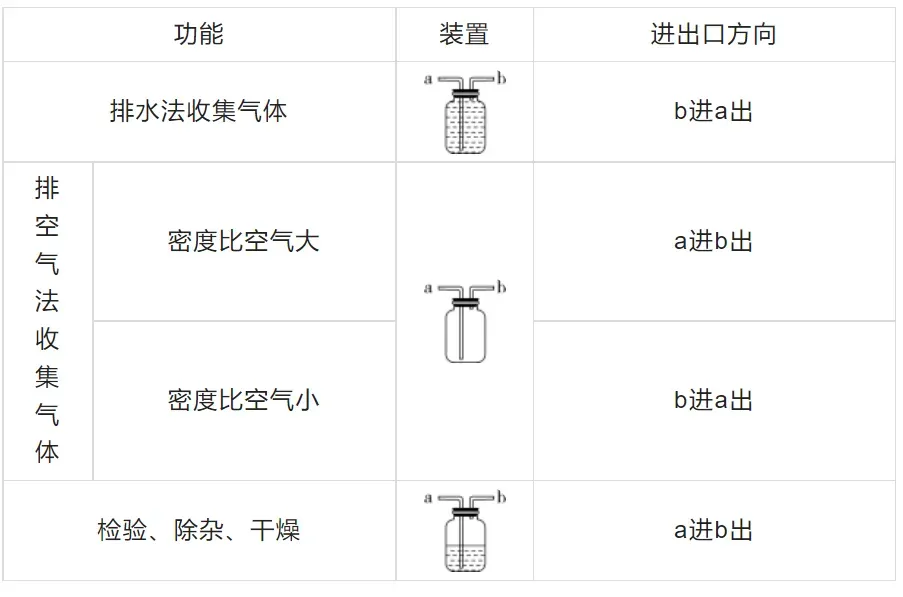
05 推断题题眼 1. 物质的颜色 (1) 固体的颜色 ①黑色:铁粉、炭粉(C)、CuO、MnO2、Fe3O4 ②红色:Fe2O3(或红棕色)、Cu(或紫红色)、红磷 ③暗紫色:KMnO4 (2) 溶液的颜色 ①蓝色⇔含Cu2+的溶液,如:CuSO4、Cu(NO3)²等溶液 ②浅绿色⇔含Fe²+的溶液,如:FeCl₂、FeSO4等溶液 ③黄色⇔含Fe³+的溶液,如:FeCl₃、Fe(NO₃)₃、Fe₂(SO4)₃等溶液 ④紫红色⇔含MnO-4的溶液,如KMnO4溶液 (3)沉淀的颜色 ①蓝色沉淀:Cu(OH)₂ ②白色沉淀(5种):BaSO4、AgCl、CaCO3、BaCO3、Mg(OH)2 【注意】不溶于稀硝酸的白色沉淀(2种):BaSO4、AgCl 溶于酸并有气体放出的白色沉淀(2种):CaCO3、BaCO3 溶于酸但没有气体放出的白色沉淀(1种):Mg(OH)2 ③红褐色沉淀:Fe(OH)3 2. 物质的俗称/主要成分 (1)物质的俗称 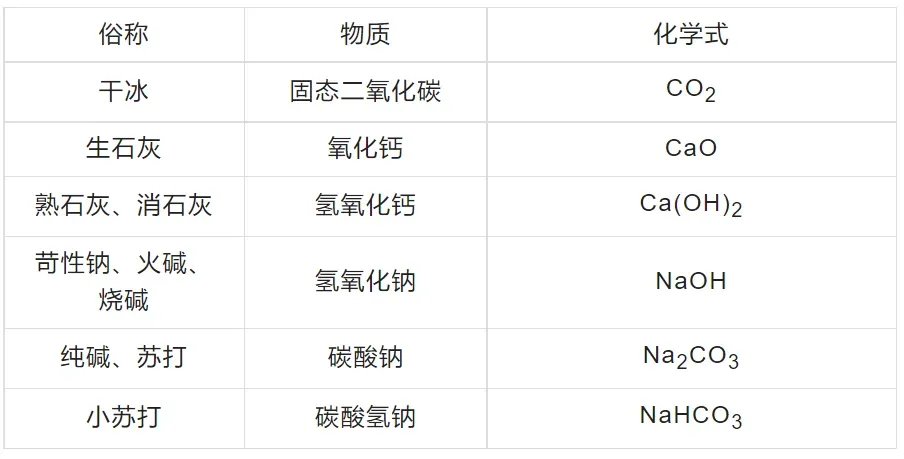
(2)主要成分 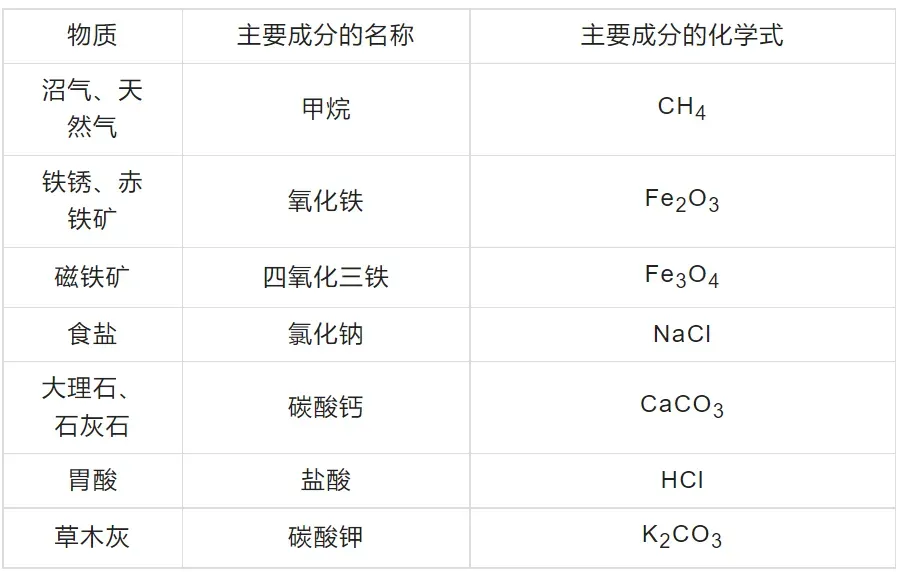
3. 物质的性质与用途 (1)单质 ①能供给呼吸、支持燃烧、能使带火星木条复燃的气体是O2。 ②可作食品保护气的是N2。 ③可用作理想清洁燃料的是H2。 ④具有还原性,可用于冶炼金属的气体是H2。 ⑤可用作食品干燥剂(脱氧剂)的是铁粉。 ⑥具有导电性、能用作电池电极的是石墨。 ⑦质软、可用于制铅笔芯的是石墨。 ⑧硬度大、可用于裁玻璃的是金刚石。 【补充】具有吸附性,可用于净水、能除去冰箱中异味的是活性炭(主要成分为碳单质)。 (2)氧化物 ①可用作光合作用的原料、常用作灭火剂、制作汽水、固态可用于人工降雨的是CO₂。 ②会导致温室效应,能使澄清石灰水变浑浊的气体是CO₂。(2015.25) ③具有还原性,可用于冶炼金属的气体是CO。(2014.25) ④可作燃料且极易与血液中血红蛋白结合的有毒气体是CO。 ⑤与水具有相同元素组成且有消毒杀菌作用的液体是H₂O₂。 ⑥常用作食品干燥剂的是CaO。 (3)酸、碱、盐 ①常用于金属表面除锈的物质是稀盐酸(HCl)、稀硫酸(H₂SO4)。(2018.27) ②胃酸的主要成分,可帮助消化的是盐酸(HCl)。 ③可作干燥剂且具有脱水性的是浓H2SO4。 ④常用来改良酸性土壤的是熟石灰[Ca(OH)2]。 ⑤实验室用来检验二氧化碳的试剂是澄清石灰水[Ca(OH)2]。 ⑥可用作干燥剂的碱是NaOH。 ⑦炉具清洁剂的主要成分是NaOH。 ⑧可用作补钙剂的是CaCO3。 ⑨常用作调味品、配制生理盐水的是NaCl。 ⑩工业上广泛用于玻璃、造纸、纺织和洗涤剂生产的是Na2CO3。 ⑪用于焙制糕点、发酵粉的主要成分是NaHCO3。⑫用作建筑材料的是CaCO3、Ca(OH)2。 ⑬用于配制波尔多液的是Ca(OH)2和CuSO4。 ⑭用于治疗胃酸过多的是Al(OH)3、Mg(OH)2、NaHCO3。 4. 物质和元素之最 (1)物质之最 ①日常生活中应用最广泛的金属、目前世界上年产量最高的金属、提取量最大的金属:Fe ②人类最早使用的金属:Cu ③空气中体积分数最大(含量最多)的气体:N₂ ④最理想的清洁燃料、相对分子质量最小的单质、密度最小的气体:H₂ ⑤天然存在最硬的物质:金刚石 ⑥最常用的溶剂、最常见的无色、无味的液体:H₂O ⑦相对分子质量最小的氧化物:H₂O ⑧人体中含量最多的物质:H₂O ⑨最简单的有机物:CH4 (2) 元素之最 ①地壳中含量最高的元素:O ②形成化合物种类最多的元素:C ③地壳中含量最高的金属元素:Al ④人体中含量最多的金属元素:Ca 5. 组成元素相同/含同一种元素的物质 ★组成元素相同的物质 (1)氧化物 ①液体(无色液体):H₂O₂和H₂O ②气体:CO₂和CO ③固体:Fe₂O₃和Fe3O4 (2)盐 FeCl2和FeCl3、FeSO4和 Fe2(SO4)3等 ★含同一种元素的物质 (1)常见含有相同的非金属元素的物质 ①C⇐⇒C、CO、CO₃、CaCO₃ ②O⇐⇒O₂、H₂O、H₂O₂、CaCO₃ ③H⇐⇒H₂、H₂O、H₂O₂、HCl (2)常见含有相同的金属元素的物质 ①Fe⇐⇒Fe、Fe₂O₃、Fe3O4、FeCl3[或Fe2(SO4)3]、FeCl2(或FeSO4)、Fe(OH)3 ②Cu⇐⇒Cu、CuO、Cu(OH)2、CuCl2(或CuSO4) ③Ca⇐⇒CaO、Ca(OH)2、CaCO3 ④Na⇐⇒NaCl、NaOH、Na2CO3、NaHCO3 6. 特殊反应条件 (1)反应过程较为复杂:铁生锈 
(5)催化剂:H₂O₂分解、KClO₃分解 06 初中常见化学方程式 类型一 实验室制取气体 
现象:在空气中燃烧发出微弱的淡蓝色火焰,在氧气中燃烧发出明亮的蓝紫色火焰;相同点:放出热量,生成有刺激性气味的气体。 8. 红磷(或白磷)在氧气中燃烧 
现象:发出蓝色火焰。 类型2 有二氧化碳参与的反应 13. 二氧化碳与澄清石灰水[Ca(OH)2溶液]反应CO₂+Ca(OH)₂=== CaCO₃↓+H₂O 现象:澄清石灰水变浑浊。 应用:检验二氧化碳. 14. 二氧化碳与氢氧化钠反应CO₂+2NaOH=== Na₂CO₃+H₂O 15. 二氧化碳与水反应(使紫色石蕊溶液变红的原因):CO₂+H₂O=== H₂CO₃ 16. 二氧化碳与碳在高温条件下反应 类型5 金属与酸、盐溶液的反应 Ⅰ. 金属与酸反应(置换反应)条件:金属的活动性必须排在氢之前。 17. 锌与稀硫酸反应Zn+H2SO4=== ZnSO4+H2↑Zn+2HCl=== ZnCl2+H2↑ 现象:有气泡产生。 18. 铁与稀酸反应Fe+2HCl=== FeCl₂+H₂↑Fe+H2SO4=== FeSO4+H2↑ 现象:有气泡产生,溶液变为浅绿色。 19. 镁与稀硫酸反应Mg+H2SO4=== MgSO4+H2↑ 现象:有气泡产生.Ⅱ. 金属与盐溶液的反应(置换反应) 条件:①金属单质的活动性排在盐溶液中金属之前(K、Ca、Na除外);②盐必须可溶。 20. 铁与铜盐溶液反应Fe+CuSO4=== FeSO4+CuFe+CuCl2=== FeCl2+CU 现象:有红色固体析出,溶液由蓝色变为浅绿色。 21. 铜与硝酸银溶液反应Cu+2AgNO3=== Cu(NO3)2+2Ag 现象:有银白色固体析出,溶液由无色变为蓝色。 22. 锌与硫酸铜反应:Zn+CuSO4=== ZnSO4+Cu 现象:有红色固体析出,溶液由蓝色变为无色。 23. 铝与硫酸亚铁反应:2Al+3FeSO4=== Al2(SO4)3+3Fe 现象:溶液由浅绿色变为无色。 类型3 金属氧化物与酸的反应 24. 氧化铁与酸(稀盐酸、稀硫酸)反应(除铁锈)Fe₂O₃+6HCl=== 2FeCl₃+3H₂OFe₂O₃+3H₂SO4=== Fe2(SO4)3+3H2O 现象:红棕色粉末逐渐减少,溶液由无色变为黄色 25. 氧化铜与酸(稀盐酸、稀硫酸) 反应:CuO+ 2HCl=== CuCl2+H2OCuO+H2SO4=== CuSO4+H2O现象:黑色粉末逐渐减少,溶液由无色变为蓝色。 类型4 酸、碱、盐之间的反应 酸与碱反应通式:酸+碱―→ 盐+H₂O 26. 稀盐酸与氢氧化钠反应:HCl+NaOH=== NaCl+H₂O 27. 稀硫酸与氢氧化铜反应:H2SO4+Cu(OH)2=== CuSO4+2H2O 28. 稀盐酸与氢氧化钙反应:2HCl+Ca(OH)₂=== CaCl₂+2H₂O 29. 稀盐酸与氢氧化镁反应:2HCl+Mg(OH)₂=== MgCl₂+2H₂O 30. 稀硫酸与氢氧化钡反应:H2SO4+Ba(OH)2=== BaSO4↓+2H₂O 稀硫酸与氢氧化钠反应:H₂SO4+2NaOH===Na2SO4+H2O 稀硫酸与氢氧化钾反应:H2SO4+2KOH===K2SO4+H₂O 酸与盐反应通式:酸+盐→ 新酸+新盐 31. 稀盐酸与硝酸银反应HCl+AgNO3=== AgCl↓+HNO₃ 32. 稀硫酸与氯化钡反应H2SO4+BaCl2=== BaSO4↓+2HCl 33. 稀盐酸与碳酸钠反应2HCl+Na₂CO₃=== 2NaCl+CO₂↑+H₂O 34. 稀硫酸与碳酸钠反应:H2SO4+Na2CO3=== Na2SO4+H₂O+CO₂↑ 稀盐酸与碳酸氢钠HCl+2NaHCO₃===Na₂CO₃+HCl+CO₂↑ 碱与盐反应通式:碱+盐―→ 新碱+新盐条件(发生原因):反应物均可溶,有沉淀或气体生成 35. 氢氧化钙(熟石灰)与碳酸钠(纯碱)反应Ca(OH)₂+Na₂CO₃=== CaCO₃↓+2NaOH 36. 氢氧化钠与硫酸铜反应2NaOH+CuSO4=== Na₂SO4+Cu(OH)₂↓ 37. 氢氧化钠与氯化铜反应2NaOH+CuCl₂=== Cu(OH)₂↓+2NaCl 38. 氢氧化钠与氯化铁反应:3NaOH+FeCl₃=== Fe(OH)3↓+3NaCl 39. 氢氧化钡与硫酸钠反应:Ba(OH)₂+Na₂SO4=== BaSO4↓+2NaOH 盐与盐反应通式:盐1+盐2―→ 新盐1+新盐2 反应条件(发生原因):反应物均可溶,有沉淀生成 40. 碳酸钠与氯化钙反应Na₂CO₃+CaCl₂= CaCO₃↓+2NaCl 41. 碳酸钠与氯化钡反应:Na₂CO₃+BaCl₂= BaCO₃↓+2NaCl 42. 氯化钠与硝酸银反应:NaCl+AgNO₃=AgCl↓+NaNO₃ 43. 硫酸钠与氯化钡反应:Na2SO4+BaCl₂=== BaSO4↓+2NaCl 类型5 其他反应 45. 氧化钙与水反应(放出热量)CaO+H₂O=== Ca(OH)₂ 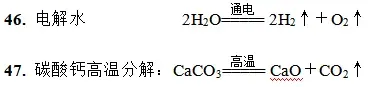
49. 碳酸分解H₂CO₃===H₂O+CO₂↑ 
END 
精彩内容 

点分享 
点收藏 
点在看 
点点赞

01
初中化学重要人物及其成就





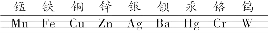

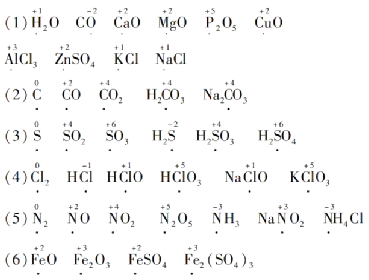



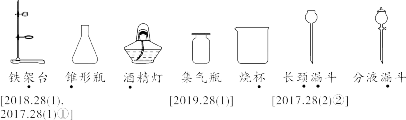
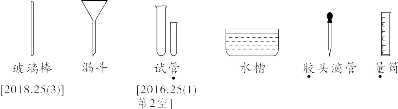
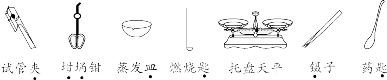

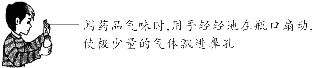

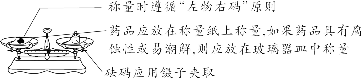
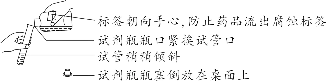
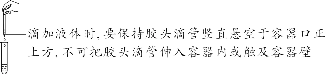
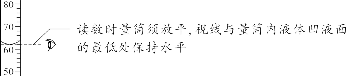
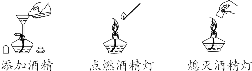
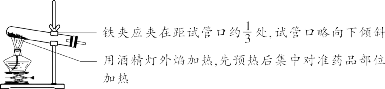
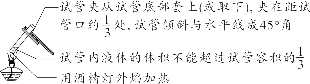

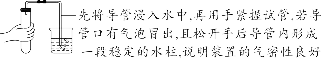
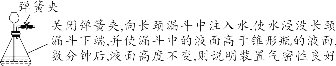
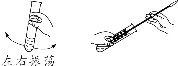

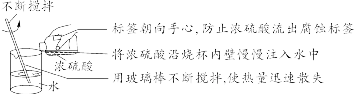
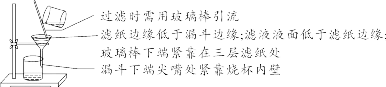
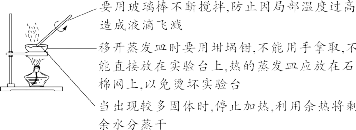
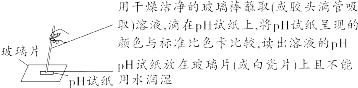

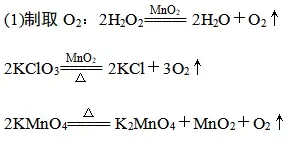
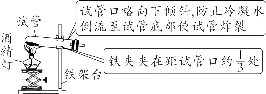


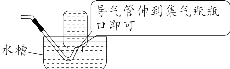

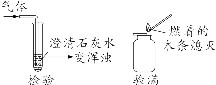







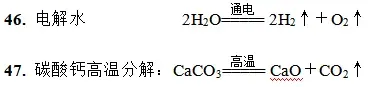

注:本文来源于网络,由济南天材初中圈汇总整理,贵在分享,如有侵权,联系删除。


官宣!多省地生会考开卷不计分,济南会跟进吗?文末附30天冲刺攻略!





本文来自网友投稿或网络内容,如有侵犯您的权益请联系我们删除,联系邮箱:wyl860211@qq.com 。
